首页 > 医疗资讯/ 正文
在接受开腹腹部手术的患者中,术后肺部并发症(PPCs)较为常见,且与较差的预后相关。在多种适应证中,微创腹腔镜腹部手术正日益取代开腹手术,且近年来这类手术常由机器人辅助完成。
已有研究表明,接受机器人辅助手术(RAS)患者的PPCs发生率高于接受包括传统腹腔镜手术(CLS)在内的非机器人辅助手术的患者。RAS患者PPCs发生率升高的原因可能在于手术持续时间更长,导致术中通气时间延长;此外,RAS中患者需采取极端体位,可能损害呼吸系统力学功能,进而需要更高强度的通气支持(即更高的驱动压(DP)和/或通气机械功率(MP)),而这也可能增加PPCs的发生风险。
为更深入了解传统腹腔镜与机器人辅助腹腔镜腹部手术患者的PPCs发生率及相关影响因素,研究者对两项全球前瞻性研究(全麻手术期间通气管理局部评估研究[LASVEGAS])与机器人手术全麻期间通气管理及其对术后肺部并发症影响的评估研究[AVATaR])的个体患者数据进行了标准化处理与合并,建立了一个新的汇总数据库——腹腔镜与机器人辅助手术(LapRAS)数据库。
2025年9月17日,JAMA Surgery刊发该研究的结果。该研究基于LapRAS数据库进行预先计划的汇总分析,旨在比较传统腹腔镜与机器人辅助腹腔镜腹部手术术后PPCs的发生率,并确定哪些患者相关、手术相关及麻醉相关因素与PPCs相关。研究者假设,两种手术方式下PPCs发生率的差异与通气持续时间的差异关联性更强,而非与机械通气强度的差异相关。

方法
研究设计与伦理审批
本队列研究是对两项多中心观察性研究(LASVEGAS与AVATaR)的个体患者数据分析。这两项研究的方案均已获得协调中心机构审查委员会的伦理批准。根据国家法规要求,在必要时获取了患者的书面知情同意书。
研究对象
LASVEGAS与AVATaR两项研究具有共同的纳入标准:年龄≥18岁、因择期或非择期手术接受全麻并需有创通气。本研究数据来源于2013年1月至2019年3月期间,美洲、欧洲、中东和北非31个国家163个中心的患者。
本分析额外排除了以下患者:LASVEGAS研究中未接受腹腔镜手术的患者、从CLS或RAS转为开腹手术的患者、术前近期接受过通气治疗的患者、通气数据集不完整导致无法计算通气强度的患者,以及PPCs随访数据不完整的患者。
患者分类
未接受机器人辅助的CLS患者被归类为CLS组,接受机器人辅助手术的患者被归类为RAS组。无患者同时接受CLS和RAS。
结局指标
主要结局指标:术后前5天内发生1种及以上PPCs。PPCs定义为出现以下至少1种临床情况:新发急性呼吸窘迫综合征、肺炎、气胸、急性呼吸衰竭、需氧疗,以及术后需有创或无创机械通气。两项研究中采用的详细定义具有一致性。
次要结局指标:各类单独PPCs的发生情况、住院时间(LOS),以及术后28天的住院死亡率。
定义与计算
基于汇总数据库的患者基线特征,计算体重指数(BMI)、预计体重,以及加泰罗尼亚外科患者呼吸风险评估(ARISCAT)评分。分别评估机械通气强度、手术持续时间与麻醉持续时间。
采用3种不同的候选指标评估机械通气强度(均与特定时间点向肺部输送的机械能量相关,与手术持续时间无关):驱动压(DP)、驱动压的4倍加上呼吸频率(4DP+RR),以及机械功率(MP)。
驱动压(DP)计算:在容量控制通气模式下,DP=平台压(Pplat)-呼气末正压(PEEP);在压力控制通气模式下或未采用呼气末暂停的容量控制通气模式下,DP=最大吸气压(Pinsp)-PEEP。
机械功率(MP)计算:容量控制通气模式下,采用简化公式:机械功率(MP)(焦耳/分钟)=0.098×潮气量×呼吸频率×(平台压-0.5×驱动压);压力控制通气模式下或未采用呼气末暂停的容量控制通气模式下,公式为:机械功率(MP)(焦耳/分钟)=0.098×潮气量×呼吸频率×(最大吸气压-0.5×驱动压)
非手术通气时间:定义为术中通气持续时间减去手术持续时间,即患者术前准备或苏醒期间接受机械通气的时间。
样本量
本研究未进行正式样本量计算,纳入患者数量基于可获得的患者数据确定。观察到的PPC事件总数决定了纳入逻辑回归模型的协变量最大数量,遵循“每10个观察到的PPC事件最多纳入1个协变量”的原则。此外,研究团队对主要混合效应逻辑回归模型进行了基于模拟的事后检验效能分析:通过生成200个模拟数据集,估算检测术中通气持续时间效应的效能,并确定在90%效能下通气强度的最小可检测比值比(OR)。
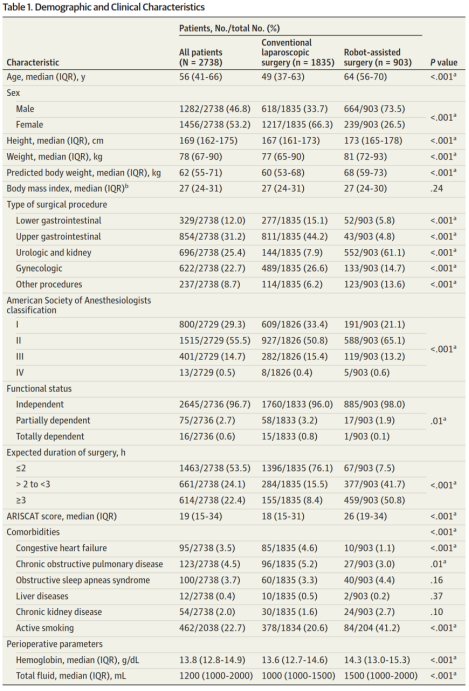
表1 患者人口统计学和临床特征
结果
LASVEGAS研究共9864例患者,AVATaR研究共905例患者,本分析最终纳入2738例患者(中位年龄[IQR]:56[41-66]岁;女性1456例,占53.1%),其中CLS组1835例,RAS组903例。排除原因主要包括:非腹腔镜手术或转为开腹手术、通气数据缺失或PPCs随访数据缺失。患者基线特征汇总于表1。RAS组的ARISCAT评分中位数(IQR)高于CLS组(26[19-34] vs 18[15-31])。
结局指标
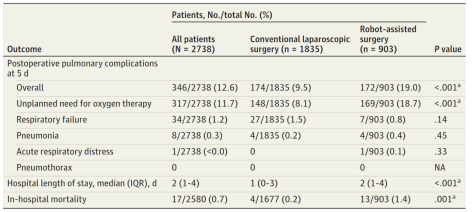
术后5天内,RAS组903例患者中172例(19.0%)发生PPCs,CLS组1835例患者中174例(9.5%)发生PPCs(未校正P<0.001)。各类PPCs的详细发生情况见表2。RAS组住院时间(LOS)中位数(IQR)长于CLS组(2[1-4]天 vs 1[0-3]天,未校正P<0.001)。RAS组未校正死亡率同样高于CLS组(13例,1.4% vs 4例,0.2%,未校正P=0.001)(表2)。
表2 患者临床结局
机械通气强度与持续时间
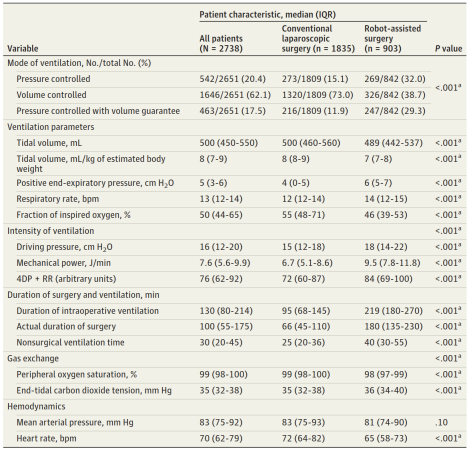
与CLS组相比,RAS组患者通气潮气量更小,但呼气末正压(PEEP)、呼吸频率(RR)、吸气压及平台压更高(表3),导致通气强度更高:驱动压(DP)中位数(IQR)为18[14-22]cm H₂O vs 15[12-18]cmH₂O(P<0.001);机械功率(MP)中位数(IQR)为9.5[7.8-11.8]焦耳/分钟 vs 6.7[5.1-8.6]焦耳/分钟(P<0.001);4DP+RR中位数(IQR)为84[69-100] vs 72[60-87](P<0.001)(累积分布曲线见图A-C,详细数据见表3)。
RAS组的术中通气持续时间(中位数[IQR]:219[180-270]分钟 vs 95[68-145]分钟,P<0.001)、手术持续时间(中位数[IQR]:180[135-230]分钟 vs 66[45-110]分钟,P<0.001)及非手术通气时间(中位数[IQR]:40[30-55]分钟 vs 25[20-36]分钟,P<0.001)均长于CLS组(累积分布曲线见图D-F,详细数据见表3)。RAS组中,225例患者(25.0%)的非手术通气时间超过55分钟。
表3 患者术中临床变量
多变量模型
单变量逻辑回归分析显示,与CLS相比,RAS与PPCs发生相关(未校正OR:2.12,95%CI:1.33~3.38,P=0.001)。根据Akaike信息准则(AIC),最优模型纳入术中通气持续时间与4DP+RR指标。
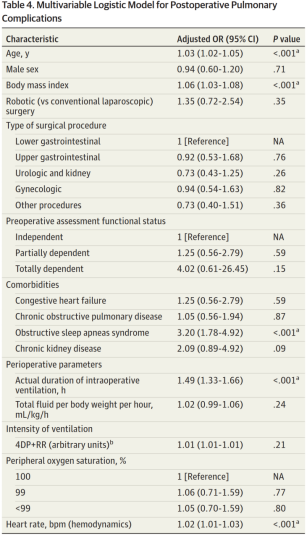
多变量分析显示,以下因素与PPCs存在独立关联:年龄(aOR:1.03,95%CI:1.02~1.05,P<0.001)、BMI(aOR:1.06,95%CI:1.03~1.08,P<0.001)、阻塞性睡眠呼吸暂停综合征(aOR:3.20,95%CI:1.78~4.92,P<0.001)及术中通气持续时间(aOR:1.49,95%CI:1.33~1.66,P<0.001);而手术方式(即RAS vs CLS,aOR:1.35,95%CI:0.72~2.54,P=0.35)及以4DP+RR评估的通气强度(aOR:1.01,95%CI:1.01~1.01,P=0.21)与PPCs无独立关联(表4)。
事后检验效能分析显示,本研究检测术中通气持续时间与PPCs关联的效能为99%;在当前样本量下,以90%效能可检测到的4DP+RR(通气强度)最小比值比(OR)为1.01。
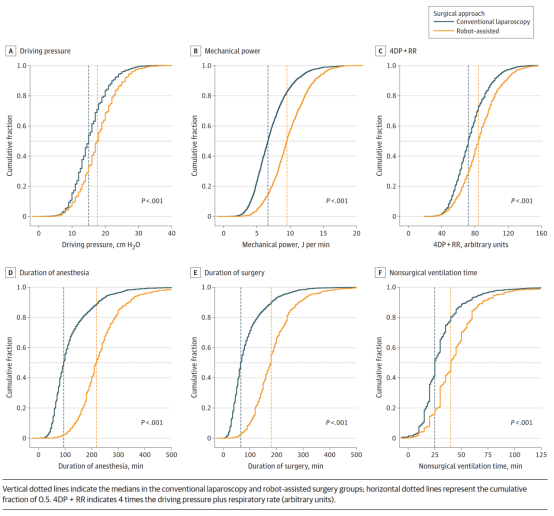
图通气强度与通气持续时间相关指标的累积分布曲线
预先计划的敏感性分析
多变量中介分析结果显示,RAS与CLS对PPCs的直接关联无统计学意义;术中通气持续时间介导了RAS与PPCs的表观关联(ACME:1.04,95%CI:1.02~1.05,P<0.001),而4DP+RR无介导作用(ACME:1.00,95%CI:1.00~1.00,P=0.33)。
在1772例术中通气持续时间匹配的患者亚组与1174例4DP+RR匹配的患者亚组中,多变量模型结果保持一致:仅术中通气持续时间与PPCs存在独立关联,而4DP+RR或手术方式(RAS vs CLS)均无此关联。
住院时间(LOS)回归模型分析证实,LOS与通气持续时间相关(OR 1.43,95%CI:1.35~1.50),而与4DP+RR或手术方式(RAS vs CLS)无关(补充资料1中的表e17)。
事后分析
在主要多变量模型中加入4DP+RR与术中通气持续时间的交互项后,主效应结果未改变,但交互项与术中通气持续时间本身在多变量逻辑模型中均达到统计学意义,提示通气强度与PPCs的关联程度可能因手术持续时间不同而存在差异。
表4 术后肺部并发症的多变量逻辑回归模型
结论
与接受传统腹腔镜手术的患者相比,接受机器人辅助手术的患者未校正PPCs发生率更高,且接受机械通气的时间更长、强度更大;然而,仅通气持续时间与PPCs的发生存在独立关联,通气强度或手术方式类型均无此关联。
麻海新知的述评
随着微创外科技术的普及,机器人辅助手术(RAS)凭借操作精准度高、术者疲劳度低等优势,在腹部外科领域的应用占比逐年攀升。然而,术后肺部并发症(PPCs)作为围术期常见不良事件,不仅延长患者住院时间、增加医疗成本,更与术后30天死亡率显著相关。该研究则首次明确“术中通气持续时间”是介导RAS与PPCs关联的核心因素,而非手术方式本身或通气强度。该研究为理解RAS相关PPCs的发病机制提供了关键证据,也为临床优化围术期通气管理指明了方向。
该研究在设计与分析层面有下述三个重要亮点。首先,多中心大样本数据支撑,结果外推性强。研究整合了两项全球前瞻性队列研究(LASVEGAS与AVATaR)的个体患者数据,覆盖美洲、欧洲、中东及北非31个国家163个中心,最终纳入2738例患者,是目前针对“腹腔镜vs机器人辅助手术PPCs”样本量最大的研究之一。大样本与广泛的地域代表性有效降低了选择偏倚,使得“RAS组PPCs发生率(19.0%)显著高于CLS组(9.5%)”这一基线发现更具临床普适性。
其次,统计分析设计精巧,精准解析了因果关联。针对“通气时间、通气强度、手术方式”三者间的复杂关系,研究采用了层层递进的统计策略:首先通过混合效应逻辑回归控制中心聚类效应与基线混杂(如年龄、BMI、合并症);其次通过Akaike信息准则(AIC)解决通气时间与强度的共线性问题,筛选出最优评估指标组合(术中通气持续时间+4DP+RR);最终通过中介分析与匹配队列分析(1:1最近邻匹配)证实:仅通气持续时间与PPCs存在独立关联(aOR=1.49,95%CI1.33~1.66),而手术方式(aOR=1.35,P=0.35)与通气强度(aOR=1.01,P=0.21)均无独立影响[2]。这一设计巧妙排除了“手术方式直接导致PPCs”的误区,明确了“RAS→通气时间延长→PPCs升高”的因果链条,填补了既往研究“知其然不知其所以然”的空白。
最后,临床问题聚焦明确,首次揭示“时间介导”机制。既往研究多关注RAS与PPCs的关联性,或孤立探讨通气强度(如驱动压、机械功率)的影响,而该研究首次将“手术方式-通气参数-PPCs”纳入统一分析框架,提出“通气持续时间是核心中介因素”的创新结论。更具临床价值的是,其事后分析发现“通气强度的影响依赖手术时长”:在短时间手术中,通气强度与PPCs的关联性更显著;而在长时间手术中,通气时间的主导作用掩盖了强度的影响。这一发现为不同时长手术的通气策略个体化调整提供了重要依据。
尽管该研究设计精良,但仍需客观看待其局限性,这些局限也正是未来研究需突破的重点。一方面,关键混杂因素数据缺失,可能影响结论精准度。研究未收集外科医生操作经验、气腹压力、患者体位细节(如RAS常用的头低足高位程度)等数据。已有研究证实,气腹压力升高会增加胸膜腔内压、降低肺顺应性,而RAS中极端体位可能进一步加重呼吸力学紊乱;此外,外科医生学习曲线长短可能影响手术时长,进而间接影响通气时间。这些未纳入的变量可能存在残余混杂,需在后续研究中补充评估。另一方面,观察性研究设计局限,难以确立因果关系。作为基于现有数据库的二次分析,该研究仅能提供“关联证据”,无法证实“缩短通气时间可降低RAS相关PPCs”的因果推断。例如,通气时间延长可能与RAS手术的技术复杂性(如泌尿外科手术占比高,达61.1%)直接相关,而手术类型本身也可能影响PPCs风险,尽管研究已校正手术类型,但仍无法完全排除其与通气时间的交互作用。
总之,该研究的核心价值不仅在于明确了通气时间的中介作用,更在于其对临床实践的“纠偏”意义——长期以来,围术期通气管理的重点多集中于“强度控制”(如限制驱动压<15cmH₂O、采用肺保护性通气),而该研究提示:在RAS这类长时间手术中,“时间控制”可能比“强度控制”更重要。结合现有证据,可从两方面深化对这一主题的认知。
1. 通气管理策略的“个体化调整”:基于手术时长的分层思维
研究的事后分析为临床提供了重要启示:短时间手术(如<2小时CLS)中,需重点控制通气强度(如避免高驱动压),而长时间手术(如>3小时RAS)中,应优先缩短通气时间。针对RAS这类长时间手术,未来可能需要将“通气时间控制”纳入ERAS(加速康复外科)流程,例如通过术前优化设备准备、术中提高手术效率、术后缩短苏醒期通气时间,以降低PPCs风险。
2. 手术方式选择的“风险-获益平衡”:不能忽视的临床决策维度
尽管RAS在操作精准度、术后疼痛控制等方面具有优势,但该研究提示其PPCs风险升高的核心症结是通气时间延长。因此,在选择手术方式时,需结合患者个体情况(如年龄、肺功能储备、手术类型)综合评估。例如,对于肺功能较差的老年患者,若CLS可满足手术需求,应优先选择以缩短通气时间;而对于复杂手术(如机器人辅助根治性前列腺切除术),则需通过优化通气管理(如缩短非手术通气时间、采用个体化PEEP)来抵消通气时间延长的风险。
总体而言,该研究通过严谨的方法学设计,首次揭示了“术中通气持续时间”在RAS与PPCs关联中的中介作用,为理解这一临床难题提供了全新视角。其核心价值不仅在于回答了“RAS为何PPCs发生率更高”的问题,更在于为临床实践指明了方向——在RAS围术期管理中,“缩短通气时间”应成为与“控制通气强度”同等重要的优先级。未来需通过前瞻性干预试验验证这一结论,并结合多学科协作,将“时间控制”理念融入标准化流程,最终实现RAS技术优势与围术期安全的有机统一。
原文:
Serafini SC, Hemmes SNT, Queiroz VNF, et al. Postoperative Pulmonary Complications in Conventional Laparoscopic vs Robot-Assisted Abdominal Surgery. JAMA Surg. 2025:e253581. doi: 10.1001/jamasurg.2025.3581.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)