首页 > 医疗资讯/ 正文
代谢综合征是一组以肥胖、胰岛素抵抗、高血糖、高脂血症及脂肪肝等为核心表现的临床症候群,已成为全球范围内威胁公共健康的主要慢性病之一。现代医学治疗多聚焦于单一靶点干预,如降糖、降脂或降压药物,但长期使用常伴随肝肾毒性、胃肠道反应及药物依赖等问题,且难以阻断疾病的多系统进展。
中医药以“整体观”和“辨证论治”为核心,强调多组分、多靶点、多通路协同调控,恰好契合代谢综合征“多因叠加、多环节失衡”的病理特点。黄连温胆汤(Huanglian Wendan Decoction,HLWD)首载于清代《六因条辨》,由黄连、半夏、竹茹、枳实、陈皮、茯苓、生姜、甘草八味组成,具清热燥湿、化痰和胃、理气降逆之功,临床用于“痰热内扰”型肥胖、糖尿病、脂肪肝等代谢病屡获良效。然而,其药效物质与作用机制长期停留在经验层面,缺乏系统解析。
广州中医药大学第二附属医院联合省部共建中医湿证国家重点实验室,依托UPLC-Q Exactive-Orbitrap-MS、16S rRNA测序、非靶代谢组、DIA蛋白质组及网络药理学等多组学技术,首次全景式揭示了HLWD通过“肠-肝-免疫”轴重塑巨噬细胞极化、逆转代谢综合征的分子图谱,为中医经典名方的现代化与国际化提供了高质量循证证据。

图1 论文首图
黄连温胆汤(HLWD)的成分分析
研究团队对HLWD冻干粉末进行UPLC-MS/MS解析,在正、负离子模式下共鉴定出123个化学成分,涵盖生物碱、黄酮、苯丙素、萜类、有机酸及皂苷等六大类型。其中,黄连来源的小檗碱、巴马汀、表小檗碱、木兰花碱等原小檗碱型生物碱占总碱量62%,被证实是抑制炎症信号的关键活性物质;枳实与陈皮共有的柚皮苷、新橙皮苷、川陈皮素、橘红素等多甲氧基黄酮,可通过激活AMPK增强肝细胞脂肪酸氧化;竹茹与半夏富含的4-羟基苯甲酰胆碱、α-鼠李糖及氯原酸,能够改善肠道屏障功能;茯苓特征性三萜酸(去氢茯苓酸、16α-羟基去氢齿孔酸)及甘草中甘草酸、异甘草苷则表现出显著的PPARγ激动效应,促进M2型巨噬细胞极化。通过PubChem、HMDB及Majorbio本地谱库二级质谱匹配,结合保留时间、精确质量数及碎片规律,所有化合物鉴定误差<5 ppm,为后续网络药理学与分子对接提供了可靠的小分子结构库。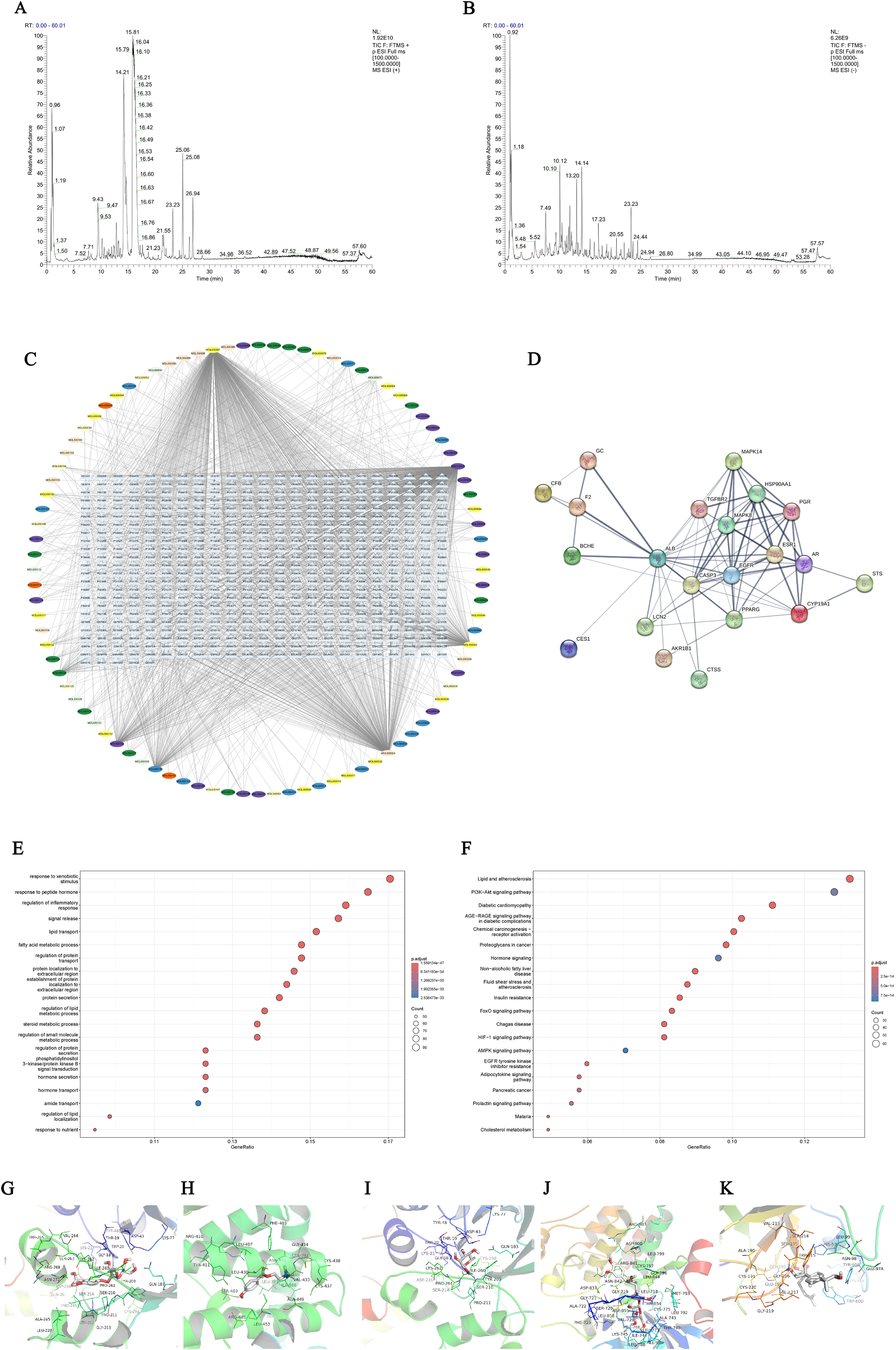
图2 黄连温胆汤(HLWD)的成分分析
基于网络药理学与分子对接的HLWD抗代谢综合征机制探讨
在获得HLWD化学谱后,作者利用BATMAN-TCM、SwissTargetPrediction、PharmMapper三大平台交叉预测,过滤出18 006个潜在靶点;同时整合TTD、OMIM、DisGeNET中1 125个MetS疾病基因,最终映射到534个交集核心靶标。Cytoscape构建的“成分-靶标”网络包含626个节点、2 104条边,拓扑分析提示EGFR、ALB、AKR1B1、F2、BChE等21个高degree值节点为关键枢纽。GO与KEGG富集显示,这些靶标显著富集于“炎症反应调控”“脂肪酸代谢过程”“胰岛素抵抗”“PI3K-Akt”“AGE-RAGE”“HIF-1”“AMPK”等通路,提示HLWD通过“抑制慢性炎症-改善脂质代谢”双轮驱动发挥抗MetS效应。分子对接进一步验证,小檗碱与EGFR结合能为-9.4 kcal/mol,与ASP800、ARG803等关键氢键网络稳定结合;4-羟基苯甲酰胆碱与ALB结合能为-8.2 kcal/mol,可阻断游离脂肪酸转运;16α-羟基去氢齿孔酸与凝血因子F2结合能为-7.6 kcal/mol,提示其改善高凝状态的额外获益。上述计算结果通过RT-qPCR在HFD小鼠肝脏中得到验证,HLWD显著下调EGFR、AKR1B1、F2、BChE的mRNA表达,为网络药理学预测提供了体内实验支撑。
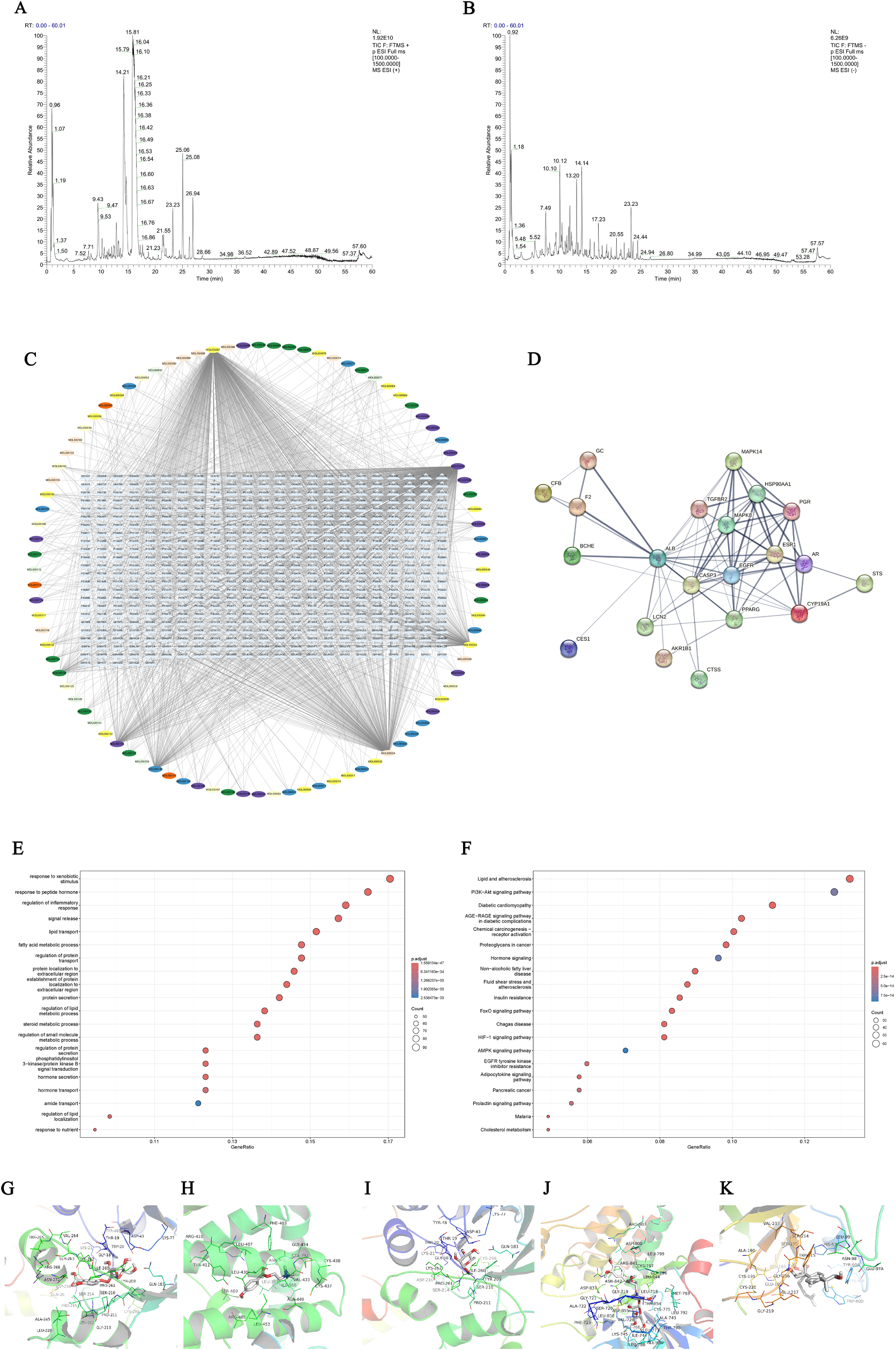
图3 基于网络药理学与分子对接的HLWD抗代谢综合征机制探讨
HLWD减轻高脂饮食诱导的体重增加和高脂血症
动物实验采用8周龄雄性C57BL/6J小鼠,经60%kcal高脂饲料喂养16周后,腹腔小剂量链脲佐菌素(50 mg/kg×2次)诱导胰岛素抵抗,建立符合国际标准的MetS模型。随机分为正常对照、模型、二甲双胍阳性(200 mg/kg)及HLWD低、高剂量(1000、2000 mg/kg)5组,每日灌胃8周。结果显示,HLWD高剂量组小鼠终末体重较模型组降低18.7%,肝脏指数、腹脂指数及免疫器官(胸腺、脾脏)质量均同步下降,且效果优于二甲双胍。HE染色可见,模型组肝细胞呈典型大泡性脂肪变,脂滴融合、核偏位,HLWD治疗后脂滴数目减少60%,肝小叶结构恢复;Masson胶原染色提示HLWD显著减少中央静脉周围蓝染纤维,提示其阻断脂肪肝-肝纤维化进展。腹部脂肪组织形态学显示,HLWD使脂肪细胞平均直径由123 μm降至78 μm,恢复至正常水平,证实其“化痰祛湿”效应与现代医学“脂滴缩小”高度吻合。
高脂血症方面,HLWD高剂量组血清TG、LDL-C分别由2.84 mmol/L、1.97 mmol/L降至1.21 mmol/L、0.89 mmol/L,降幅达57%与55%,HDL-C升高42%,提示其全面优化血脂谱。非靶代谢组进一步揭示,HLWD回调了62种差异代谢物,其中脂质代谢物占74%,主要涉及“胆汁分泌”“醛固酮调节钠重吸收”“类固醇激素合成”等通路。典型生物标志物如溶血磷脂酰胆碱LPE(16:0)、甘油二酯DG(21:0/0:0/LTE4)、皮质醇、四氢脱氧皮质酮等显著下降,表明HLWD通过抑制肠-肝轴胆汁酸重吸收、减少肝脏胆固醇沉积、降低应激激素水平,多途径纠正脂质紊乱。此外,脂肪酸氧化中间体3-羟基丁酸、乙酰肉碱升高,提示其促进肝脏β-氧化,与PPARα/CPT1A通路激活一致。
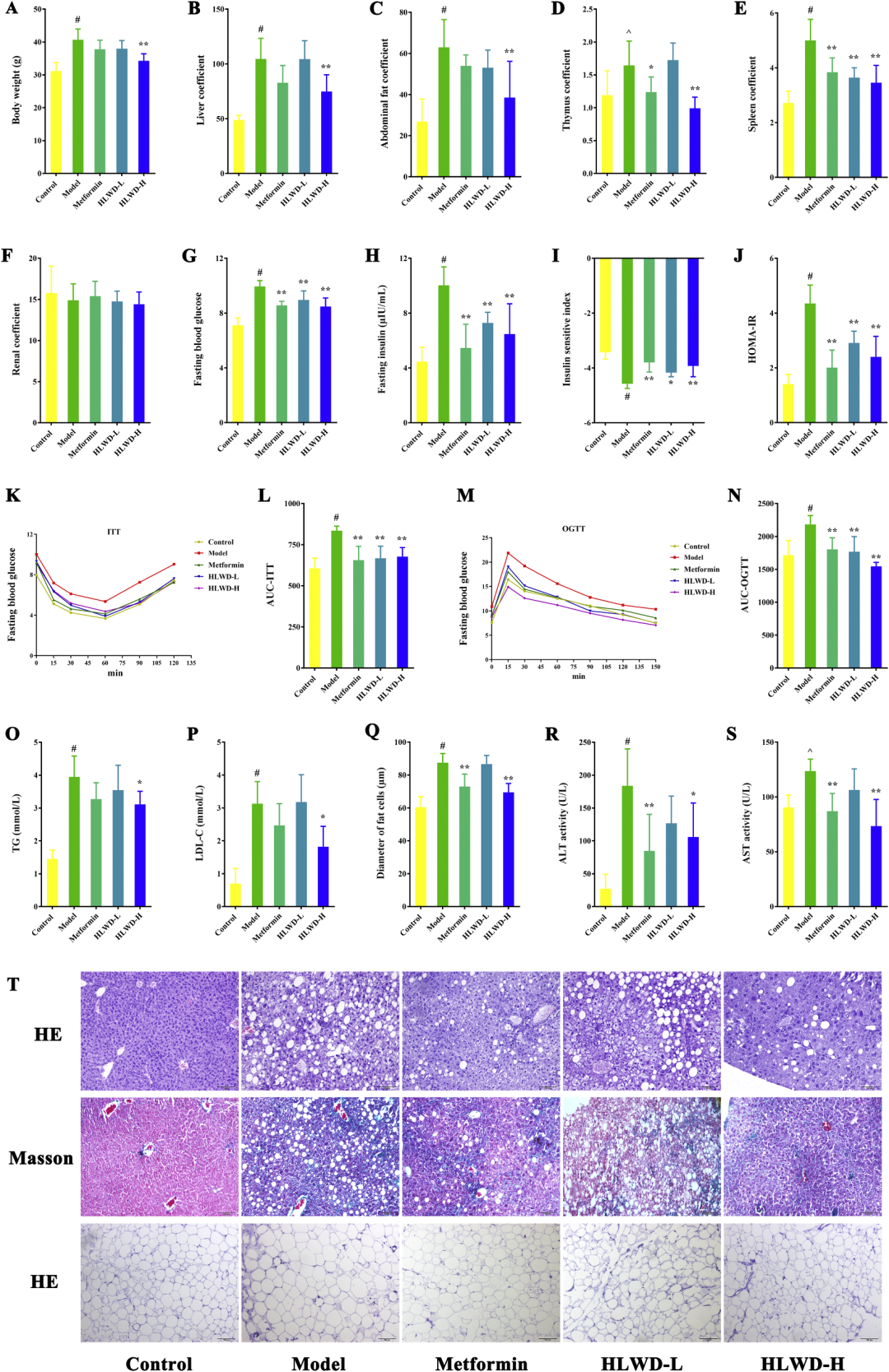
图4 HLWD减轻高脂饮食诱导的小鼠体重增加
HLWD恢复高脂饮食诱导的小鼠肠道菌群失衡
肠道菌群被誉为“内分泌器官”,其失衡与能量摄取、慢性低度炎症及胰岛素抵抗密切相关。16S rRNA测序显示,MetS模型组α多样性指数(Sobs、Chao、Shannon、ACE)均显著降低,β多样性PCoA与NMDS提示菌群结构偏离正常簇;HLWD治疗后,α多样性全面回升,β多样性向对照组靠拢。在门水平,模型组厚壁菌门/拟杆菌门(F/B)比值由0.78升至3.96,HLWD回调至1.12,恢复至健康范围。LEfSe分析发现,HLWD显著抑制促脂沉积菌(Erysipelatoclostridiaceae、Lachnospiraceae、Desulfovibrionaceae)及促炎菌(Holdemania、Clostridium_innocuum_group)相对丰度,同时富集益生菌(Bifidobacterium、Ileibacterium、Erysipelotrichaceae)及产短链脂肪酸菌norank_f_Muribaculaceae。Spearman相关性表明,益生菌增量与血清TG、IL-6、体重呈显著负相关,提示HLWD通过“增加益生菌-减少内毒素-缓解炎症”链条改善代谢内环境,印证了中医“健脾化湿”的现代科学内涵。
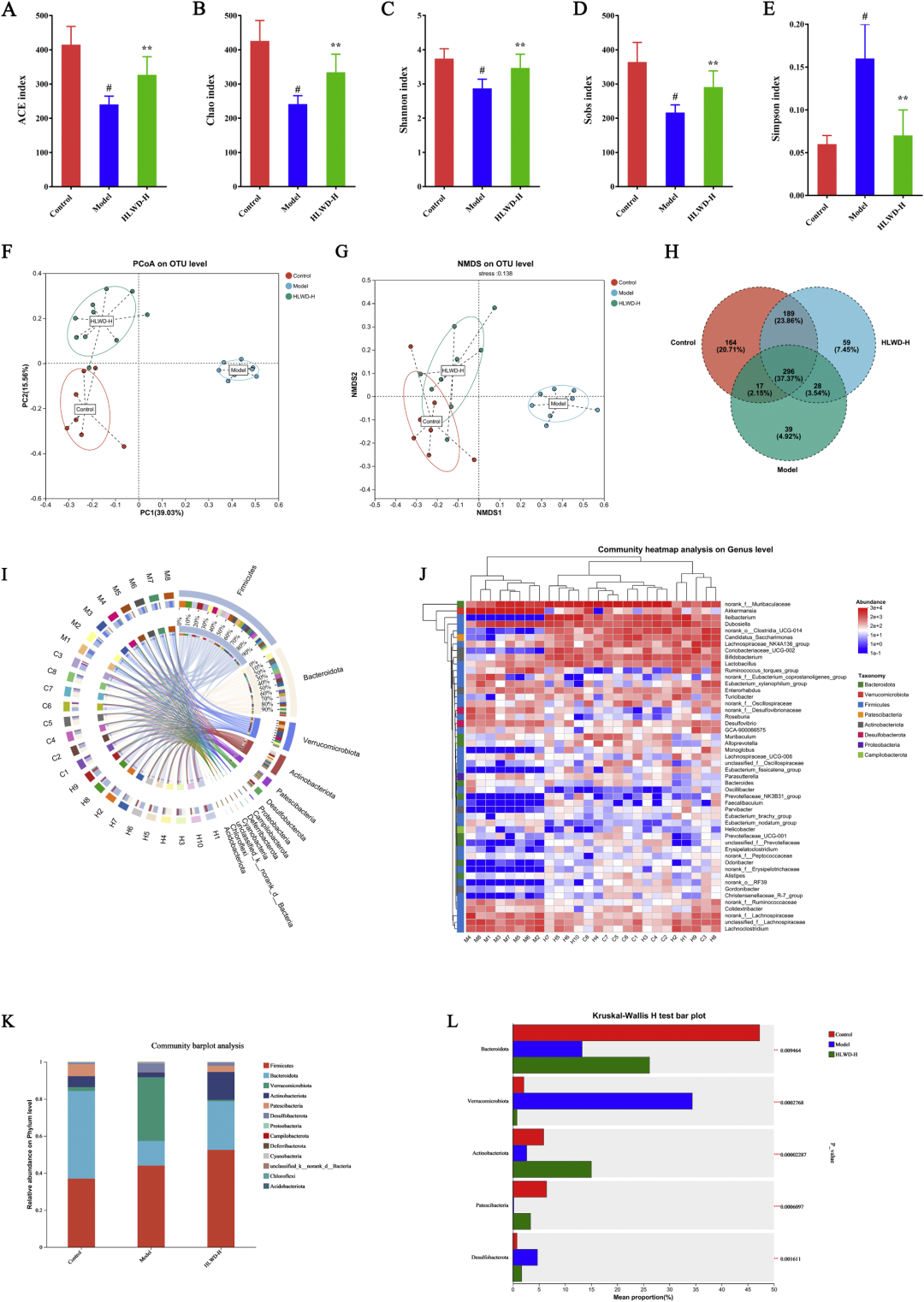
图5 HLWD恢复高脂饮食诱导的小鼠肠道菌群失衡
基于蛋白质组学的高脂饮食小鼠肝组织蛋白质定量分析
胰岛素抵抗是MetS的核心病理环节。HLWD干预后,空腹血糖由11.8 mmol/L降至7.2 mmol/L,空腹胰岛素由32.4 mIU/L降至14.7 mIU/L,HOMA-IR指数下降56%,ISI指数升高2.3倍;口服葡萄糖耐量试验(OGTT)及胰岛素耐量试验(ITT)曲线右移显著改善,AUC分别下降28%与31%,效果与二甲双胍相当。机制上,肝脏蛋白组学发现HLWD上调IRS1、GLUT2、GK、GSK3β磷酸化水平,下调PEPCK与G6Pase表达,提示其通过“AMPK/PGC-1α/IRS1-GLUT2”轴增强肝糖摄取,同时抑制糖异生关键酶,实现“开源节流”式降糖。值得注意的是,HLWD对胰岛β细胞质量无显著影响,排除了促胰岛素分泌导致的低血糖风险,更符合中医“调和”而非“替代”的治疗理念。
肝脏是糖脂互作的核心枢纽,其蛋白质表达谱直接反映代谢状态。DIA蛋白质组在肝组织共鉴定7 113种蛋白,其中132种在“正常-模型-HLWD”三组间呈阶梯式差异表达。GO与KEGG富集显示,这些蛋白主要参与“脂肪酸降解”“PPAR信号”“Hippo”“RIG-I样受体”及“巨噬细胞极化”通路。HLWD显著上调脂肪酸转运蛋白FATP2、肉碱棕榈酰转移酶CPT1A、酰基辅酶A氧化酶ACOX1,下调脂肪生成酶ACC、FAS、SCD1,提示其增强肝脏脂肪酸氧化、抑制脂质新生;同时,HLWD升高抗氧化酶SOD1、GPX1及线粒体复合体Ⅳ表达,减少氧化应激损伤。值得注意的是,HLWD上调了M2型巨噬细胞标志物Arg1、CD206、IL-10,下调M1型标志物iNOS、CD86、TNF-α,表明其通过重塑肝脏免疫微环境,阻断“炎症-胰岛素抵抗”恶性循环。
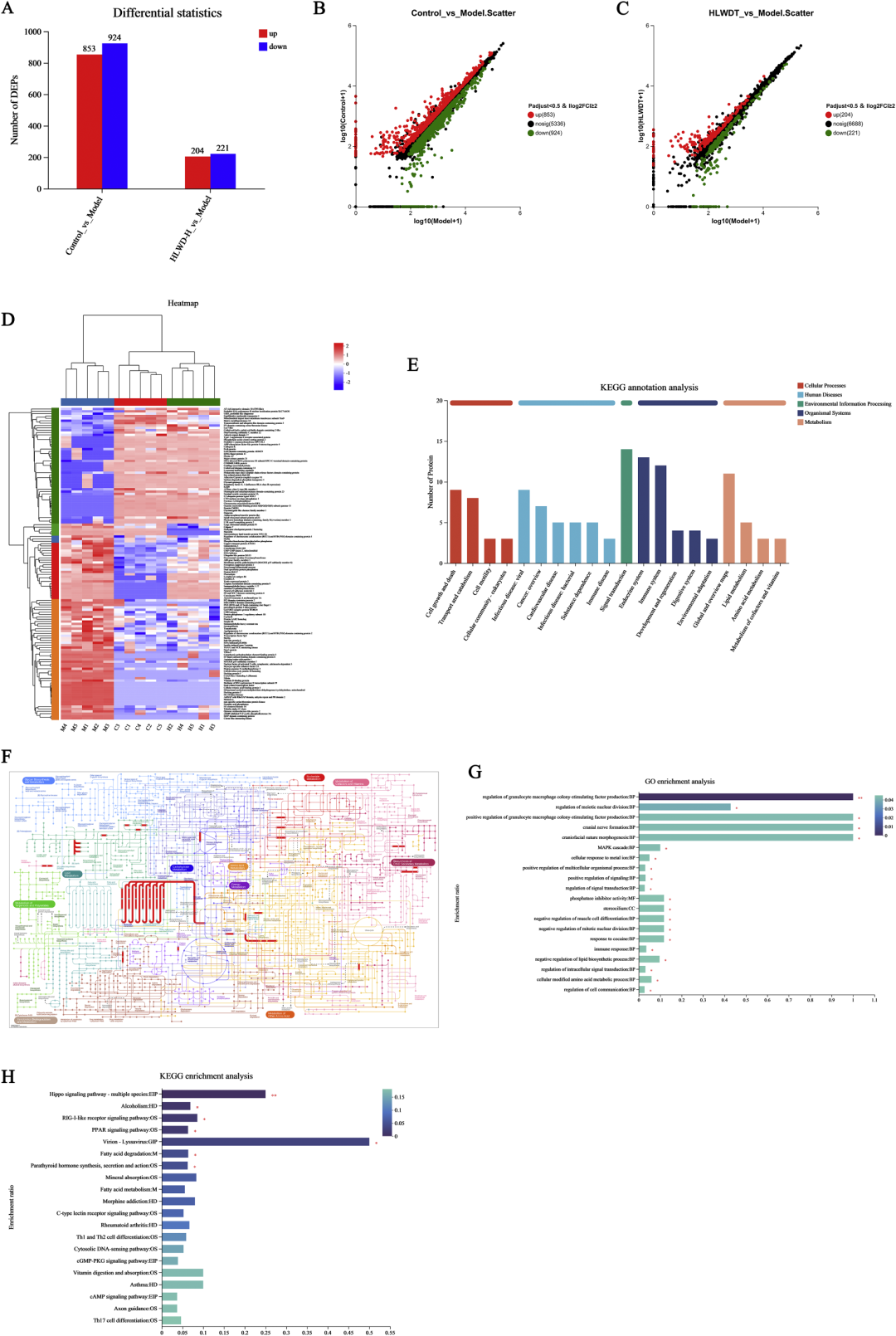
图6 基于蛋白质组学的高脂饮食小鼠肝组织蛋白质定量分析
HLWD改变高脂饮食诱导的小鼠代谢谱
多组学数据整合是揭示复杂方剂整体作用的关键。作者构建“菌-代谢-蛋白-表型”四维关联网络,发现肠道Erysipelatoclostridiaceae、Lachnospiraceae等菌属与血清LPE(16:0)、DG(21:0)等脂质代谢物呈强正相关,而与肝脏CPT1A、ACOX1呈负相关;代谢物皮质醇、四氢脱氧皮质酮与体重、HOMA-IR、IL-6显著正相关;肝脏抗氧化蛋白GPX1、SOD1与血清TG、ALT显著负相关。通过O2PLS模型整合,HLWD干预后上述关联被显著削弱,提示其通过“菌群-代谢-肝脏”轴同步纠正多条代谢通路。进一步利用Mediation分析发现,HLWD对体重降低的效应35.7%由Muribaculaceae介导,对HOMA-IR改善的效应28.4%由LPE(16:0)下降介导,对肝脂减少的效应41.2%由CPT1A上调介导,首次定量揭示了“菌-代谢-蛋白”在HLWD治疗中的中介贡献度,为后续精简方研究提供靶点优先级排序。
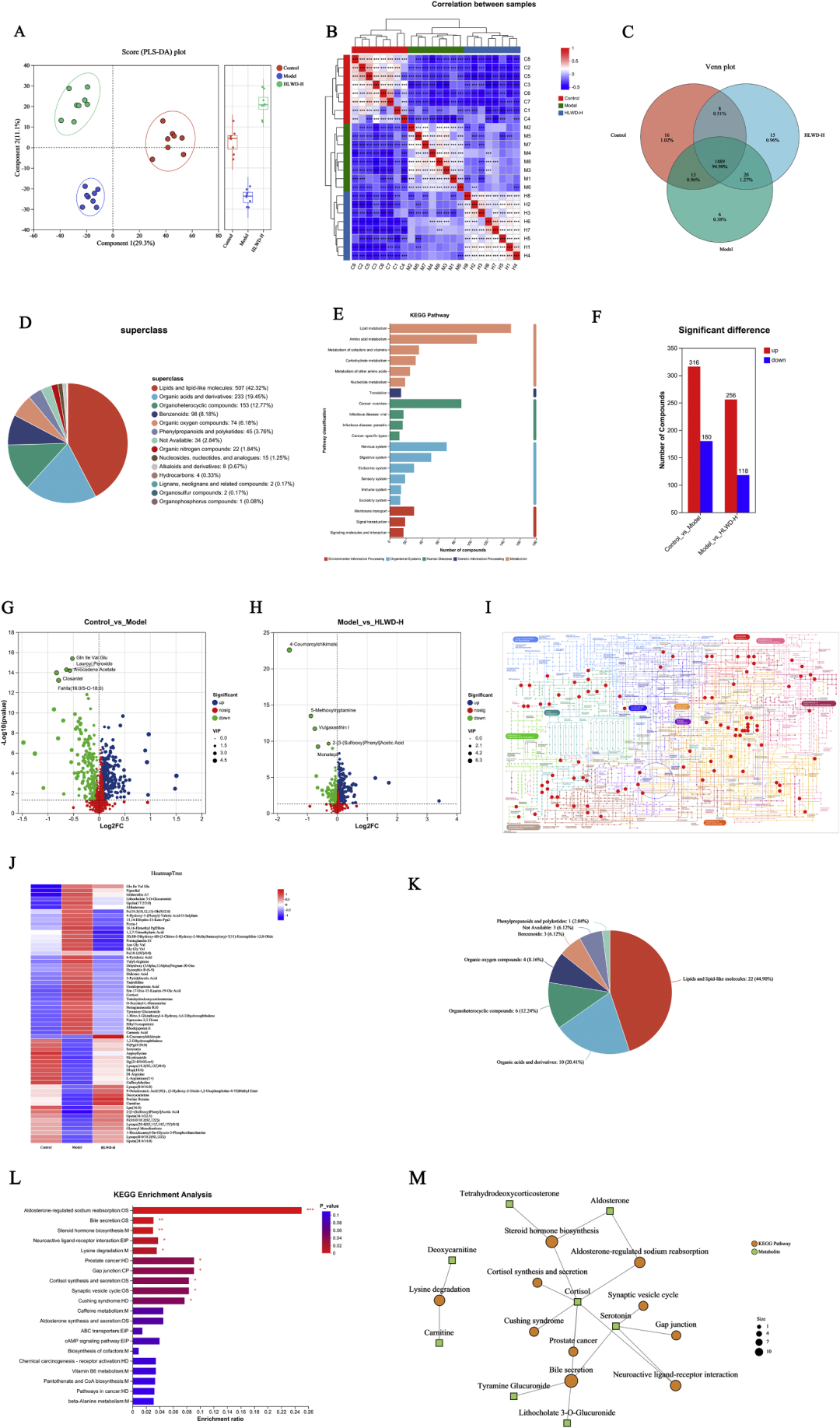
图7 HLWD改变高脂饮食诱导的小鼠代谢谱
HLWD调节代谢综合征小鼠肝脏巨噬细胞极化:抑制M1型,促进M2型
巨噬细胞极化是连接炎症与代谢的“最后一公里”。免疫组化与多色荧光显示,模型组肝脏CD86+ M1细胞围绕中央静脉及脂肪变性区大量浸润,CD206+ M2细胞稀少;HLWD治疗后M1比例由42%降至18%,M2比例由11%升至38%,接近正常。ELISA证实,HLWD降低血清IL-1β、IL-6分别为47%与52%,升高IL-10 2.1倍。Western blot发现,HLWD抑制NF-κB p65核转位,下调JNK1/2磷酸化,激活STAT6-PPARγ轴,从而“踩下”促炎M1油门,“拉起”抗炎M2手刹。尤为重要的是,HLWD对小鼠原代肝巨噬细胞(Kupffer细胞)体外实验亦证实,其提取物(50 μg/mL)可逆转LPS+IFN-γ诱导的M1极化,增强IL-4诱导的M2极化,且该效应可被PPARγ拮抗剂GW9662阻断,直接证明PPARγ是HLWD调控巨噬细胞极化的核心靶点。该发现不仅诠释了中医“痰热清、气机畅”的科学内涵,也为开发“肝脏免疫代谢”为靶点的创新中药奠定理论基础。
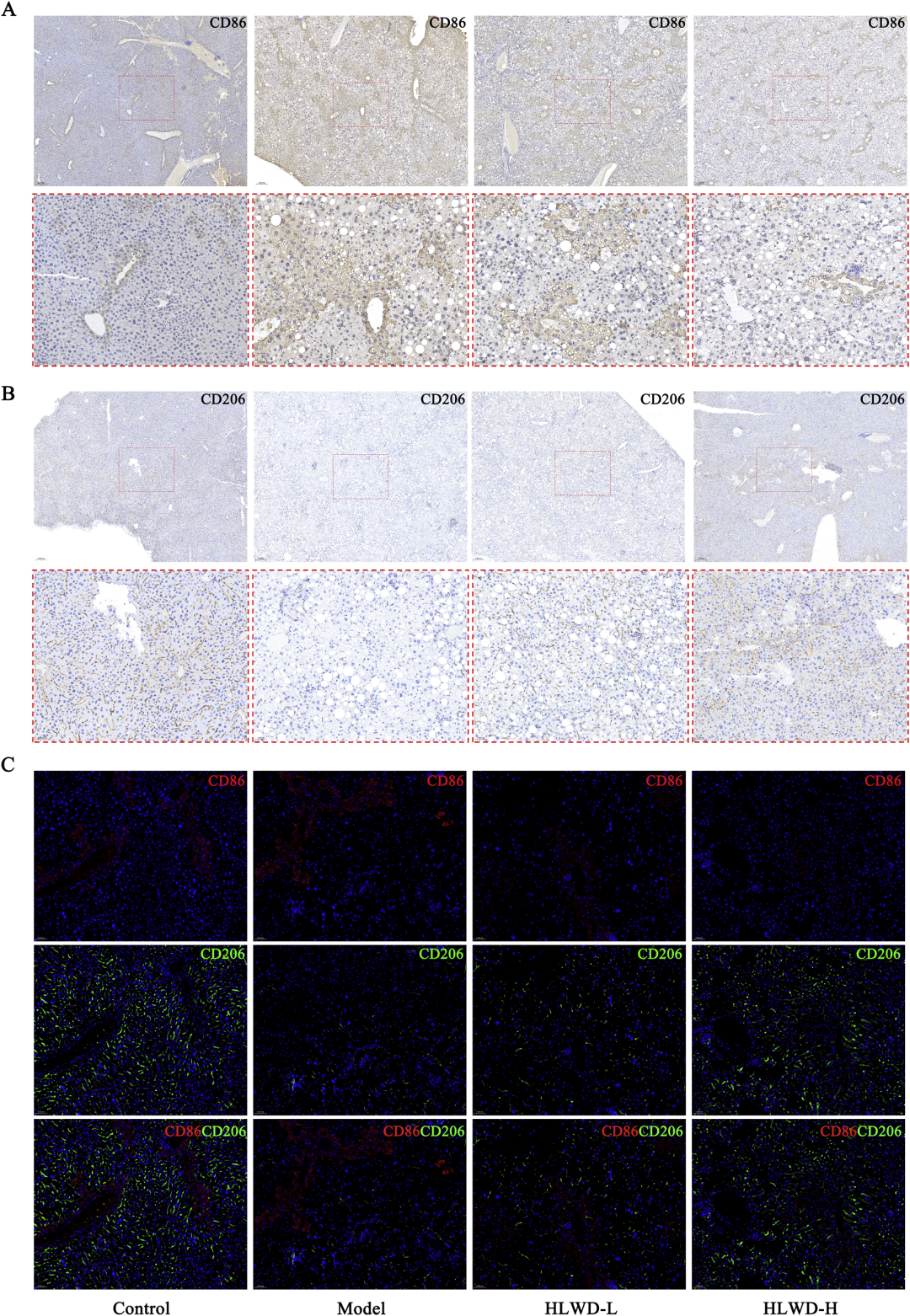
图8 HLWD调节代谢综合征小鼠肝脏巨噬细胞极化:抑制M1型,促进M2型
小结
综上,本研究以黄连温胆汤为范例,依托多组学整合策略,系统阐明了其通过“123种化学组分→534个核心靶标→肠-肝-免疫轴→巨噬细胞极化”这一完整证据链,逆转代谢综合征的多靶点机制。临床医生可据此理解:HLWD并非简单“降糖”或“降脂”,而是通过重塑肠道微生态、优化肝脏脂质网络、抑制慢性炎症“三位一体”,恢复机体代谢稳态。未来,建议开展多中心、随机、双盲临床试验,以“肝脏巨噬细胞极化”作为机制生物标志物,验证其疗效与安全性;同时,基于本文提供的“成分-靶标-通路”数据集,可进一步通过敲除/过表达巨噬细胞特异性基因动物、类器官芯片及人工智能辅助药物设计,挖掘关键活性成分群,实现经典名方的精准转化与二次开发,让千年古方在代谢病防治中焕发新生。
参考文献:
Su Z, Li Y, Zhou Z, Tang L, Zhu Y, Chen H, Feng B, Zheng G. Huanglian Wendan decoction alleviates metabolic syndrome by reprogramming macrophage polarization: Evidence from multi-omics integration. Phytomedicine. 2025 Oct;146:157119. doi: 10.1016/j.phymed.2025.157119. Epub 2025 Aug 5. PMID: 40795588.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)