首页 > 医疗资讯/ 正文
斑马鱼作为一种小型脊椎动物,在生物医学研究领域日益受到重视,特别是在罕见遗传性神经肌肉疾病的研究中展现出独特价值,其体型小巧、繁殖迅速、胚胎透明以及外部受精等特点,为科学家观察发育过程、进行遗传操作和高通量筛选提供了便利。此外斑马鱼与人类在基因和生理功能上具有高度保守性,超过百分之七十的人类蛋白在斑马鱼中存在同源物,尤其是与疾病相关的蛋白同源比例高达八成以上,这使得斑马鱼成为研究复杂人类疾病的理想模型。在罕见神经肌肉疾病领域,由于患者数量稀少、疾病异质性强以及研究资源有限,传统哺乳动物模型的应用受到限制,而斑马鱼凭借其独特优势,填补了从基础研究到临床前应用之间的空白,为疾病机制解析和治疗策略开发提供了强有力的工具。

在斑马鱼模型中,研究罕见神经肌肉疾病的方法主要包括自然突变体的筛选与基因工程改造两大类,自然突变体通常通过化学诱变剂如乙基亚硝基脲诱导产生,随后通过表型筛选鉴定出与人类疾病相关的突变品系。例如在杜氏肌营养不良症研究中发现的sapje等品系,它们携带不同外显子的无义突变,导致dystrophin蛋白功能丧失,此外基因编辑技术的广泛应用极大拓展了斑马鱼模型的构建能力,CRISPR/Cas9系统能够精准敲除或引入特定基因突变,模拟人类疾病的遗传背景。例如在肢带型肌营养不良症研究中,研究人员利用CRISPR/Cas9成功构建了capn3b基因敲除模型,用于模拟LGMDR1亚型的病理特征。另一种常用技术是 Morpholino反义寡核苷酸 knockdown,通过抑制特定基因的翻译或剪接,快速评估基因功能缺失对肌肉发育的影响,这种方法在多种LGMD亚型如LGMDR2和LGMDR9的研究中被广泛采用。此外转基因技术如Tol2转座子系统也被用于在斑马鱼中过表达人类突变基因,例如在LGMDD1研究中注射突变型DNAJB6 RNA以模拟患者肌肉缺陷,这些方法不仅能够重现人类疾病的关键表型,还便于在整体动物水平进行实时观察和高内涵分析。
通过上述方法构建的斑马鱼模型在研究杜氏肌营养不良症方面取得了显著成果,多个dystrophin缺失品系如sapje、sapje-like等被证实表现出进行性肌肉功能障碍和纤维结构异常,与人类DMD患者病理特征高度一致,利用这些模型,研究人员开展了大规模药物筛选,发现多种小分子化合物能够部分纠正肌肉表型,例如通过双折射成像技术评估肌肉完整性,筛选出组蛋白去乙酰化酶抑制剂等表观遗传调节剂。此外在药物重定位研究中,已获批用于其他疾病的化合物如线粒体通透性转换孔抑制剂也在斑马鱼DMD模型中显示出改善肌肉功能的潜力。近年来基于CRISPR/Cas9的遗传筛选平台还被用于鉴定DMD疾病修饰基因,研究人员在斑马鱼中敲低已知修饰基因如LTBP4和THBS1的同源物,并发现gahit16、man1a1等新型修饰因子能够影响疾病严重程度,这些发现为开发联合治疗策略提供了新靶点。
在肢带型肌营养不良症研究领域,斑马鱼模型为理解多种亚型的病理机制贡献了重要数据。根据遗传方式和致病基因不同,LGMD被分为常染色体显性和隐性两大类,涉及CAPN3、DYSF、SGCA等多个基因,通过Morpholino knockdown技术构建的hnrpdl模型表现出体型异常、运动受限等肌病表型,证实了HNRPDL与LGMDD3的关联。在钙蛋白酶病研究中,CRISPR/Cas9生成的capn3b突变体在应激条件下出现明显肌肉损伤,为评估整体干预措施提供了可靠模型。对于dysferlinopathy,斑马鱼模型揭示了dysferlin蛋白在肌膜修复和结构稳定中的关键作用,其缺失导致进行性肌无力特征性步态异常。在肌聚糖病研究中,针对β-和δ-肌聚糖的 knockdown和 knockout模型均表现出进行性肌营养不良表型,与人类患者病理进展相似,此外在FKRP相关肌营养不良研究中,多种基因编辑模型被用于探索疾病机制,发现FKRP参与高尔基体中纤连蛋白的唾液酸化过程。这一过程对维持基底膜完整性至关重要,其他LGMD亚型如LGMDR25和LGMDR26也通过popdc1和popdc3 knockdown模型得到深入解析,这些模型显示出肌原纤维排列紊乱、肌膜连接异常等特征,为理解疾病发病机制提供了新视角。
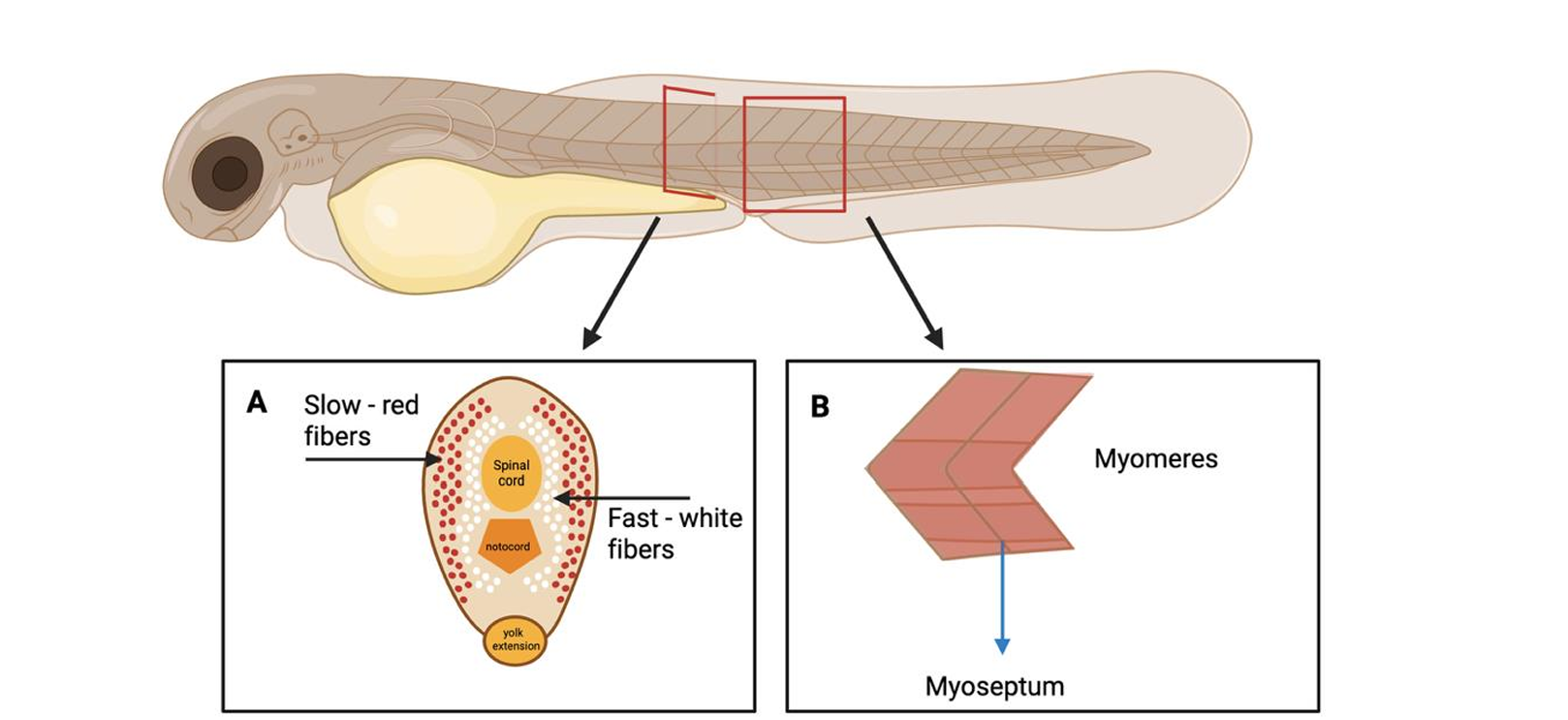
图:斑马鱼肌肉组织示意图
布罗迪肌病作为一种超罕见疾病,在斑马鱼模型中取得了独特研究进展。由于小鼠SERCA1敲除模型因呼吸衰竭早期致死,斑马鱼accordion突变体成为研究该病的主要动物模型,这些acc品系携带ATP2A1基因的不同点突变,导致SERCA1蛋白功能受损。其中acc^tq206突变体表型最为严重,其S766F突变位于M5结构域的柔性铰链区,该区域在钙离子结合与解离过程中发生构象变化,突变后蛋白构象自由度受限,严重影响钙离子转运功能。在药物测试方面,accordion幼虫被用于评估CFTR校正剂的治疗潜力,初步结果显示该化合物在改善肌肉松弛功能的同时未引起明显毒性反应,为布罗迪患者的药物治疗提供了新方向。
斑马鱼模型在罕见神经肌肉疾病研究中展现出显著优势,其胚胎透明特性便于直接观察肌肉发育和病理变化,而快速繁殖能力和小体型则支持大规模药物筛选和表型分析。与哺乳动物模型相比,斑马鱼维护成本低、伦理限制较少,且基因操作技术成熟,能够快速构建多种疾病模型。在DMD、LGMDs和BM等疾病研究中,斑马鱼不仅帮助阐明了致病机制,还加速了治疗策略的开发,尤其是在高通量化合物筛选中表现出高效性和预测性。随着基因编辑技术和成像方法的不断进步,斑马鱼模型将在未来罕见病研究中发挥更重要作用,为理解疾病复杂性、开发靶向疗法带来新希望,同时也有助于减少哺乳动物使用,符合动物福利的伦理要求。
原始出处:
Akyürek, E.E.; Erba, M.; Dalla Barba, F.; Sandonà, D.; Sacchetto, R. Zebrafish as a Model Organism for Research in Rare Genetic Neuromuscular Diseases. Int. J. Mol. Sci. 2025, 26, 8832.
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。
猜你喜欢
- Int J Ment Health Addiction:学业动机、学业压力和手机成瘾之间的关联:智慧的中介作用
- 肌张力减低怎么治疗呢,肌张力减低是什么呢
- 如何看懂体液免疫检测十大指标?
- 卫仕犬猫营养品备受消费者青睐 荣膺派读奖2024年度“用户喜爱的品牌”双项大奖
- 日本一大学丢失大量氰化物,可致160-250人死亡
- 春季容易皮肤过敏?做好5项措施可预防
- 冬季,流感疫苗应当如何接种
- 睡觉前护肤的方法都有哪些?
- 痛心!近期报道两起患者院内死亡!要么判为一级甲等医疗事故;要么索赔200万,连告两家医院!为何医生越来越难当了?带来哪些教训?
- Eur Radiol:双层双能CT肺灌注鉴别急性肺栓塞与慢性血栓栓塞性肺动脉高压
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)