首页 > 医疗资讯/ 正文
胃癌作为全球范围内常见的恶性肿瘤之一,其发病率和死亡率居高不下,尤其在中晚期患者中预后较差,因此开发有效的预后预测工具对于临床治疗决策具有重要意义。肿瘤微环境由肿瘤相关基质和肿瘤浸润淋巴细胞等组成,近年来被证实与肿瘤的进展、转移及治疗反应密切相关,然而其在临床常规应用中的推广仍面临诸多挑战,包括评估标准不统一、人工判读主观性强以及缺乏自动化量化手段等。尽管深度学习方法在数字病理图像分析中展现出潜力,但由于高质量标注数据获取困难、模型可解释性不足以及临床工作流整合复杂等问题,其实际应用效果受限。本研究旨在通过构建一种基于深度学习的肿瘤微环境定量表征框架,开发新型生物标志物,以提升胃癌预后预测的准确性和可重复性。

本研究采用回顾性设计,共纳入来自三星医疗中心的320例晚期胃癌患者作为内部验证队列,以及来自首尔国立大学医院的186例患者作为外部验证队列。所有患者均接受手术切除并在术后因复发或转移接受姑息化疗,排除了术前接受放化疗的病例。研究选取每位患者最具代表性的石蜡组织块进行苏木精-伊红染色、免疫组织化学染色及下一代测序分析。全玻片图像在20倍放大下扫描,并由经验丰富的病理学家选定肿瘤区域进行分析,排除正常黏膜、溃疡及坏死区域。为减少标注需求,本研究创新性地利用免疫组织化学染色图像作为生物学参考,通过虚拟染色技术将H&E图像转化为对应的细胞角蛋白、白细胞共同抗原和结蛋白免疫组织化学图像,并训练卷积神经网络识别正常上皮区域。
在深度学习框架构建方面,研究采用了注意力门控生成对抗网络进行虚拟染色,并利用EfficientNet-B3模型进行正常上皮分类。生成器网络采用对称编码器-解码器结构,通过注意力门控机制突出空间特征,提升染色定位准确性;判别器则负责区分真实与虚拟免疫组织化学图像。损失函数结合平滑L1损失、结构相似性损失和二元交叉熵损失,并特别引入了DAB通道特异性损失以增强染色特征学习。模型训练过程中应用了随机旋转、缩放、翻转和高斯模糊等图像增强技术,并针对不同染色模式优化损失权重。图像配准通过全局与局部两步法实现,确保H&E与免疫组织化学图像在像素级对齐。基于虚拟染色输出的组织区域,研究进一步计算了肿瘤-基质比和肿瘤浸润淋巴细胞比例,其中肿瘤-基质比定义为基质面积占肿瘤与基质面积之和的比例,肿瘤浸润淋巴细胞比例则为淋巴细胞面积占肿瘤与基质面积之和的比例。
通过自助抽样法生成100个样本,研究确定了肿瘤-基质比和肿瘤浸润淋巴细胞的最佳截断值分别为0.76和0.03,据此将患者分为低风险与高风险亚型。进一步整合这两种亚型,利用单变量Cox回归系数构建TMEpATH评分系统,将患者划分为低、中、高风险三组。模型性能通过一致性指数、时间依赖性曲线下面积和综合曲线下面积等指标进行评估,并在内外部队列中验证其预后判别能力。统计学分析包括Kaplan-Meier生存分析、log-rank检验、Cox比例风险模型以及逻辑回归,所有分析均使用R软件完成,显著性水平设定为P值小于0.05。
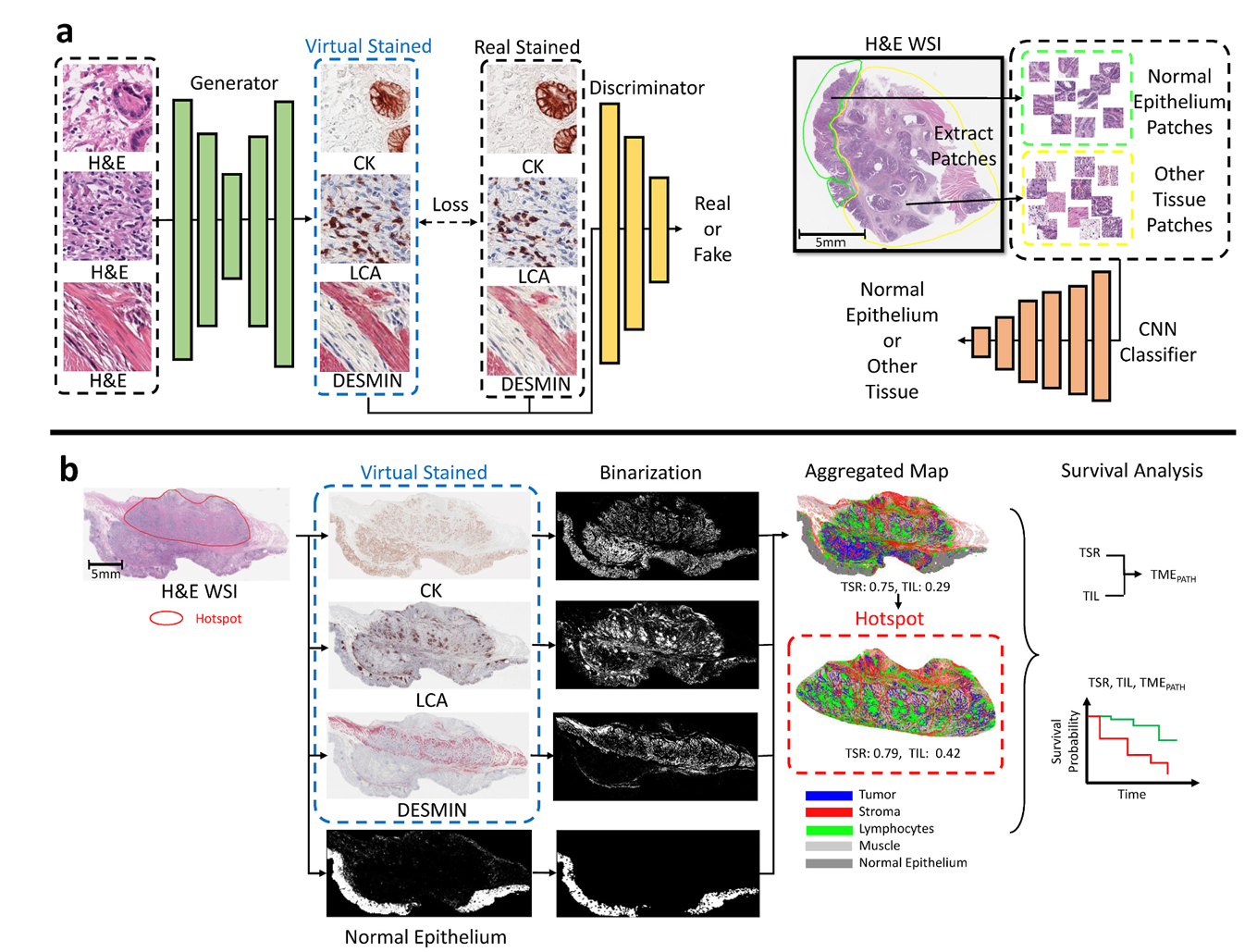
图1 所提出的基于深度学习框架的概述
在深度学习模型性能方面,虚拟染色模型在峰值信噪比、结构相似性指数和Dice系数等指标上均表现优异,其中DAB通道损失的引入显著提升了各染色模式的生成质量。细胞角蛋白、白细胞共同抗原和结蛋白的最佳β值分别为50、30和10,复合得分最高。正常上皮分类模型的受试者工作特征曲线下面积达到0.97,显示出极高的分类准确性。视觉对比显示虚拟染色图像在整体和局部水平均与真实免疫组织化学图像高度一致,验证了模型在生物特征再现方面的可靠性。患者特征分析表明,在三星医疗中心队列中,肿瘤-基质比与性别、年龄、TNM分期和Lauren分类显著相关,而肿瘤浸润淋巴细胞则与Lauren分类及化疗反应相关;在首尔国立大学医院队列中,肿瘤-基质比与Lauren分类独立相关,而肿瘤浸润淋巴细胞未显示显著关联。
预后分析结果显示,肿瘤-基质比亚型在三星医疗中心队列中与总生存期显著相关,高风险组死亡风险比为1.430,一致性指数为0.531;在外部验证队列中虽未达统计学显著性,但趋势一致。肿瘤浸润淋巴细胞亚型在外部队列中表现更佳,高风险组死亡风险比为1.691,一致性指数为0.564。整合性生物标志物TMEpATH在内外部队列中均显著分层患者预后,三星医疗中心队列中中风险与高风险组相对于低风险组的死亡风险比分别为1.281和1.768,一致性指数为0.545;首尔国立大学医院队列中相应风险比分别为1.389和2.435,一致性指数为0.579。此外,TMEpATH在预测无复发生存方面也表现出一定能力,内外部队列的受试者工作特征曲线下面积分别为0.561和0.587,提示其可能作为化疗反应的辅助预测指标。
基因组学关联分析揭示,肿瘤-基质比与微卫星不稳定性、肿瘤突变负荷及CDH1、ERBB2、BRD3等多个基因突变显著相关;TMEpATH则与微卫星不稳定性、肿瘤突变负荷以及BRCA2、CDH1、ATM等基因突变密切相关。这些发现表明,所开发的生物标志物不仅具有预后价值,还与胃癌的关键分子特征相关联,为进一步理解肿瘤生物学机制提供了线索。
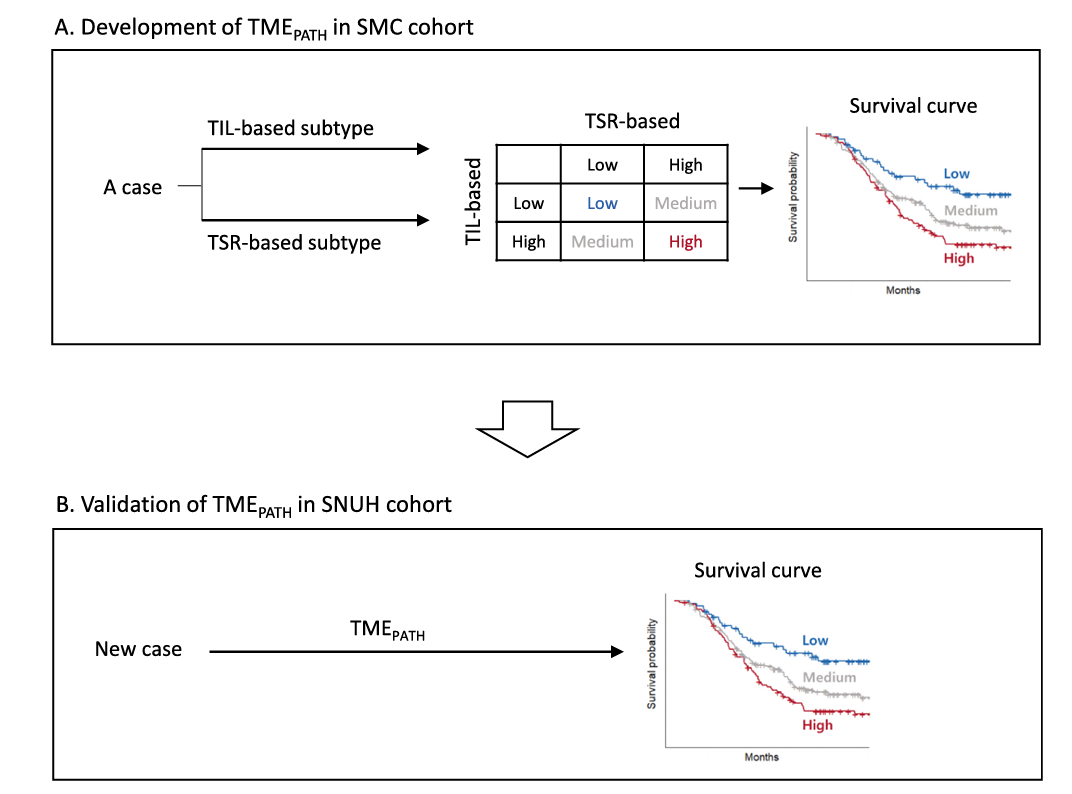
图2 使用示例说明TMEpATH的开发和验证
本研究通过构建一种注释高效的深度学习框架,实现了从常规H&E图像中自动化、定量化表征肿瘤微环境,并开发出具有临床适用性的预后生物标志物。TMEpATH在独立队列中验证了其稳健的预后判别能力,且与重要基因组改变显著相关,为胃癌的个体化治疗决策提供了潜在工具。尽管当前方法在模型管理和热点区域依赖方面存在局限,未来通过 unified 多分支架构和自动化热点检测有望进一步提升效率与精度。研究结果支持肿瘤微环境在胃癌预后中的核心作用,并为数字病理在临床实践中的整合奠定了坚实基础。
原始出处:
Hong Y, Chi SA, Lee HS, Hwang I, Kang SY, Ahn S, Kim K, An JY, Choi MG, Lee JH, Bae JM, Sohn TS, Kim K-M. Tumor microenvironment-based classification for predicting gastric cancer prognosis. Computers in Biology and Medicine. 2025;197:110938. doi:10.1016/j.compbiomed.2025.110938
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)