首页 > 医疗资讯/ 正文
结直肠癌是威胁人类健康的主要恶性肿瘤之一,全球癌症统计数据显示,2022年全球新发癌症 1996 万例,结直肠癌仍是发病率居前三的恶性肿瘤。国家癌症中心基于肿瘤登记及随访监测发布了2022年中国恶性肿瘤疾病负担情况,新发结直肠癌病例数位居第二,达 52 万例(男性 31 万例,女性 21 万例),死亡病例为 24 万例。结直肠癌治疗已迈入精准化、个体化时代,分子标志物检测作为精准治疗的基石,在结直肠癌临床诊疗中发挥着日益重要的作用。
针对分子检测在结直肠癌和小肠腺癌患者中的价值,小编整理了几个问题:1.结直肠癌MMR蛋白与MSI检测结果为什么会不一致?2.结直肠癌肝转移患者,基因检测选择原发灶还是转移灶?3.恩考芬尼联合西妥昔单抗治疗BRAF V600E突变结直肠癌患者疗效如何?4.结直肠癌患者为何还需关注HER2扩增/过表达?5.NCCN指南推荐晚期小肠腺癌患者进行哪些分子检测?
绘真:1.结直肠癌MMR蛋白与MSI检测结果为什么会不一致?
赵振国教授:
MMR蛋白检测采用IHC进行检测,MSI检测可采用PCR-毛细管电泳法或NGS进行。研究显示,在结直肠癌中,基于分子水平的MSI检测结果与蛋白质水平的MMR检测结果高度一致,一般情况下可以达到 92%-99.74%,甚至 100%。但在实际检测中,两者之间仍有可能出现不一致的情况。
MMR蛋白检测受到很多因素影响,比如新辅助治疗、标本前处理、染色过程质控以及病理医师判读等等。而DNA层面MSI检测则要求对肿瘤细胞占比比较高,在检测前必须进行病理质控。再有,检测样本间的异质性也是导致两种检测结果的不一致的可能原因。除了这些原因,最新的《结直肠癌分子病理检测临床实践指南(2025版)》还做出了如下解释,pMMR/MSI-H情况的发生一般归因于以下几种情况:①MLH1、MSH2、MSH6或PMS2基因中的错义突变,这些变异导致蛋白功能丧失但抗原保留,故而不影响其免疫组织化学表达;②MSI-H也可能由其他基因突变导致,如MLH3、MSH3、PMS1突变以及POLE/POLD1基因突变。dMMR/MSS情况的发生可能归因于某些MMR蛋白的缺失被其他蛋白的功能补偿所掩盖,如MSH6的缺失被MSH3的功能补偿;部分患者在新辅助治疗后MSH6表达会出现不同程度的缺失,但MSI检测表现为MSS型。
所以该指南建议,对于MMR与MSI检测结果不一致的情况,在确认结果无误之后,通过免疫组织化学检测显示为dMMR或通过MSI PCR/NGS检测表明为MSI-H的患者,推荐免疫检查点抑制剂相关治疗。




绘真:2.结直肠癌肝转移患者,基因检测选择原发灶还是转移灶?
赵振国教授:
肝脏是结直肠癌血行转移最主要的靶器官,而肝转移又是结直肠癌患者最主要的死亡原因。有 15%-25% 结直肠癌患者在确诊时就合并有肝转移,我们称其为同时性肝转移,另有 15%-25% 的患者在结直肠癌原发灶根治术后发生肝转移,其中绝大多数(80%-90%)的肝转移灶初始无法获得根治性切除,这就需要我们进一步的治疗。
结直肠癌患者原发灶和转移灶中的RAS(KRAS、NRAS)、BRAF的基因突变状态一致性是非常高的,高达 90% 以上(91%-98.8%),MMR/MSI的一致性同样也是非常高的,高达 96.6%。所以CSCO指南明确指出,结直肠癌患者基于样本的可获取性,原发灶及转移灶均可进行检测;当原发灶和转移灶对治疗反应不一致时,建议对原发灶和转移灶都进行基因检测。
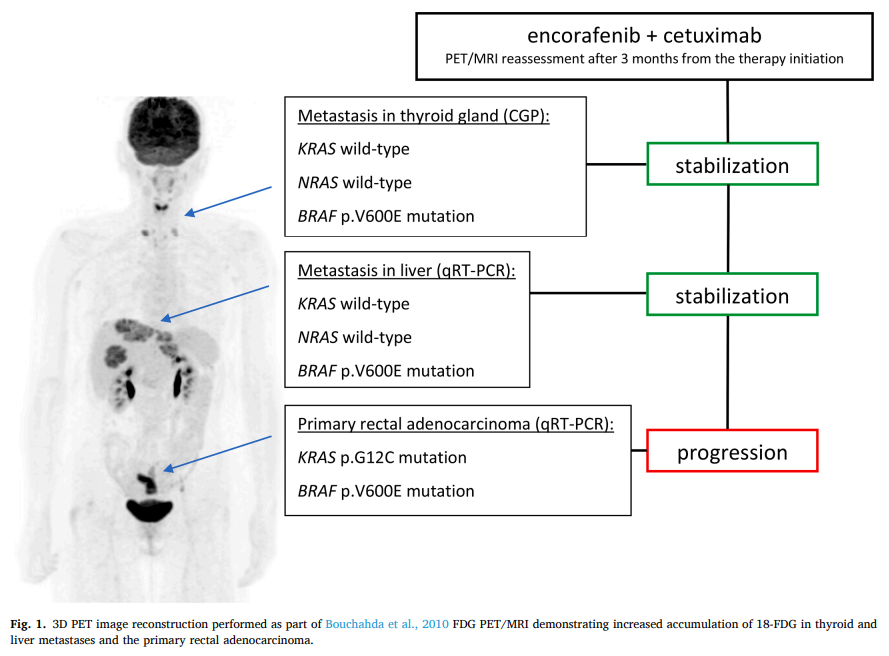
我们举一个例子,一名 44 岁的女性患者诊断为直肠腺癌,伴有肝脏和甲状腺同时性转移。对其原发灶进行基因检测,结果显示KRAS和BRAF基因突变。患者开始FOLFOXIRI联合贝伐珠单抗系统治疗。后续疾病进展后,甲状腺转移灶和肝转移灶进一步检测发现BRAF突变,但KRAS和NRAS基因仍旧为野生型。患者接受了BRAF抑制剂恩考芬尼和抗EGFR单克隆抗体西妥昔单抗治疗。治疗效果显示,联合治疗使两个未携带KRAS突变的转移灶病情稳定,同时存在KRAS和BRAF突变的原发肿瘤则对治疗没有反应。总体上,采用的治疗方案提高了患者的总生存期和生活质量。






绘真:3.恩考芬尼联合西妥昔单抗治疗BRAF V600E突变结直肠癌患者疗效如何?
赵振国教授:
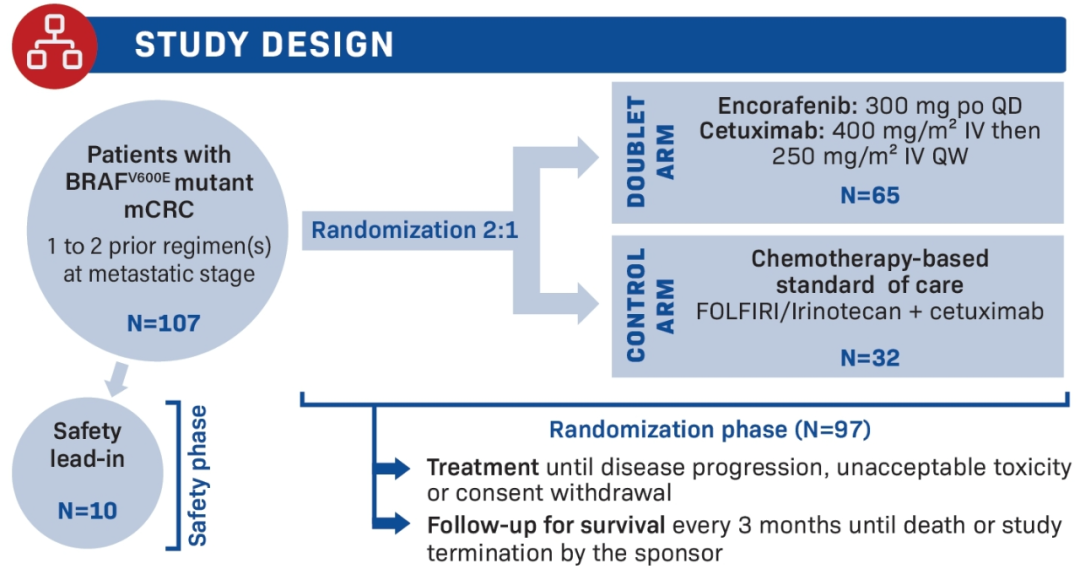
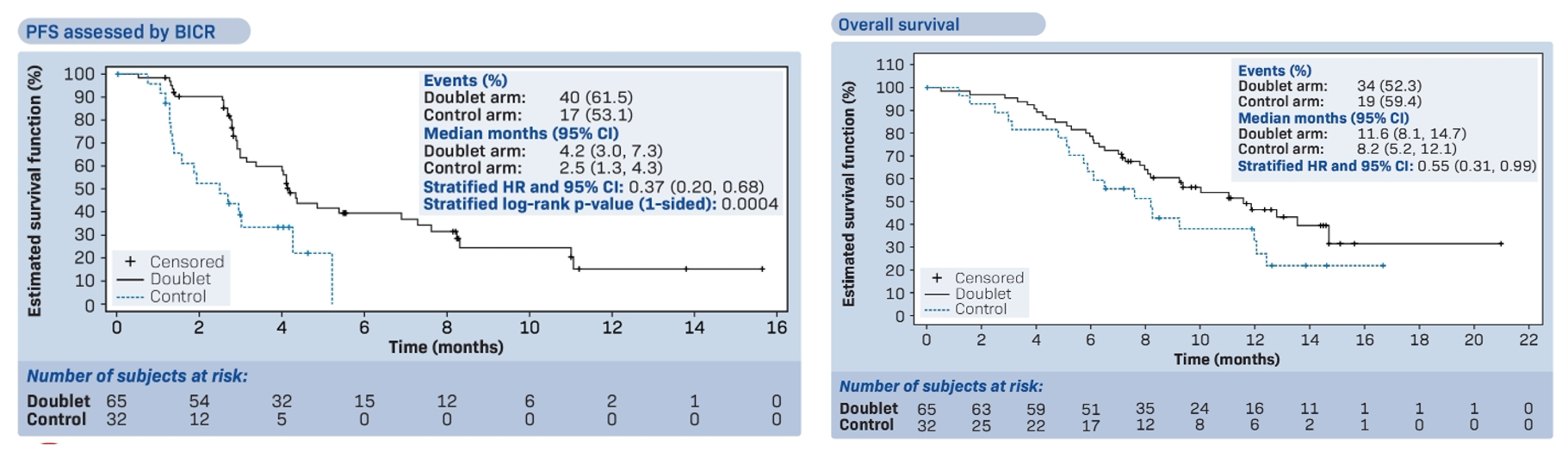
转移性结直肠癌患者中BRAF基因的突变率一般为 5%-10%,其中 90% 以上突变位点是V600E位点。今年 7 月份,恩考芬尼和西妥昔单抗的联合疗法获得NMPA批准,用于既往接受过系统治疗的BRAF V600E突变型转移性结直肠癌成人患者。在中国开展的桥接试验NAUTICAL CRC研究中,恩考芬尼+西妥昔单抗组和伊立替康/FOLIFIRI+西妥昔单抗组的中位无进展生存期(PFS)分别为 4.2 个月和 2.5 个月(HR 0.37, 95%CI 0.20-0.68,P=0.0004),中位总生存期(OS)分别为 11.6 个月和 8.2 个月(HR 0.55,95%CI 0.31-0.99)。可以看到恩考芬尼更优。
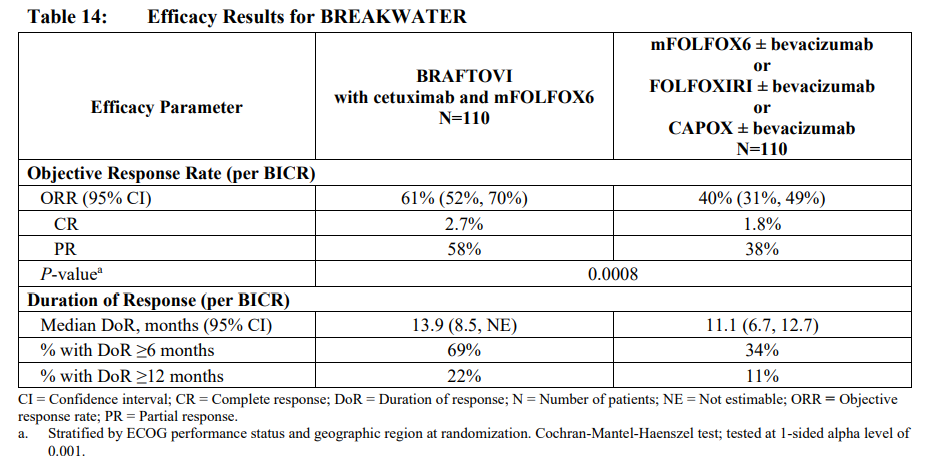
针对BRAF V600E突变结直肠癌患者的一线治疗,去年年底,FDA加速批准了恩考芬尼联合西妥昔单抗和mFOLFOX6治疗方案。研究显示,试验组的客观缓解率(ORR)为 61%,而对照组仅为 40%,中位缓解持续时间(DoR)分别为 13.9 个月和 11.1 个月。我们可以看到恩考芬尼联合西妥昔单抗不管是一线还是后线治疗,效果更好。我们也希望该联合疗法能够尽快在国内上市,以便给患者提供更多的治疗选择。



绘真:4.结直肠癌患者为何还需关注HER2扩增/过表达?
赵振国教授:
在结直肠癌中,HER2扩增或过表达的发生率仅为 3% 左右,但在RAS/BRAF野生型肿瘤中,其发生率较高,达到 5%-14%。
NCCN指南建议,对所有转移性结直肠癌患者进行HER2扩增检测。诊断检测可通过免疫组化(IHC)、荧光原位杂交(FISH)或二代测序(NGS)进行。对于HER2 IHC 3+、IHC 2+/ISH+或NGS检测显示扩增,且RAS和BRAF为野生型的结直肠癌患者,推荐使用抗HER2治疗,包括曲妥珠单抗+(帕妥珠单抗或图卡替尼或拉帕替尼)。指南推荐德曲妥珠单抗仅用于HER2扩增(IHC 3+)的肿瘤。
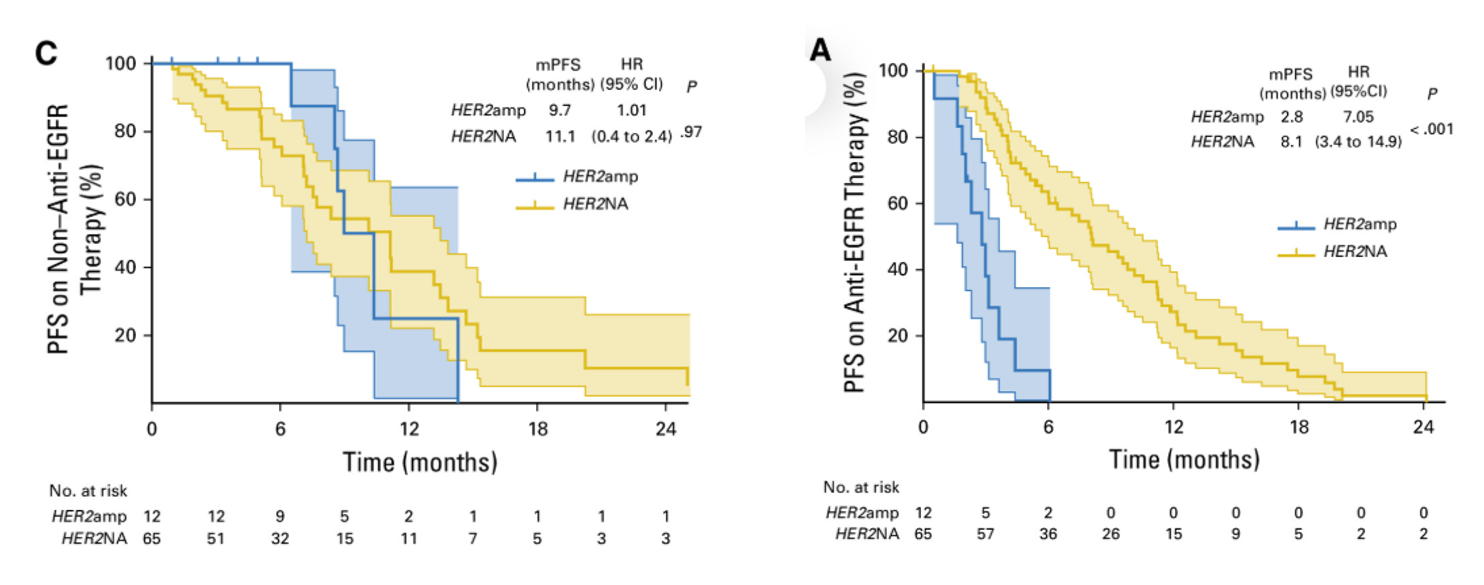
在一项纳入 98 例RAS/BRAF野生型转移性结直肠癌患者的队列研究中,未使用EGFR抑制剂治疗时,无论HER2状态如何,中位PFS相近。然而,在使用EGFR抑制剂治疗同时,HER2扩增患者的PFS显著短于无HER2扩增患者(2.8 个月vs 8.1 个月)。尽管HER2扩增或过表达在预后中的作用存在争议,但临床数据表明,HER2扩增或过表达可作为抗EGFR治疗反应的负预测性生物标志物。




绘真:5.NCCN指南推荐晚期小肠腺癌患者进行哪些分子检测?
赵振国教授:
原发性小肠癌作为一种罕见的消化道肿瘤,起源于小肠内壁分泌黏液的细胞,多为腺癌,占 30%-40%。小肠肿瘤患者因缺乏特异性临床表现,导致疾病早期诊断困难,一般发现时已处于中晚期,其 5 年生存率也比较低,不足 30%。
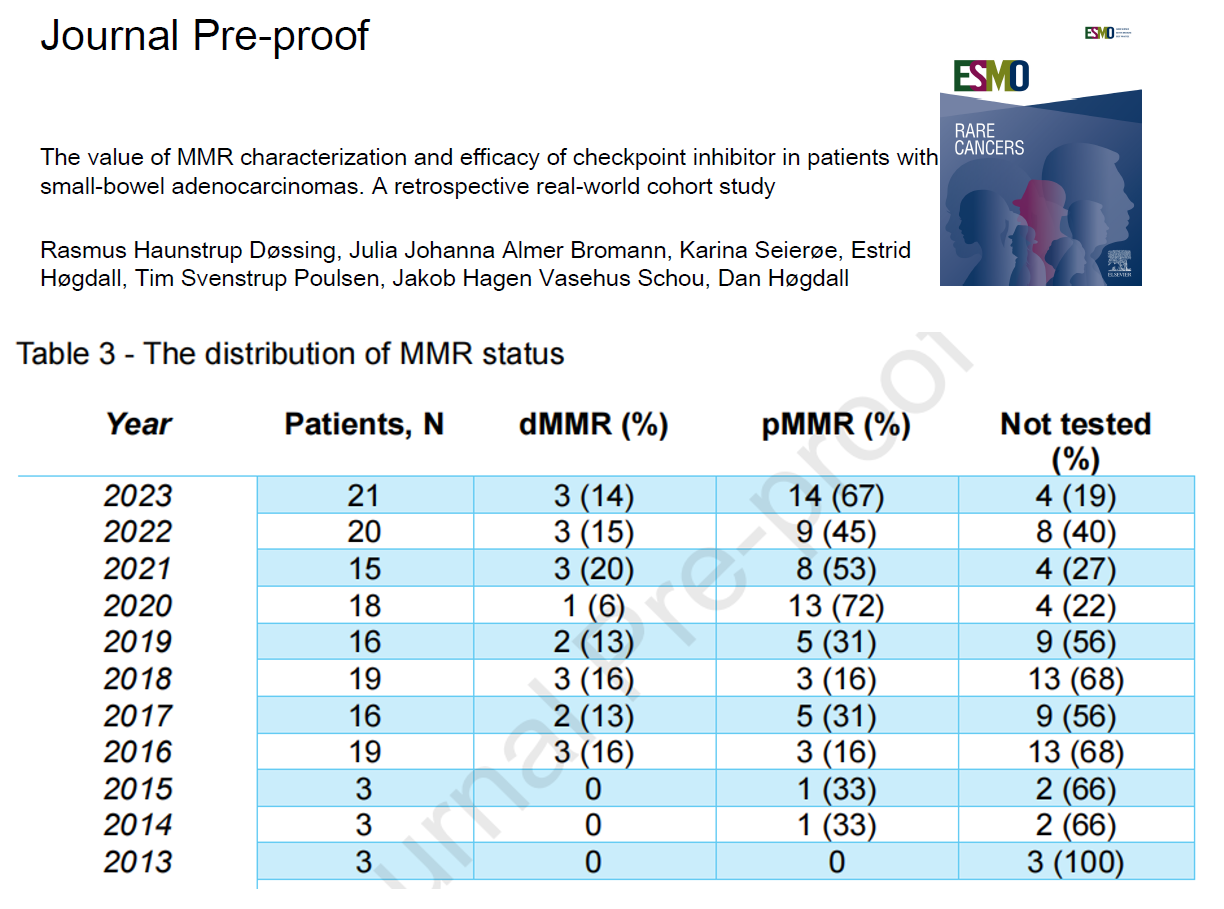
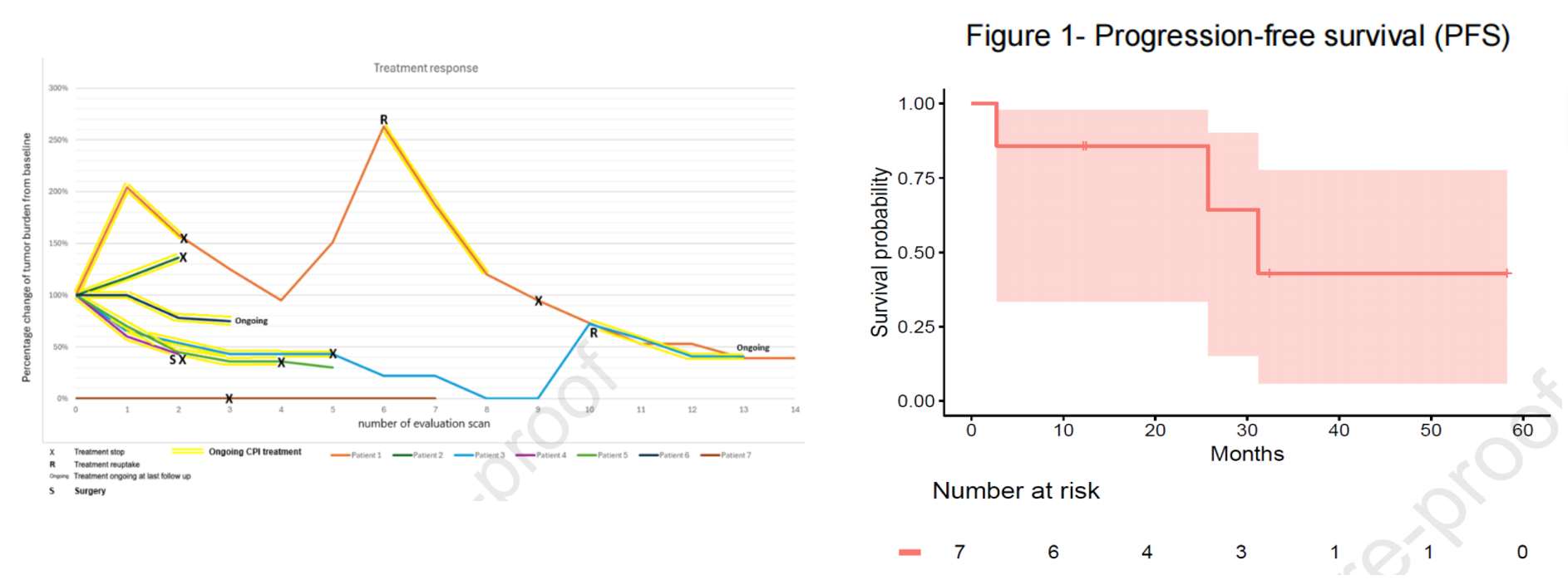
针对转移性小肠腺癌的全身治疗,NCCN指南推荐的分子检测有以下几个:BRAF V600E突变检测指导达拉非尼+曲美替尼治疗,KRAS G12C突变检测指导索托雷塞和阿达格拉西布,HER2扩增检测指导德曲妥珠单抗,以及泛癌种靶点NTRK、RET融合基因检测,此外还推荐了免疫治疗效果评价相关指标dMMR/MSI-H、POLE/POLD1突变以及TMB-H。一项真实世界研究也表明 ,在接受MMR蛋白检测的 85 例小肠腺癌中,15 例(18%)被归类为dMMR型,其中 7 例接受了免疫治疗,结果还是比较好的,6 例获得了客观缓解,并且疗效持久,中位无进展生存期(mPFS)达到了 31 个月。
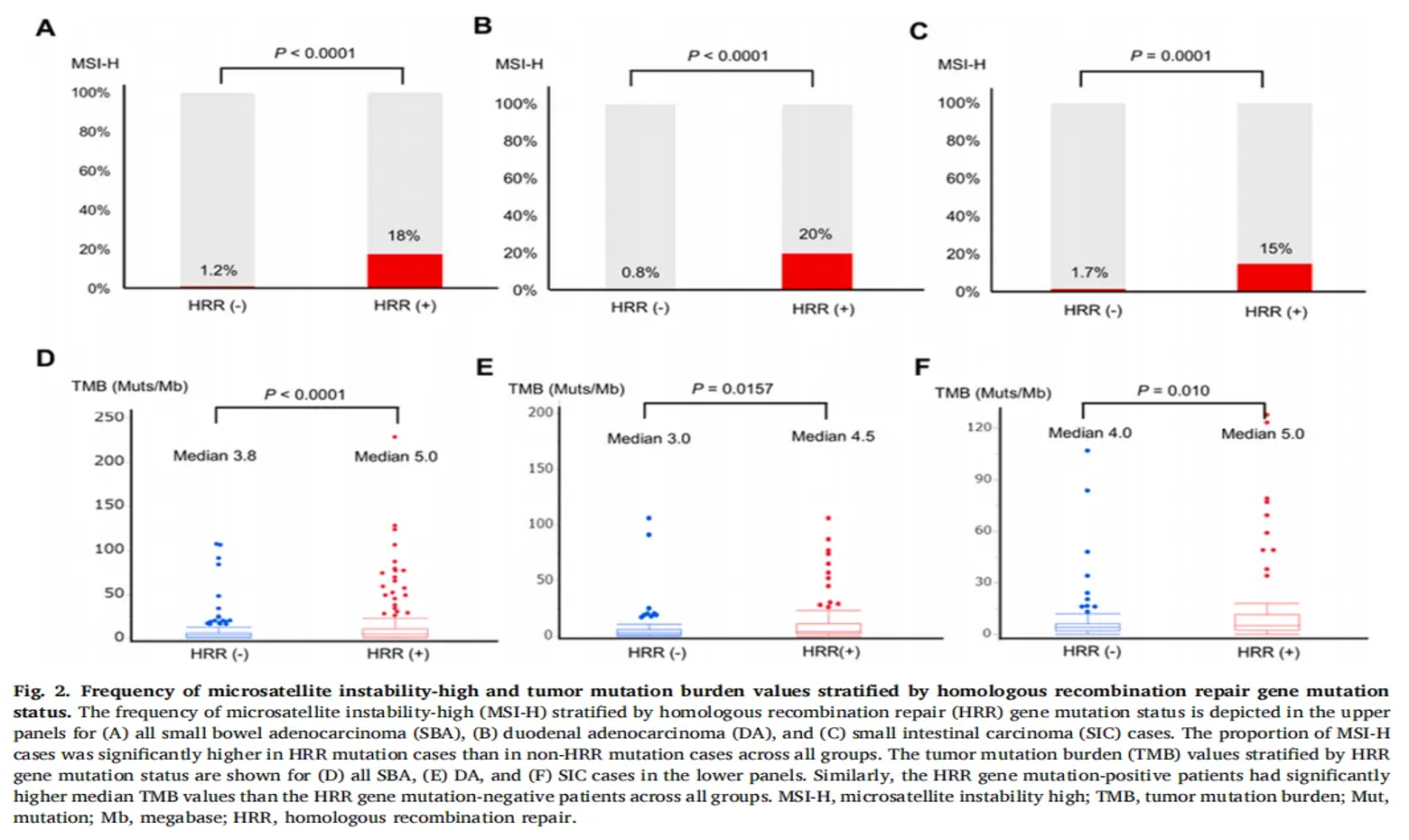
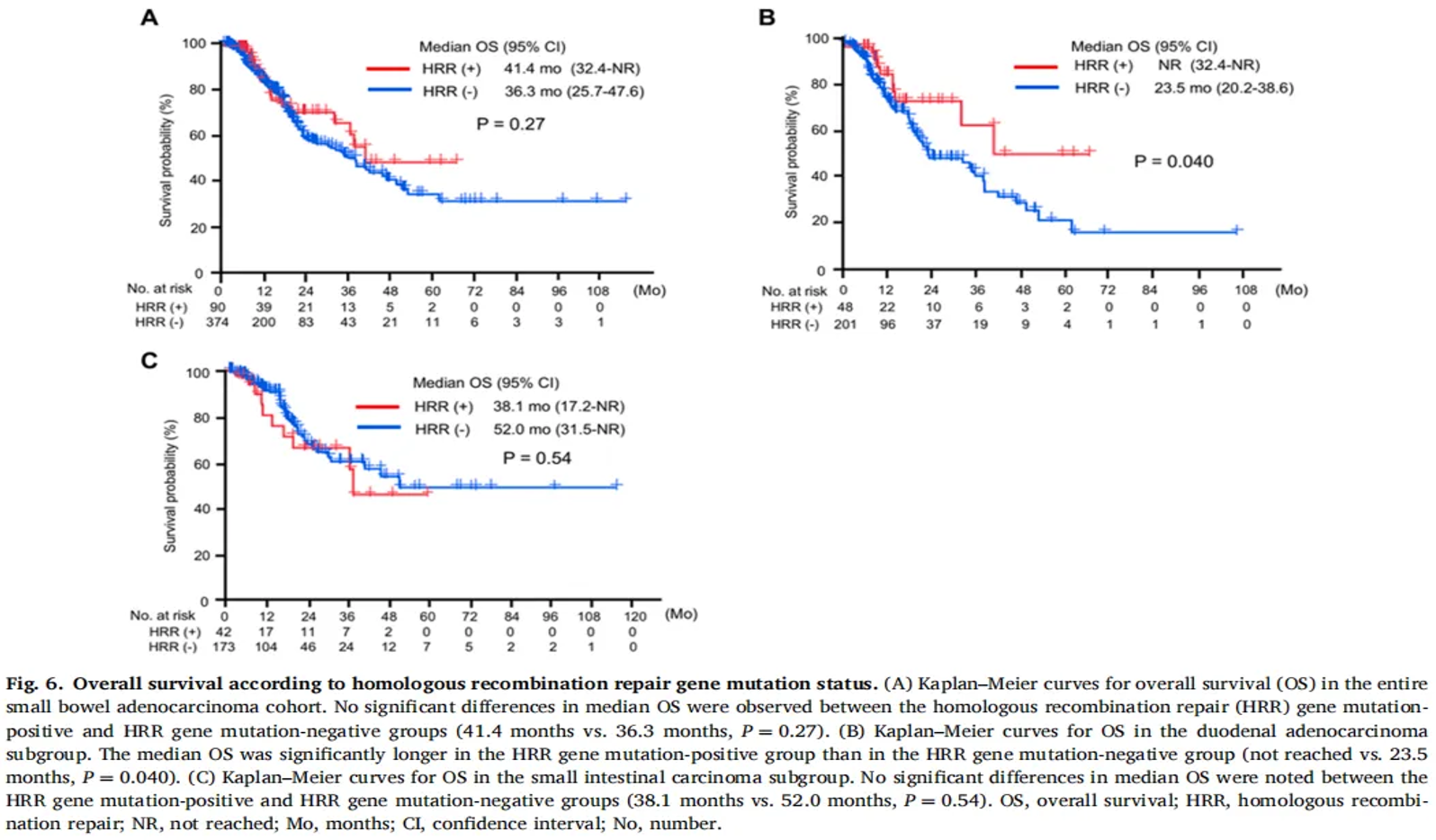
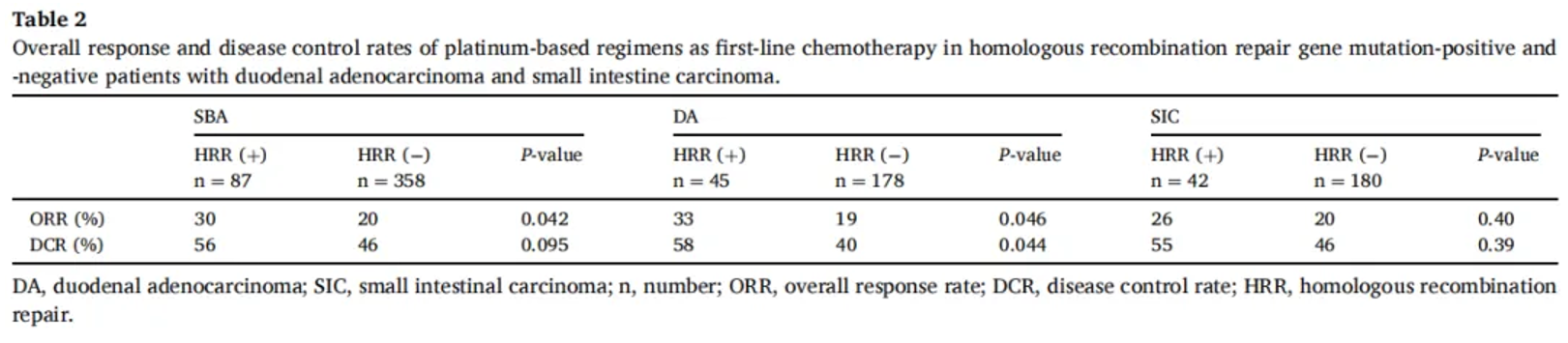
目前,还有其他一些分子指标正处于临床试验阶段,其中多个指标已取得阳性结果,例如HRR相关基因突变。有研究显示,在小肠腺癌中HRR相关基因突变阳性与更高的MSI-H发生率相关,也与更高的TMB水平相关。在十二指肠腺癌中,HRR相关基因突变阳性总体治疗效果更好,获得更长的总生存期(OS)。也表明HRR相关基因突变对铂类化疗敏感性更好,有更高的缓解率。




- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)