首页 > 医疗资讯/ 正文
屋外大雨滂沱,这也太适合睡觉了吧;外面寒风萧瑟,这也太适合睡觉了吧;阳光炙烤大地,空气仿佛凝固,这也太适合睡觉了吧……仿佛人生中任何一种天气,都是钻进被窝、闭上眼睛、灵魂暂时离线的完美借口。尤其在忙碌一天后,那种“裹进棉被就像沉入云端”的幸福感,几乎能治愈一天的疲惫,怎么睡都睡不够。
但奇怪的是——总有那么一小撮“异类”,他们每天只睡四五个小时,却精神奕奕、思维清晰,不靠咖啡提神、不靠闹钟叫醒,连周末都不怎么补觉。他们真的是“天赋异禀”吗?还是藏着某种我们尚未解锁的科学原理?
近期来自中国科学院联合加州大学旧金山分校的研究团队发表在《美国国家科学院院刊》(PNAS)上的一项研究[1],终于为这种“睡得少还不困”的神奇现象揭开了冰山一角的面纱。研究聚焦于盐诱导激酶3(SIK3)基因,发现其N783Y突变竟可以“天赋短睡”而不疲惫。

“天赋短睡”基因的发现
这些“天赋短睡者”在学术上有个更正式的名字——功能性自然短睡者(FNSS)。他们不仅睡得短,还睡得香、精神好,身体也倍儿棒,堪称睡眠界的“开挂选手”。那么问题来了:他们到底是怎么做到的?
为了解开这个谜团,研究人员找到了这项研究的“主角”——一位主观报告自己每天只睡约3小时,并且在这种短睡状态下认知和生理功能并未受到影响的受试者。
研究团队当然不愿放过这个“顺藤摸瓜”的机会,于是开展了全外显子组测序,试图在她的基因中找到隐藏的“短睡密码”。经过层层筛查和数据比对,最终缩小到6个可能与短睡表型相关的基因突变。而在这6个候选中,有一个名字格外醒目——SIK3。
为什么SIK3这么值得关注?因为早在小鼠模型的研究中,这个基因就已经被发现与睡眠时长密切相关。简单来说,它曾经“有案底”,现在在人类短睡者身上再次被“点名”,自然要重点关注。
果不其然,研究人员很快发现了一个关键细节:这位受试者的SIK3基因在第783号氨基酸位置发生了一个小小的突变——原本是天冬酰胺(Asparagine,N),却被替换成了酪氨酸(Tyrosine,Y),这个突变就被命名为N783Y突变。
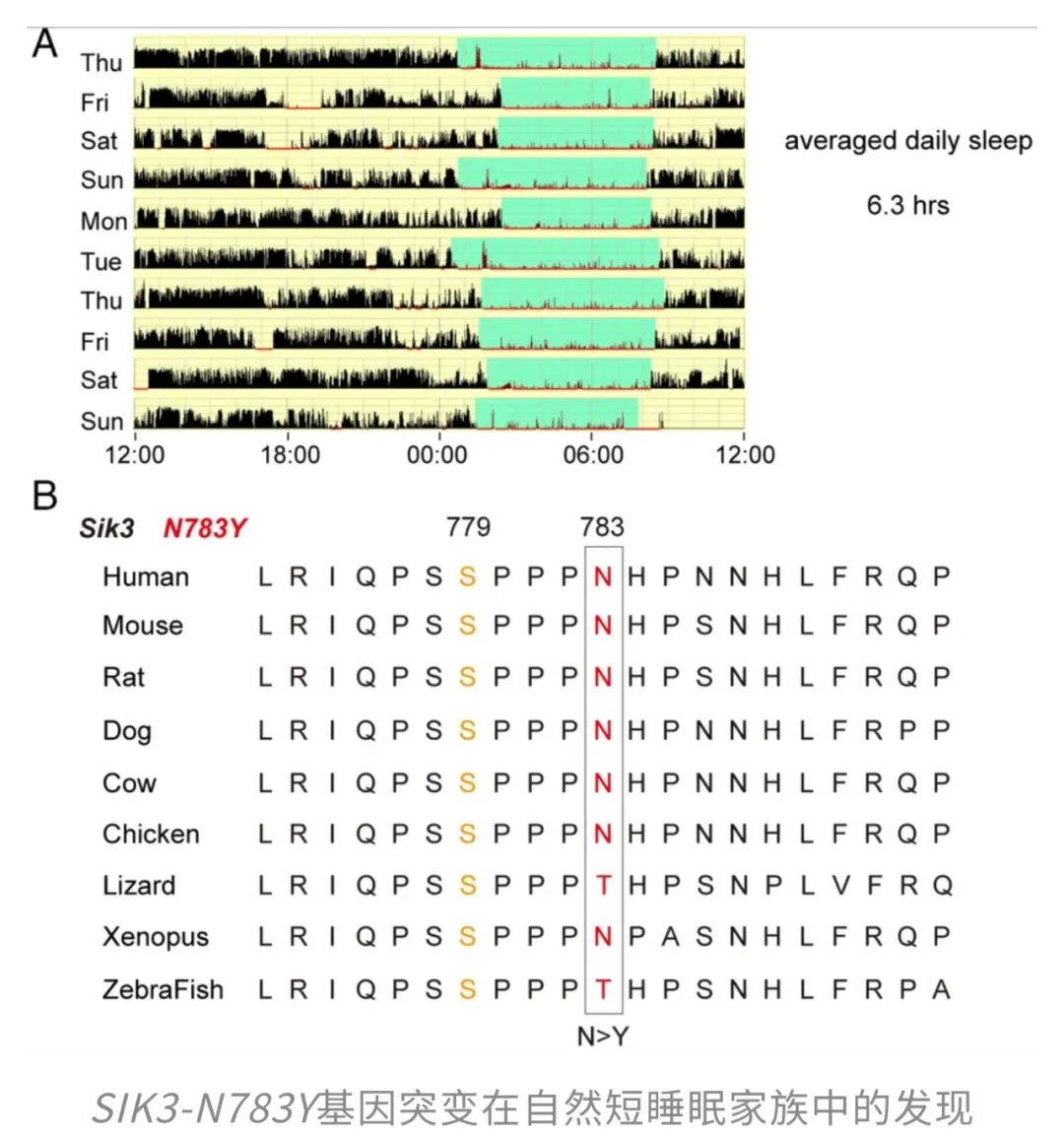
睡觉的“开关系统”被精简成高效版
为了进一步揭示SIK3-N783Y突变为何会让人“睡得短还不困”,研究人员决定从分子层面下手,看看这个小小的突变有没有影响SIK3的“老本行”——也就是它作为激酶的催化功能。
此前的研究已经发现,SIK3在调控睡眠这件事上很有发言权。它的工作方式是通过磷酸化某些下游蛋白质,让这些“执行者”去调控我们什么时候该睡觉、什么时候该清醒。而在这些被磷酸化的底物中,有两个特别重要的角色:HDAC4和HDAC5,它们在睡眠-觉醒周期中扮演着关键角色。
为了验证突变后的SIK3是否还能胜任工作,研究人员搭建了一个“体外激酶实验平台”来模拟SIK3和HDAC4/5之间的相互作用。结果显示,无论是野生型还是突变型的SIK3,都能够对HDAC4和HDAC5进行磷酸化。这说明,N783Y突变并未完全破坏SIK3的功能,它依然保留了部分催化能力。
不过,突变后的SIK3工作效率明显下降,表现得有点像“带薪摸鱼”的员工。这种状态在学界被称为“减弱型突变”——功能没完全丧失,但大打折扣。而它“指挥”下的HDAC4和HDAC5也变得“不太活跃”,整个睡眠调控网络的节奏因此发生了微妙的变化。
这可能也就解释了,为什么N783Y突变携带者虽然睡得少,但并不会像“睡眠不足党”那样状态崩塌、精神萎靡——他们体内的“睡眠控制系统”从根源上就被重新调了节奏,工作效率虽低,但运行模式更加高效。换句话说,他们不是不需要睡觉,而是睡觉的“开关系统”被精简成了高效版。
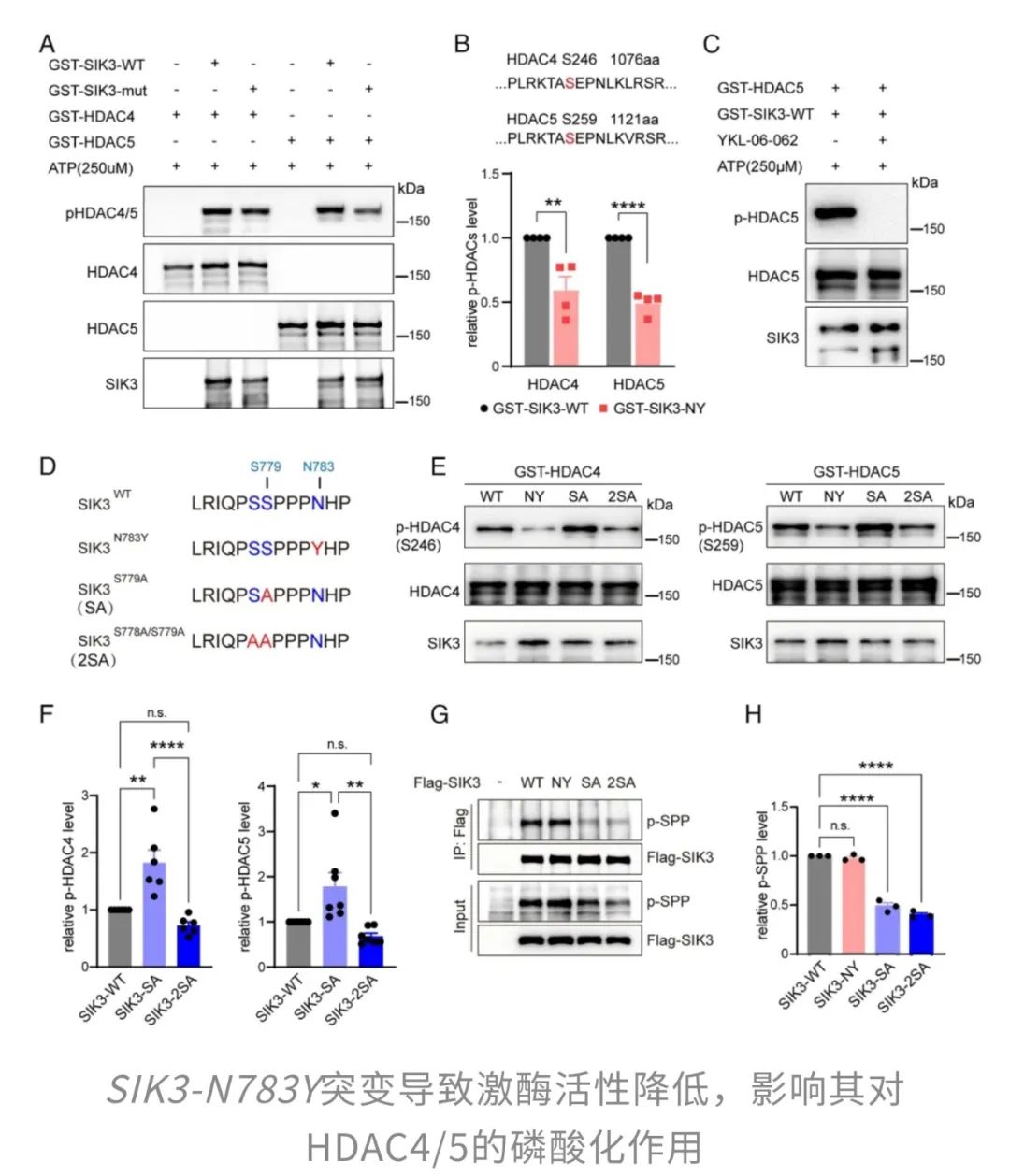
SIK3突变让小鼠自带“快充睡眠模式”
为了揭开SIK3-N783Y突变是否真的是“自然短睡”背后的操盘手,研究人员把N783Y突变精准引入小鼠身上,他们构建了一种基因编辑小鼠模型。接下来,就是观察这些“小鼠版短睡者”是否也会展现出相似的节省睡眠时间的能力。

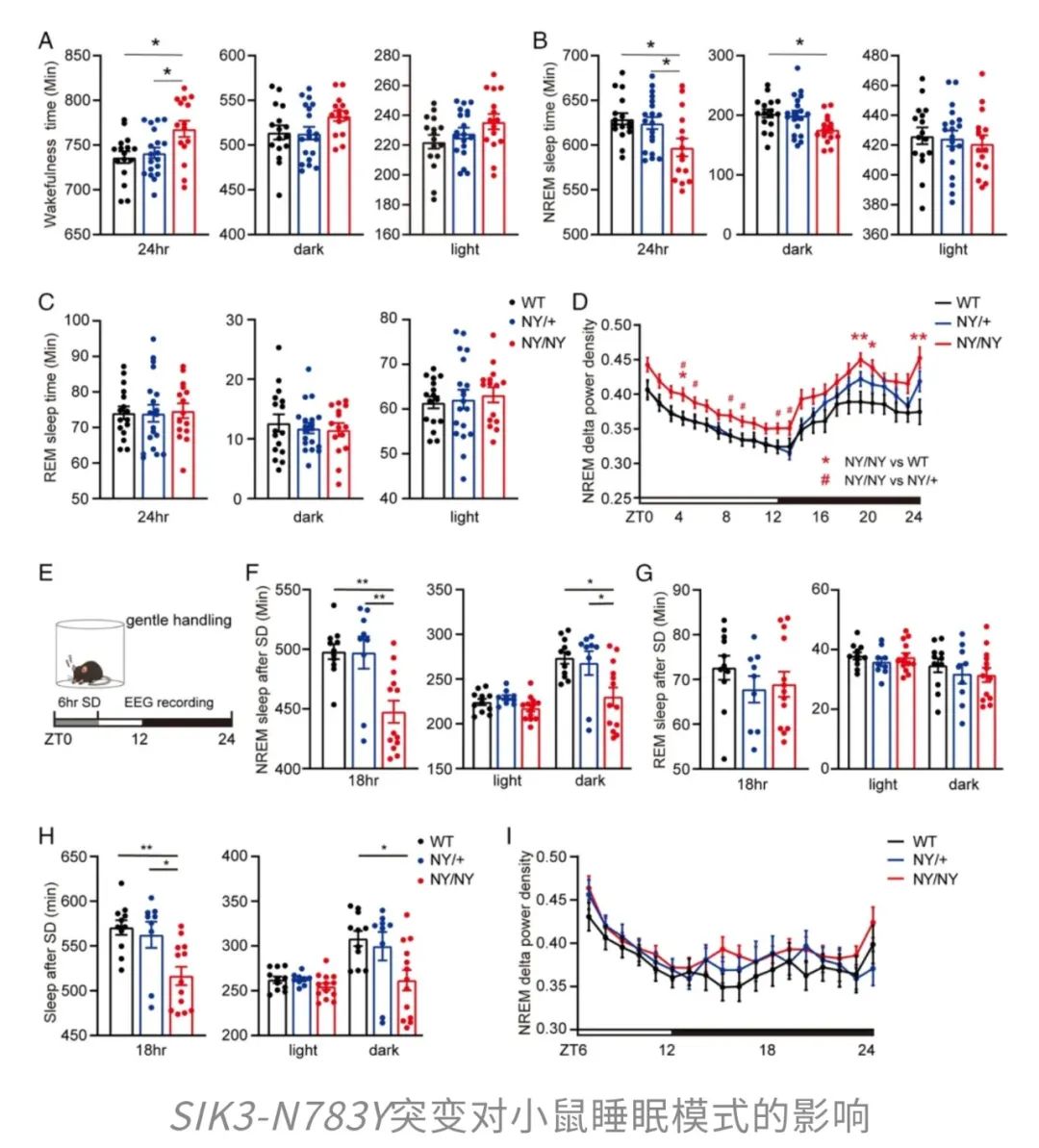
结果这些纯合子小鼠再次“反常发挥”——补觉时间竟然比正常小鼠还要少了54分钟,好像根本不太在意睡眠被打断这回事儿。
更有趣的是,虽然这些突变小鼠睡得比正常小鼠少,但它们在非快速眼动睡眠(NREM)阶段的脑电波中,δ波功率却显著升高——这个指标正是衡量睡眠深度和恢复效率的重要信号。也就是说,它们在单位时间里的睡眠“质量”更高,恢复效率更强。更为形象地理解,它们的大脑类似充电效率特别高的“快充模式”——哪怕睡得短,也能充得满。
回到分子机制层面,这一系列现象其实都可以追溯到SIK3的“懒惰表现”。N783Y突变削弱了这种激酶的工作效率,导致它在给下游蛋白打“磷酸标签”时没那么积极。而这种磷酸化状态的变化,进而扰动了睡眠调控网络的节奏,最终塑造出了这样一种高效、节约型的睡眠模式。
研究人员进一步指出,目前已经发现了数百名“天生睡得少”的人群,也已在4个基因中找到了5种可能与这种短睡表型相关的突变。
这项新研究的意义也正是在于此:它首次在人体中确认SIK3基因的N783Y突变与自然短睡密切相关。通过将该突变引入小鼠并观察到相似的短睡现象,不仅进一步丰富了我们对人类睡眠遗传机制的理解,也为未来探索高效睡眠的可能性打开了新的大门。
短睡基因之二:NPSR1-Y206H突变
如果说SIK3-N783Y突变只是“短睡基因”冰山一角,那接下来的主角NPSR1-Y206H突变,无疑让这一神秘现象更加耐人寻味。它也引起了美国加利福尼亚大学研究团队的高度关注[2]。

简单来说,NPSR1是一种接收“神经肽S”(NPS)信号的受体,相当于大脑内部的“唤醒按钮”。而这次发现的Y206H突变,让这个按钮变得更加灵敏,就像有人把闹钟调成了“震天响”,一有动静就立马清醒。

更令人瞠目的是,就算剥夺它们的睡眠,积累了不少“睡眠债”,它们也没有像正常小鼠那样赶紧“补觉”,似乎天生就对睡眠压力免疫。
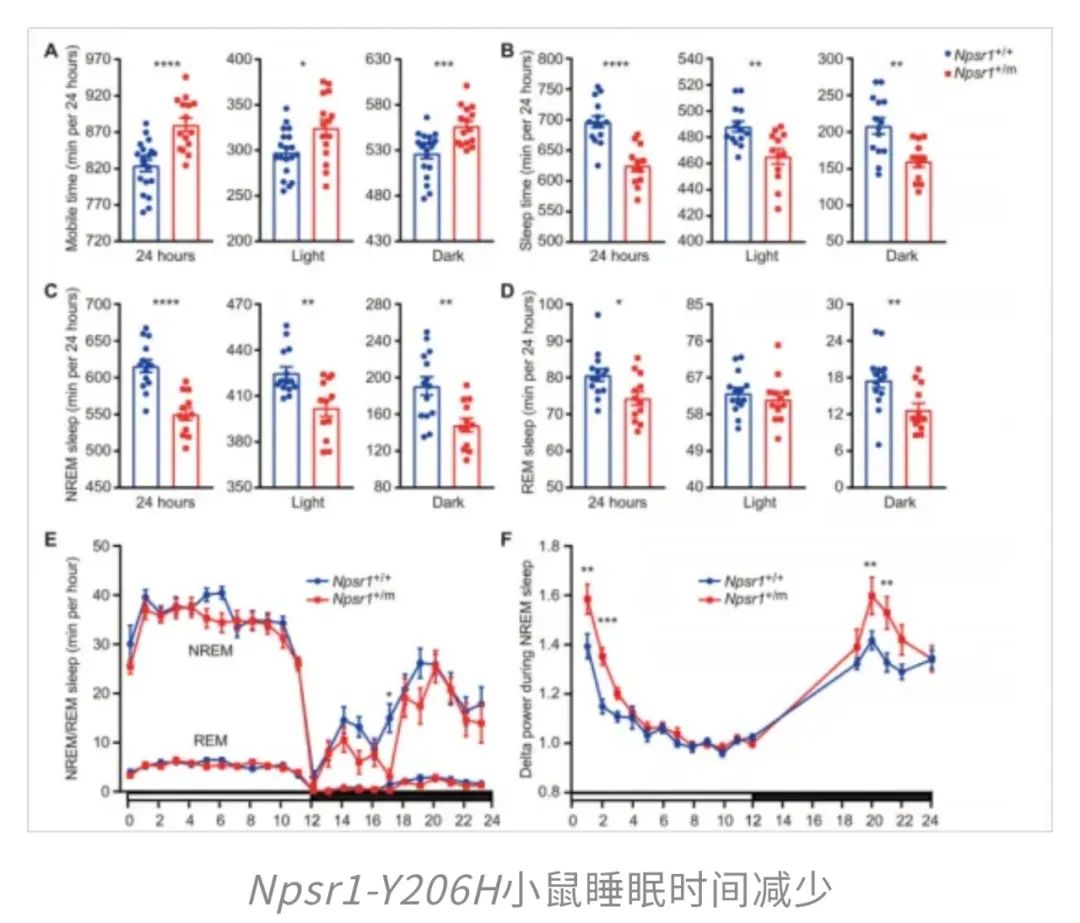
更神奇的部分还在后头。通常情况下,睡得少是会“脑子不转弯”的,尤其会影响记忆力。但这些小鼠在经历睡眠剥夺后,居然还能准确记住曾经待过的环境,表现出惊人的记忆保留力。这抗遗忘的能力,简直让“熬夜党”羡慕到哭泣。
短睡基因之三:GRM1的两种突变
无独有偶,在揭开“短睡基因”神秘面纱的旅程中,研究者又发现了另一位“幕后玩家”——GRM1基因[3]。

GRM1编码的是一种谷氨酸受体(mGluR1),在调节神经元兴奋性和突触可塑性方面扮演着重要角色,过去更多被研究于学习记忆领域,如今却也与“睡得少”扯上了关系。

短睡基因之四:ADRB1-A187V 突变
这一发现来自美国加利福尼亚大学研究团队,发表在Neuron的最新研究[4]进一步拓展了“短睡基因家族”的成员名单。研究人员发现,在一类自然短睡个体中,存在一个特别的突变:β1-AR基因中的A187V突变。这可不是个普通的基因,它编码的受体,是大脑中专门用来“接收去甲肾上腺素(NE)信号”的关键枢纽,直接参与清醒状态的维持以及快速眼动(REM)睡眠的调控。
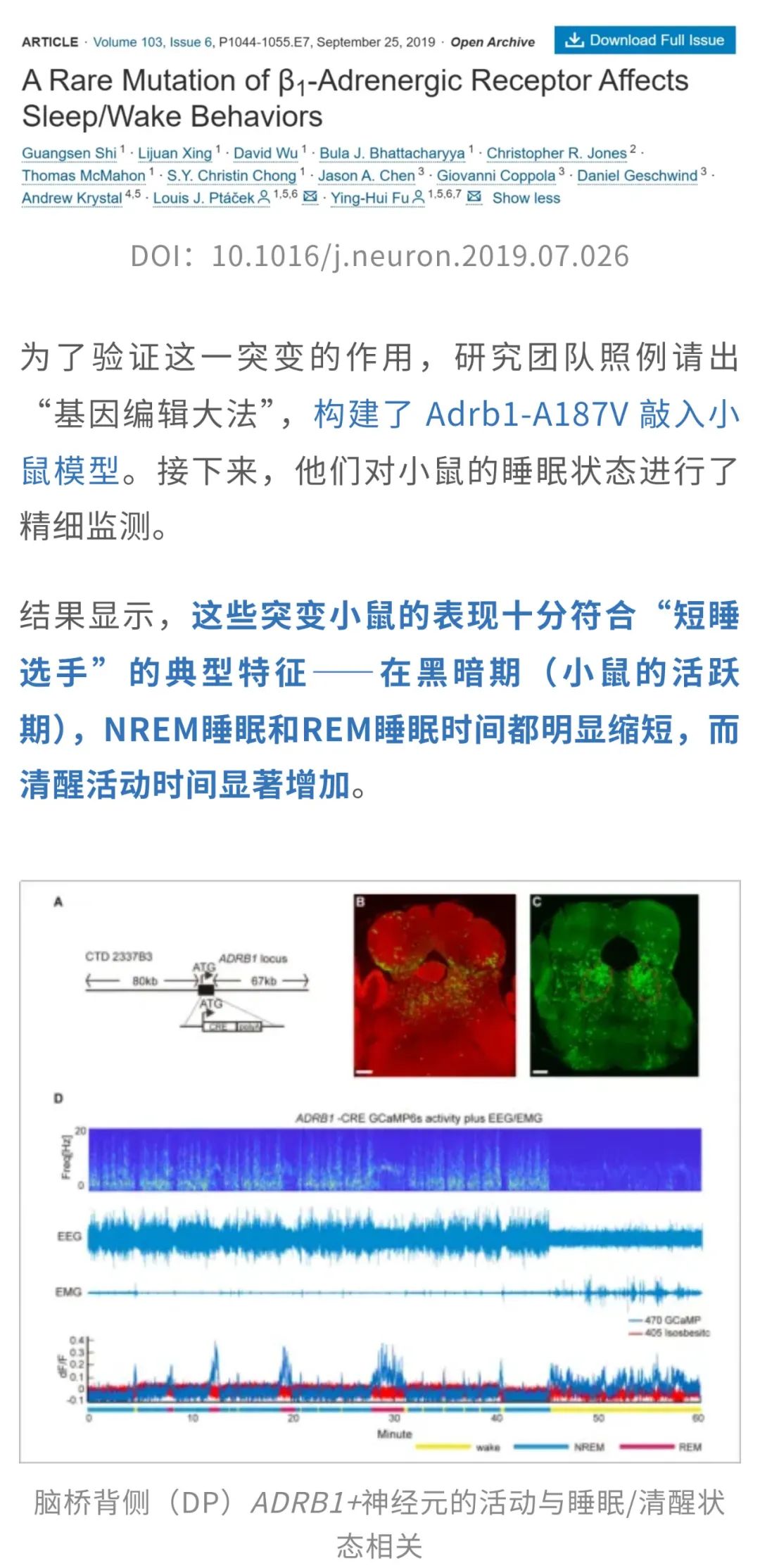
至此,我们不难发现,“短睡基因家族”正在不断扩容。每一项新发现都像拼图中的一块关键拼板,逐步勾勒出一个错综复杂、却又高度协调的睡眠调控网络。
不禁让人畅想:如果有一天,我们真正解锁了这套“睡眠黑科技”——也许只需要几个小时的睡眠,就能换来过去数十倍时间才能达成的深度休息,那将意味着什么?一觉醒来,身体“满电”、头脑清醒,从此不再为每天能睡几个小时而焦虑,也不再被困意困住生活节奏。节省下来的时间,或许能用来体验更丰富的人生、完成更多热爱的事。
仍需指出的是,上述几项研究尽管在小鼠模型中观察到睡眠时间减少等现象,但尚未完全明确这些基因在人类自然短睡眠中的具体作用机制及潜在的治疗应用前景。
参考资料:
[1]Chen H, Xing Y, Wan C, Zhang Z, Shi Z, Liang Y, Jin C, Chen Y, Zhou X, Xu J, Ptáček LJ, Fu YH, Shi G. The SIK3-N783Y mutation is associated with the human natural short sleep trait. Proc Natl Acad Sci U S A. 2025 May 13;122(19):e2500356122. doi: 10.1073/pnas.2500356122. Epub 2025 May 5. PMID: 40324078.
[2]Xing L, Shi G, Mostovoy Y, Gentry NW, Fan Z, McMahon TB, Kwok PY, Jones CR, Ptáček LJ, Fu YH. Mutant neuropeptide S receptor reduces sleep duration with preserved memory consolidation. Sci Transl Med. 2019 Oct 16;11(514):eaax2014. doi: 10.1126/scitranslmed.aax2014. PMID: 31619542; PMCID: PMC7587149.
[3]Shi G, Yin C, Fan Z, Xing L, Mostovoy Y, Kwok PY, Ashbrook LH, Krystal AD, Ptáček LJ, Fu YH. Mutations in Metabotropic Glutamate Receptor 1 Contribute to Natural Short Sleep Trait. Curr Biol. 2021 Jan 11;31(1):13-24.e4. doi: 10.1016/j.cub.2020.09.071. Epub 2020 Oct 15. PMID: 33065013.
[4]Shi G, Xing L, Wu D, Bhattacharyya BJ, Jones CR, McMahon T, Chong SYC, Chen JA, Coppola G, Geschwind D, Krystal A, Ptáček LJ, Fu YH. A Rare Mutation of β1-Adrenergic Receptor Affects Sleep/Wake Behaviors. Neuron. 2019 Sep 25;103(6):1044-1055.e7. doi: 10.1016/j.neuron.2019.07.026. Epub 2019 Aug 28. PMID: 31473062; PMCID: PMC6763376.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)