首页 > 医疗资讯/ 正文
虽然检查点免疫疗法能够有效调动T细胞应答对抗肿瘤,但其在肝细胞癌 (HCC) 中的疗效常常受到肿瘤微环境中免疫抑制性髓系细胞的抑制。
2025 年 4 月 30 日,复旦大学附属中山医院代智和余一祎共同通讯在Advanced Science 在线发表题为“Lactylation-Driven NUPR1 Promotes Immunosuppression of Tumor-Infiltrating Macrophages in Hepatocellular Carcinoma”的研究论文。该研究探讨了核蛋白1 (NUPR1) 基因在肿瘤相关巨噬细胞 (TAM) 中主要表达,该基因在介导这种抑制并影响免疫治疗结果中的作用。
通过对单细胞RNA测序 (scRNA-seq) 数据集以及体内外功能分析的全面分析,NUPR1 被确定为TAM 中的关键调控因子。NUPR1 的上调与M2巨噬细胞极化增强以及免疫检查点PD-L1和SIRPA表达增加相关,从而导致CD8+ T细胞耗竭和免疫治疗反应减弱。从机制上讲,NUPR1抑制了ERK和JNK信号通路,从而创造了有利于肿瘤进展的免疫抑制环境。此外,肿瘤来源的乳酸已被证明可通过组蛋白乳酸化上调巨噬细胞中NUPR1的表达,从而维持一个强化免疫抑制的反馈回路。NUPR1的药物靶向作用可逆转M2极化,抑制肿瘤生长,并在临床前模型中增强PD-1阻断剂的疗效,这使得NUPR1既可以作为免疫治疗反应性的潜在生物标志物,也可以作为增强HCC免疫治疗疗效的治疗靶点。

肝细胞癌 (HCC) 是全球最致命的癌症之一,其高发病率给人类带来了沉重的健康负担。传统上,肝切除术是治疗的基石;然而,术后高复发率限制了其疗效。近年来,免疫疗法,尤其是针对程序性细胞死亡受体 (PD-1/PD-L1) 轴的免疫疗法,已成为治疗的关键。尽管免疫疗法在黑色素瘤等癌症中取得了成功,但在肝细胞癌中的缓解率仍然较低(15-30%),且总生存期获益通常微乎其微。免疫抑制性肿瘤微环境 (TME) 是导致肝细胞癌免疫疗法耐药性的一个重要因素。因此,阐明并靶向这种免疫抑制的机制对于改善肝细胞癌患者的免疫疗法疗效至关重要。
肝脏作为免疫豁免器官,含有大量巨噬细胞,包括组织驻留型库普弗细胞和单核细胞衍生的巨噬细胞。这些细胞在肝细胞癌(HCC)的进展中起着关键作用,具有双重作用:它们可以通过抗原呈递和吞噬作用发挥抗肿瘤作用;相反,当它们被重编程为类似于M2巨噬细胞的肿瘤相关巨噬细胞 (TAM) 时,则促进肿瘤进展。TAM 具有显著的可塑性,其表型、代谢和功能特征多样,这不仅凸显了它们在免疫抑制中的作用,也为治疗干预提供了窗口。揭示 TAM 的分子特征并识别关键的巨噬细胞亚群对于逆转肿瘤微环境 (TME) 的免疫抑制状态和增强免疫检查点阻断 (ICB) 疗法的疗效至关重要。
(图源自Advanced Science )
NUPR1,即核蛋白1,是一种转录调控因子,参与多种细胞过程,包括细胞凋亡、细胞周期调控和DNA修复。在胰腺癌、乳腺癌和肝癌等多种癌症中,NUPR1通常过表达,并参与肿瘤的存活、增殖和化疗耐药性。值得注意的是,传统上用于治疗精神症状的三氟拉嗪和ZZW-115等化合物已被鉴定为NUPR1的选择性抑制剂,凸显了其作为癌症治疗靶点的潜力。然而,目前的研究主要集中在肿瘤细胞内的NUPR1,其在肿瘤微环境中的作用仍未得到充分探索。因此,全面分析NUPR1如何影响肿瘤微环境对于将这些发现转化为临床应用至关重要。这有可能增强治疗策略,并加深对肿瘤生物学与免疫调节关系的理解。
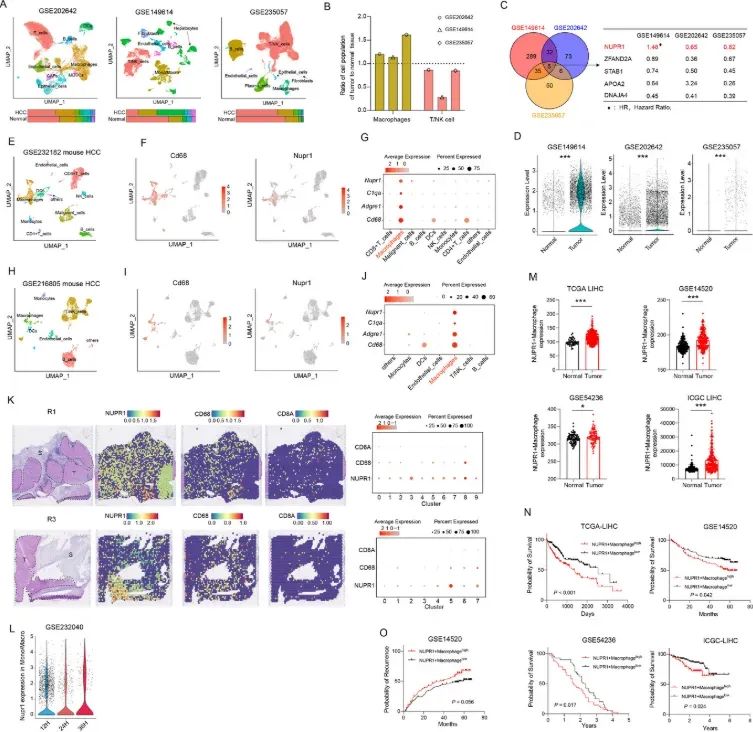
本研究利用高通量单细胞RNA测序(scRNA-seq)揭示NUPR1主要在HCC微环境中的TAM中表达。与NUPR1低表达的巨噬细胞相比,NUPR1高表达的巨噬细胞表现出较低的促炎和T细胞支持功能。药理学抑制NUPR1可增强HCC肿瘤对抗PD-1疗法的体内敏感性。此外,我们发现肿瘤细胞中的乳酸可诱导巨噬细胞组蛋白H3K18乳酸化,从而上调NUPR1转录。本研究揭示了NUPR1在增强HCC免疫检查点阻断(ICB)疗法疗效方面的新作用,为肿瘤免疫逃逸的分子机制提供了新的见解,并概述了靶向TAM以增强T细胞抗肿瘤反应的新策略。
参考消息:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202413095
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)