首页 > 医疗资讯/ 正文
个性化癌症疫苗可激发强大的 T 细胞免疫力和抗肿瘤效力,但鉴定肿瘤特异性抗原仍然具有挑战性,严重限制了治疗窗口。采用癌细胞膜的仿生纳米疫苗显示出固有的生物相容性,并刺激T细胞对多种肿瘤抗原的反应,尽管肿瘤会发展出多种机制来减少抗原呈递。
2025 年 5 月 23 日,复旦大学生物医学研究院罗敏唯一通讯在Nature Communications上在线发表题为“Neoantigen enriched biomimetic nanovaccine for personalized cancer immunotherapy”的研究论文。研究展示了一种基于抗原富集肿瘤细胞膜(AECM)的快速和通用的制备个性化纳米疫苗的策略,用于早期干预。
干扰素-γ可有效刺激多种癌细胞的抗原提呈。通过将产生的AECM与PC7A佐剂(干扰素基因刺激因子[STING]激活聚合物)偶联,AECM@PC7A纳米疫苗即使在低剂量下也可诱导稳健的多新表位T细胞应答,从而在多种小鼠癌症模型中实现了显著的肿瘤消退和转移抑制。这种抗肿瘤应答依赖于MHC-I限制性抗原提呈和CD8+T细胞活化,而树突状细胞主要通过异装将AECM抗原提呈给初始T细胞。AECM@PC7A与不同剂型的疫苗相比,显示出显著的抗肿瘤效果,并在手术后和人源化异种移植肿瘤模型中显示出治疗潜力。这项概念验证研究为快速开发适用于广泛患者的早期干预的个性化癌症疫苗提供了一个有前景的通用途径。

免疫检查点阻断和CAR-T疗法已表明T细胞免疫在癌症免疫治疗中起着核心作用。治疗性癌症疫苗可以通过递送肿瘤抗原和免疫佐剂来诱导有效的抗肿瘤T细胞反应。源自体细胞突变的肿瘤新抗原仅由肿瘤细胞表达,提供了规避自身表位的T细胞中心耐受性的机会,从而诱导肿瘤特异性T细胞反应以根除癌症。已经开发了多种方法来改进新抗原的预测和验证。具有高免疫原性和肿瘤特异性的个性化新抗原疫苗正在临床试验中进行测试,并显示出有希望的结果。然而,目前新抗原发现的效率仍然很低,预测阳性率为<6%。特别是,整个疫苗开发过程非常耗时,通常需要3个月的一轮筛选和准备。因此,治疗窗口受到很大限制,许多癌症患者错过了早期干预,严重限制了基于新抗原的疫苗在临床实践中的广泛应用。需要以快速有效的方式设计个性化癌症疫苗的策略。
使用自体细胞衍生成分的仿生癌症疫苗在个性化免疫治疗中受到广泛关注。癌细胞可以承受来自患者的多种肿瘤抗原,允许多表位细胞毒性T淋巴细胞(CTL)反应,而无需精确的抗原鉴定和合成。使用癌细胞裂解物或辐照全癌细胞的疫苗临床试验一直在黑色素瘤、乳腺癌、胰腺癌、结直肠癌和前列腺癌患者中进行。值得注意的是,癌细胞膜含有已经经过MHC/HLA加工的肿瘤抗原,在触发肿瘤特异性T细胞反应方面具有优势。最近,在基于细胞膜的纳米疫苗的配方中探索了多种癌细胞,以进一步加速对各种T细胞的刺激。这些疫苗能够在体内诱导有效的抗肿瘤反应,并与其他免疫疗法具有良好的协同作用。
然而,肿瘤会发展出多种机制来减少抗原呈递。因此,通常需要高剂量的基于癌细胞的疫苗来引发肿瘤特异性T细胞反应,这对样本采集构成挑战并可能增加副作用。因此,通过治疗剂增加肿瘤特异性抗原丰度和对癌细胞的免疫原性,并使用这些细胞膜作为抗原来源,将提供克服这些限制的机会,以促进个性化癌症疫苗的临床使用。研究之前通过将抗原肽与合成聚合物PC7A直接混合开发了一种激活STING的纳米疫苗,在多种肿瘤模型中引发了强大的抗肿瘤T细胞反应。除了促进肽递送和胞质释放外,PC7A还是一种多价STING激动剂,可作为激活先天免疫反应的强疫苗佐剂。PC7A在大鼠和食蟹猴中提出了最佳安全性评价,目前正在进行实体癌治疗的I期临床试验(NCT06022029)。
在这项研究中进行了高通量分析,揭示了IFN-γ是不同癌细胞类型抗原呈递的有效刺激剂。抗原富集细胞膜包被的PC7A纳米疫苗(AECM@PC7A)诱导了强大的多表位T细胞应答,在多种小鼠癌症模型和人源化异种移植模型中产生了强大的抗肿瘤效果,为简单有效地设计个性化癌症疫苗提供了一个通用平台。
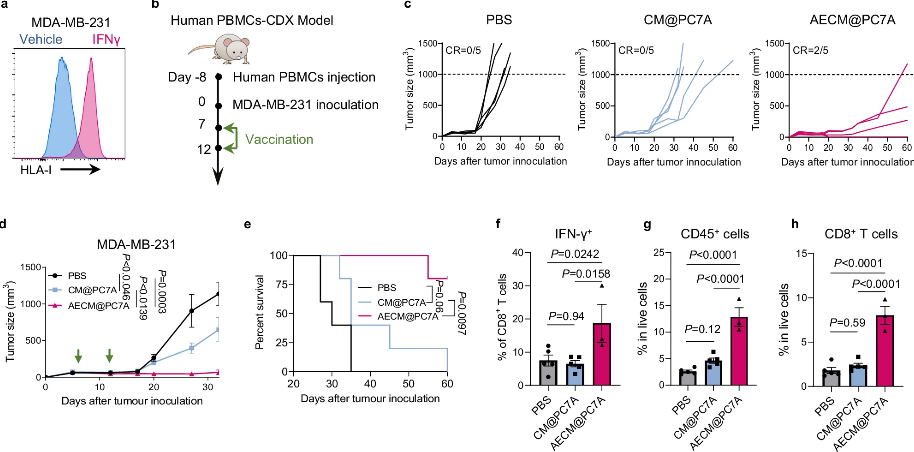
图1AECM@PC7A在人源化CDX模型中的抗肿瘤作用(摘自Nature Communications)
参考消息:
https://doi.org/10.1038/s41467-025-59977-8
猜你喜欢
- 温牛奶柚子柠檬 9种食物吃走口腔异味
- 【指南与共识】| 根治性前列腺切除术围手术期整合康复中国专家共识(2024年版)
- AI来帮忙 检车开启“智慧春运”
- 毛孔粗大如何是好 五个妙招让你皮肤紧致有弹性
- Science:DNA上的“智能泊车系统”:揭秘INO80如何通过“自锁刹车”实现精准定位
- 萝卜丝炒虾皮的做法-家常味炒菜谱
- NEJM:手术前后加用派姆单抗可显著提高早期三阴性乳腺癌的生存率
- World J Urol:中国学者揭示达罗他胺联合雄激素剥夺疗法作为局部晚期前列腺癌新辅助治疗的突破性进展
- 女生体味重怎么办,如何使体味变香
- 北京协和医院呼吸与危重症医学科新冠肺炎诊疗参考方案(2022年12月版)发布
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)