首页 > 医疗资讯/ 正文
幼儿龋齿(ECC)表现出牙齿特异性,突出了单个牙齿水平预防的需要。
2025年5月30日,香港大学黄适、中国科学院青岛生物能源与生物过程技术研究所徐健、青岛大学滕飞共同通讯在Cell Host & Microbe在线发表题为“Single-tooth resolved, whole-mouth prediction of early childhood caries via spatiotemporal variations of plaque microbiota”的研究论文,该研究发现通过菌斑微生物群的时空变化对早期儿童龋齿进行单齿分辨、全口预测。
该研究对来自两个队列的89名学龄前儿童的2,504个牙菌斑微生物群样本进行了分析,在超过11个月的时间里,以单颗牙齿的分辨率跟踪成分变化和估算的功能趋势。在健康儿童中,牙齿微生物群在上颌牙齿上表现出从前到后的生态梯度和强烈的双侧对称性。由于龋齿引起的微生物重组,这些模式在患龋儿童中被破坏。利用牙齿特异性疾病相关分类群和空间相关临床/微生物特征,使用机器学习技术开发了龋齿的空间微生物指标(空间MiC或sMiC)。sMiC在单颗牙齿分辨率下诊断ECC的准确率达到98%,在感知健康的牙齿中提前2个月预测新龋齿的准确率达到93%。这种高分辨率的ECC发育时空微生物图谱在单颗牙齿水平上解开了微生物病因学,确定了每颗牙齿的特征性微生物特征,并为牙齿特异性ECC预防策略提供了基础。

牙齿是最坚硬的器官,但它们远不是最耐用的。龋齿是一种由牙齿微生物群的慢性活动引起的慢性身体腐烂和损伤,长期以来一直是所有年龄组的全球健康和经济负担。特别是,幼儿龋齿(ECC)被定义为6岁以下儿童的任何乳牙中“存在一个或多个腐烂(非空洞或空洞病变)、缺失(由于龋齿)或填充的牙齿表面”。在中国尤其普遍, 影响超过70%的5岁儿童。作为最常见的慢性疾病,ECC会导致疼痛、感染、营养摄入受损和睡眠障碍,严重影响生活质量,并可能阻碍认知发展和学习成绩。遗憾的是,一旦开始,对牙齿的损害通常是不可逆的,年轻患者在其一生中继续遭受新损害甚至牙齿脱落的更高风险。因此,ECC的早期诊断、预后和预防性干预尤为重要。
在ECC中,环境扰动改变了口腔微生物群的平衡,最终导致致龋细菌占优势,导致牙齿组织持续脱矿。该过程具有固有的部位特异性。乳牙列由位于四个象限的20颗牙齿组成,呈现一系列基底,包括前牙、前臼齿和臼齿。这些基质独特的化学性质、形貌、解剖结构和稳定性为微生物群落提供了牙齿特有的栖息地。此外,不同的牙齿和不同的牙齿表面对ECC表现出不同的敏感性。例如,儿童的上颌前牙和臼齿比其他牙齿具有更高的龋齿发病风险。事实上,每颗牙齿都可以按照自己的轨迹走向不同的结果:健康的牙齿可能保持稳定或转变为龋齿状态,而患病的牙齿可能稳定或恶化为严重的龋齿。最后,虽然健康牙齿和龋齿在口腔中共存,但只有后者是治疗的焦点。因此,牙齿生长、健康结果和疾病治疗的部位特异性需要对这些微生物介导的过程有“牙齿特异性”的理解。然而,对于健康儿童和患龋儿童,单个牙齿水平的口腔微生物群的时空异质性仍然未知。
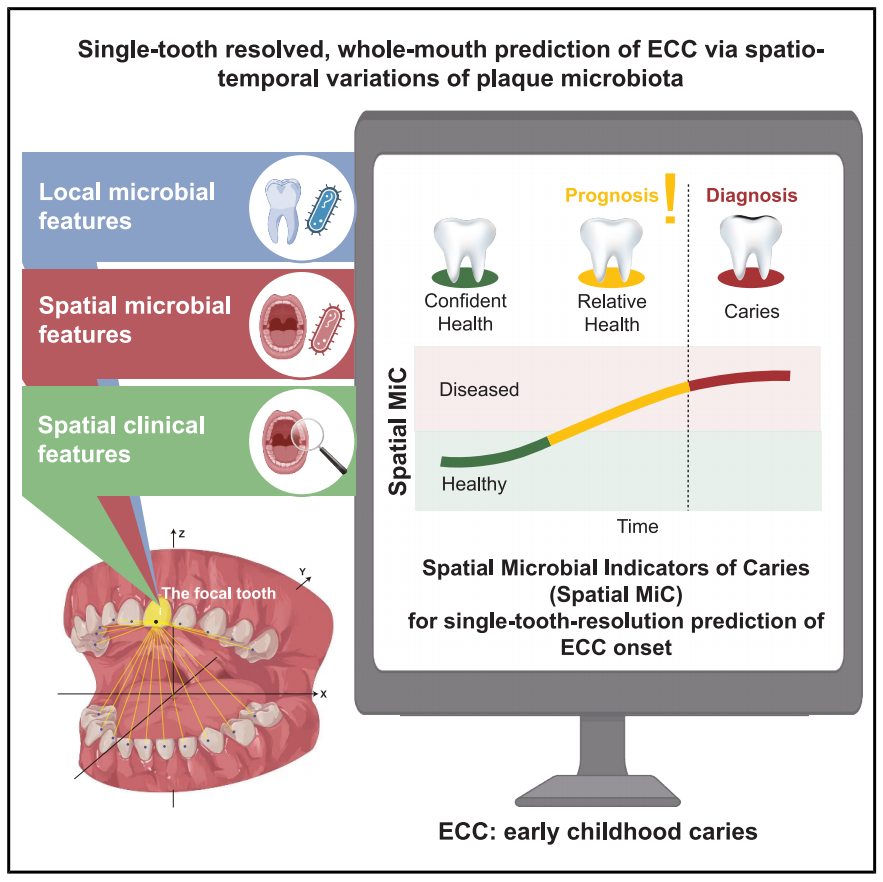
机理模式图(图源自Cell Host & Microbe)
先前的研究阐明了成人口腔微生物群的空间和时间动态。在空间维度,许多研究集中于不同口腔内生境的微生物特化和个体牙齿上微生物的微米级梯度。例如,Proctor等人使用带有地理坐标的明确空间建模来识别健康成人的前-后微生物梯度。相比之下,干燥综合征患者的口腔细菌空间梯度因唾液流量受损而减弱,而非龋齿。然而,儿童的单齿微生物群空间特征,尤其是在乳牙期,仍未得到充分描述。此外,在了解微生物群的空间异质性如何与ECC发生和发展的牙齿特异性联系方面,仍然存在关键差距。此外,仍不清楚微生物群如何在各种儿科牙齿生态位中相互作用,更重要的是,这种生态串扰是否驱动了局部ECC发病机制。因此,单颗牙齿分辨率的微生物群时空图对于解读健康儿童和患龋儿童的ECC生态学至关重要。
该研究进行了一项为期11个月的纵向研究,对来自89名4岁学龄前儿童的2,504份牙菌斑样本进行了16S rRNA基因测序,并辅以24份匹配样本的全宏基因组鸟枪法测序进行功能验证。该研究健康儿童和ECC儿童建立一个全口腔、单齿分辨率的微生物群发育模型。在单个儿童中,牙齿可能保持健康,转变成致龋状态,或者经历现有龋齿的恶化。追踪牙齿微生物群发育的高时空分辨率揭示了健康儿童和ECC儿童高度不同的区域特征。这些特征不仅是为了区分健康牙齿生长和龋齿形成,也是为了促进全面的、全口腔的、单颗牙齿特异性的ECC预后。这项工作为理解口腔微生物群和ECC发展之间的复杂相互作用建立了一个框架。未来的研究应侧重于在更大的队列中验证这些发现,并探索在儿科牙科护理中微生物靶向干预的潜力。通过将重点从被动治疗转移到主动预防,可以显著减轻ECC的负担,并改善儿童的口腔健康状况。
参考信息:
https://www.cell.com/cell-host-microbe/fulltext/S1931-3128(25)00185-4
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)