首页 > 医疗资讯/ 正文
急性肾损伤(AKI)损害肾近端肾小管细胞的能量代谢和抗氧化能力。
2025年6月3日,北京大学谢海燕、南开大学庞代文共同通讯在Nature Biomedical Engineering在线发表题为“NAD+ biosynthesis and mitochondrial repair in acute kidney injury via ultrasound-responsive thylakoid-integrating liposomes”的研究论文,该研究表明,整合类囊体片段并包封l-抗坏血酸的超声响应脂质体可以恢复AKI动物模型中肾小管细胞的能量供应和抗氧化能力以及肾功能。
静脉注射后,脂质体优先积聚在受损的肾脏中,并被近端肾小管细胞内化。在类囊体中表达的喹啉酸磷酸核糖基转移酶催化烟酰胺腺嘌呤二核苷酸(NAD+)的生物合成,促进受损线粒体的恢复。局部超声刺激激活抗坏血酸的电子转移,导致NADH的细胞质形成,并通过苹果酸-天冬氨酸穿梭恢复三磷酸腺苷。同时,增强的戊糖磷酸途径促进了NADPH的生物合成,降低了活性氧的水平。在患有急性肾损伤的小鼠和仔猪中,低剂量的脂质体可以防止肾脏损伤。

急性肾损伤(AKI)以肾功能迅速下降为特征,是发病率和死亡率增加的最常见疾病之一,但到目前为止还没有有效的治疗方法。肾近端肾小管细胞(PTCs)的存活率在很大程度上依赖于能量代谢和抗氧化反应。PTCs中的线粒体在AKI的早期阶段受到严重损伤,导致PTCs中的一系列生化活动受到干扰。特别是,三羧酸(TCA)循环明显受损,因此ATP的产生明显受阻,AKI进一步加重。同时,糖酵解途径大大增强,而戊糖磷酸途径(PPP)在AKI PTCs中受到严重抑制,导致活性氧(ROS)的过度产生和二氢烟酰胺腺嘌呤二核苷酸磷酸(NADPH)的减少,NADPH在细胞的抗氧化防御中起着关键作用。因此,AKI PTCs中积累了丰富的ROS,促进了AKI向慢性肾病(CKD)的发展。最近,已经开发了一些策略,特别是基于纳米粒子的系统,通过直接消耗ROS来治疗AKI。然而,这些方法不能从根本上预防急性肾损伤,因为ATP的提供和ROS的产生都没有得到根本克服。
烟酰胺腺嘌呤二核苷酸(NAD+)可以通过激活PGC1α来恢复受损的线粒体,并将来自能量源的电子传递到电子传递链以产生ATP。此外,NAD+是NADPH生成的前体。然而,在AKI的早期阶段,NAD+的消耗加速。此外,由于喹啉酸磷酸核糖基转移酶(QPRT)的表达明显减弱,其生物合成减少,QPRT是连接从头合成NAD+的初始步骤和最终步骤的必需酶。因此,提高PTCs中的NAD+水平对于AKI治疗至关重要
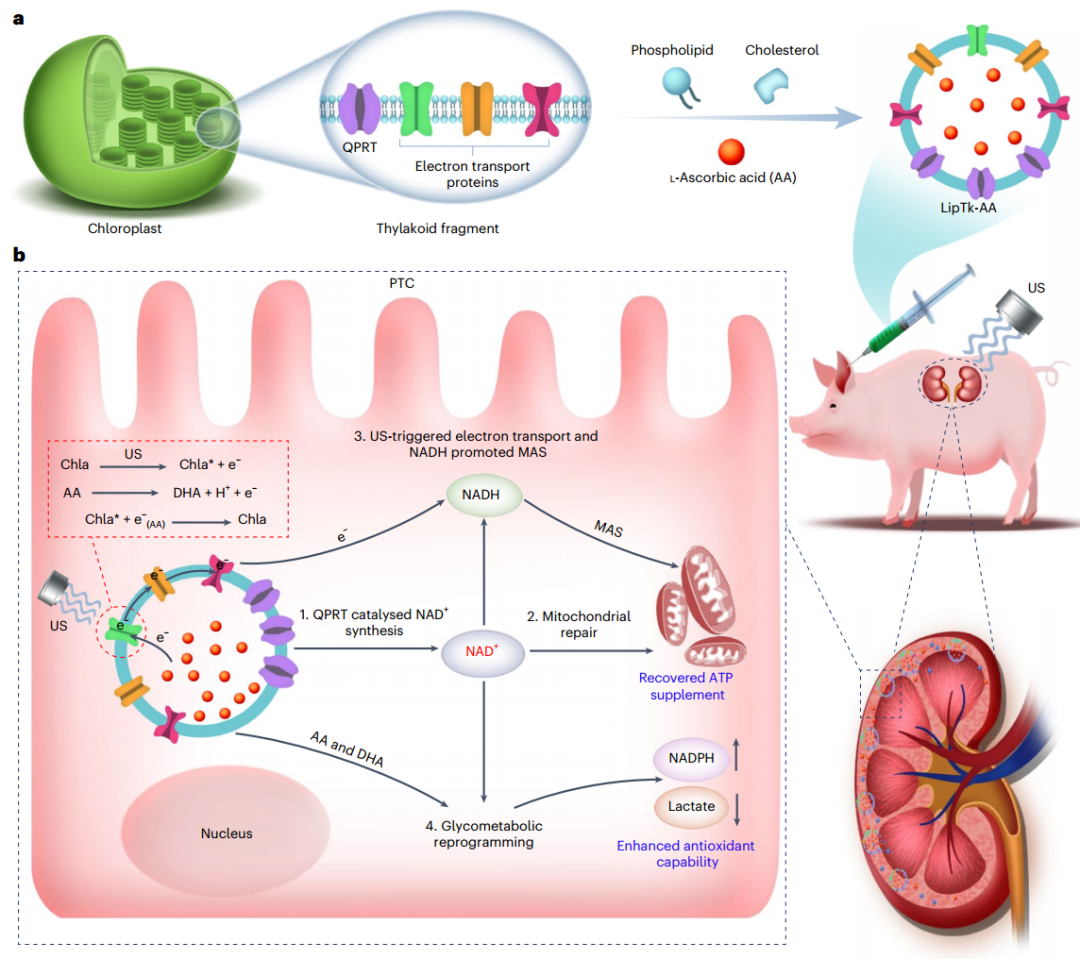
超声LipTk-AA治疗急性肾损伤(图源自Nature Biomedical Engineering)
该研究通过将类囊体片段(Tk)与纳米脂质体(Lip)整合并将l-抗坏血酸(AA)加载到蛋白脂质囊泡(LipTk)中,构建了用于高效AKI治疗的机械纳米囊泡。由此产生的仿生LipTk AA含有QPRT和从Tk转移的完整电子传递链。全身给药后,纳米级LipTk AA可以有效地积聚在AKI肾脏中,随后由于AKI肾脏肾小球滤过屏障的通透性增强,可以穿透肾细胞。然后,QPRT催化从头开始的NAD+生物合成,促进受损线粒体的快速恢复。此外,LipTk-AA中的电子转移可以在超声刺激(US)下通过利用AA作为电子供体和NAD+作为电子受体来启动。因此,NADPH在NAD+存在下产生,而ROS含量降低。同时恢复的ATP补充和增强的抗氧化能力可以防止AKI在早期的发展以及AKI向CKD的转变。利用US的深层组织穿透能力,不仅在五种小鼠急性肾损伤模型中,而且在仔猪急性肾损伤模式中都取得了显著的治疗效果。
该研究创新性地将植物类囊体的电子传递机制引入医学纳米系统,结合抗坏血酸与超声激活,实现了NAD+的重建、线粒体修复和代谢重编程,显著改善了AKI模型中的肾功能损伤。该系统在小鼠与猪模型中均展示出卓越疗效,展示了向临床转化的巨大潜力。
参考信息:
https://www.nature.com/articles/s41551-025-01402-y#Sec33
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)