首页 > 医疗资讯/ 正文
心肌肥大是导致心力衰竭的重要病理变化。最近的研究表明,线粒体相关内质网膜(MAM)在这一病理过程中起着关键作用。然而,分子机制尚不清楚。
2025年6月9日,浙江大学胡新央、Zhu Wei共同通讯在Circulation在线发表题为“FMO2 Prevents Pathological Cardiac Hypertrophy by Maintaining the ER-Mitochondria Association Through Interaction With IP3R2-Grp75-VDAC1”的研究论文,该研究表明FMO2通过与IP3R2-Grp75-VDAC1相互作用维持ER线粒体关联,从而预防病理性心肌肥大。
在这里,研究人员检测到MAM结构中一个意想不到的成分,即FMO2,一种内质网驻留蛋白。病理性心肌肥大期间,FMO2水平降低。FMO2的缺失和过表达分别会恶化或阻止体内病理性心力衰竭的进展。进一步证明,FMO2定位于MAM结构,在那里它与肌醇1,4,5-三磷酸2型受体(IP3R2)结合,作为IP3R2-Grp75(葡萄糖调节蛋白75)-VDAC1(电压依赖性阴离子通道蛋白1)复合物的一个组成部分,维持内质网-线粒体接触,并调节线粒体Ca2+信号传导,用于生物能量学。研究发现,一种增强内质网-线粒体接触的合成肽促进了Ca2+的转移,并预防了病理性心肌肥大。该研究结果揭示了FMO2在心肌肥大中的关键作用,FMO2在维持MAM结构和功能方面起着关键作用,这可能代表了心肌肥大和心力衰竭的新机制和治疗靶点。
 心力衰竭作为各种心血管疾病的终末期,已被公认为全球死亡率和发病率的主要原因,这引发了人们对该研究领域的极大兴趣。从适应性心肌肥厚到不适应性心肌肥厚的转变与心力衰竭的进展密切相关,是心脏死亡的独立危险因素。尽管人们对不适应性心肌肥大的研究做出了巨大努力,但心肌肥大的潜在机制尚未完全了解。
心力衰竭作为各种心血管疾病的终末期,已被公认为全球死亡率和发病率的主要原因,这引发了人们对该研究领域的极大兴趣。从适应性心肌肥厚到不适应性心肌肥厚的转变与心力衰竭的进展密切相关,是心脏死亡的独立危险因素。尽管人们对不适应性心肌肥大的研究做出了巨大努力,但心肌肥大的潜在机制尚未完全了解。
最近的研究强调了细胞器相互作用在维持细胞稳态和调节各种病理过程中的关键作用,包括病理性心肌肥大。内质网(ER)似乎是细胞器交叉相互作用中最活跃的参与者,特别是与线粒体的相互作用,这已成为细胞生物学领域的一个热门话题。线粒体相关ER膜(MAM)是由特定的束缚和间隔蛋白形成的动态微区,在Ca2+信号传导、脂质转运和代谢中起着至关重要的作用。MAM在从适应性心肌肥大向不适应性心肌肥大的过渡过程中发生了变化,导致心力衰竭进展。然而,MAM的结构和功能如何受到调节并导致心力衰竭的进展(即病理性心肌肥大)尚未完全阐明。
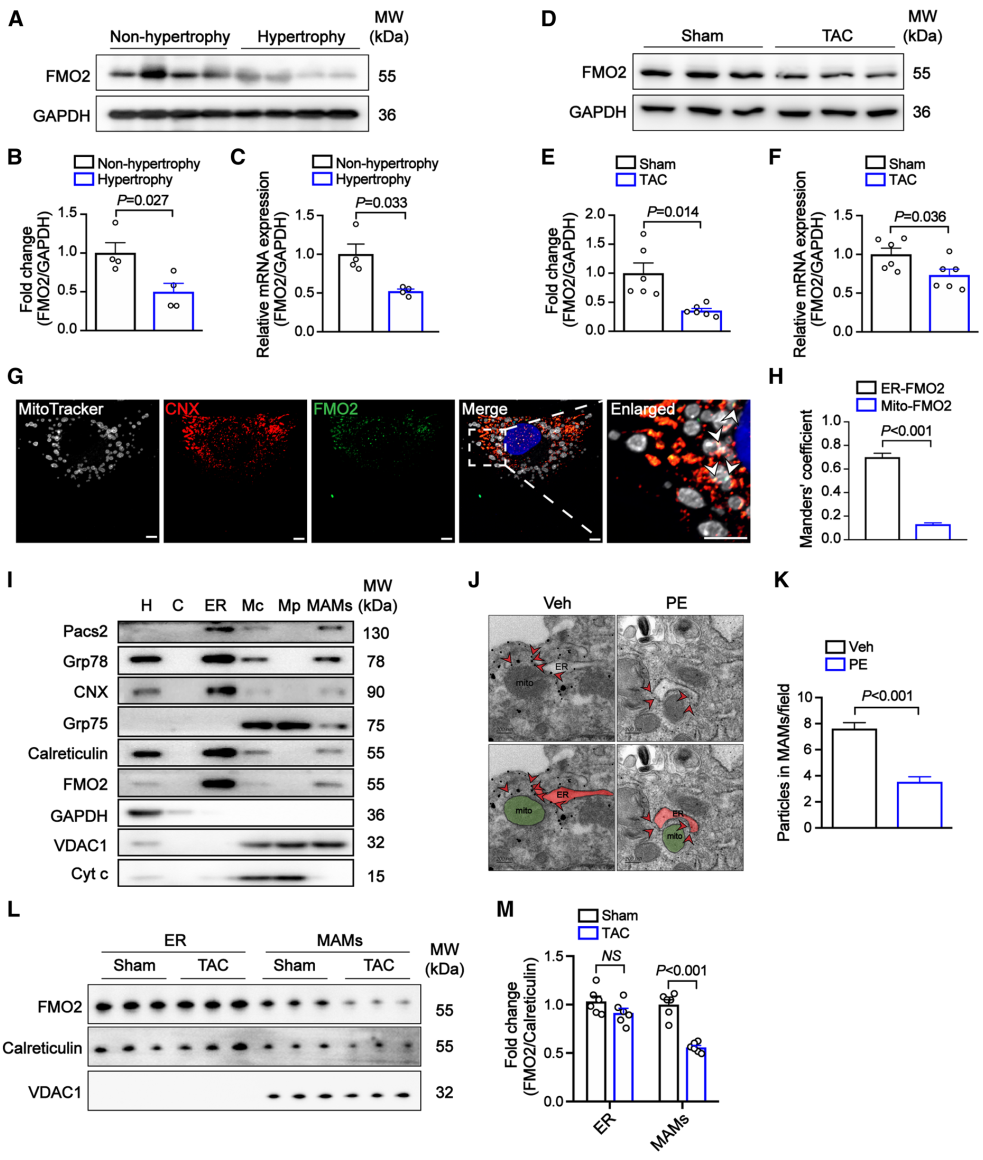
FMO2定位于MAM,在肥大的心脏中其表达减少(图源自Circulation)
有趣的是,最近的研究表明,在MAM复合物中也检测到FMO(含黄素单加氧酶)家族蛋白。FMO蛋白是一组微粒体酶,其跨膜结构域主要与ER结合。FMO2是心脏中的主要亚型,已被证明在长寿和病理纤维化中发挥作用,但其在MAM中的作用尚未得到探索。
在这项研究中,对人类肥大心脏组织的大量RNA测序分析和小鼠肥大心脏组织中MAM靶向蛋白质组学都揭示了MAM中FMO2表达的改变。进一步的实验表明,FMO2与肌醇1,4,5-三磷酸2型受体(IP3R2)结合,参与形成IP3R2/葡萄糖调节蛋白75(Grp75)/电压依赖性阴离子通道蛋白1(VDAC1)复合物,这是MAM的关键结构成分。FMO2表达的变化通过改变MAM的形成来影响ER向线粒体释放Ca2+,从而主要通过调节线粒体Ca2+水平来干扰线粒体生物能量学。因此,FMO2在心肌肥大的发病机制中起着至关重要的作用,其过表达可以预防适应不良的心肌肥大。值得注意的是,通过合成连接肽连接ER和线粒体可以增加线粒体内的Ca2+水平,并防止病理性心肌肥大的进展。总的来说,该研究不仅发现了MAMs复合物的一个新成分,还为病理性心肌肥大提供了一个新的治疗靶点。
参考信息:https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.124.072661
- 上一篇: 河北关于公示公布部分药品挂网的通知
- 下一篇:穿刺肱动脉行介入治疗的操作技巧
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)