首页 > 医疗资讯/ 正文
近年来,嵌合抗原受体(CAR)T细胞疗法在血液系统恶性肿瘤治疗中取得了突破性进展,成为复发/难治性B细胞淋巴瘤、白血病和多发性骨髓瘤的重要治疗手段。然而,伴随其强大的抗肿瘤活性而来的是一系列独特的免疫相关毒性,其中神经毒性尤为突出,严重影响治疗的安全性和患者生存质量。
目前,CAR T细胞相关的神经毒性主要包括三大类:免疫效应细胞相关神经毒性综合征(ICANS)、肿瘤炎症相关神经毒性(TIAN)以及BCMA靶向治疗后的迟发性神经并发症。ICANS是最常见的急性神经毒性,表现为从轻度认知障碍到致命性脑水肿的广泛症状;TIAN则特发于中枢神经系统肿瘤患者,由局部免疫炎症反应引发;而针对B细胞成熟抗原(BCMA)的CAR T细胞疗法则可能诱发帕金森样综合征和颅神经病变等独特并发症。
尽管糖皮质激素和细胞因子抑制剂(如IL-1/IL-6拮抗剂)已成为当前管理的主要手段,但部分难治性病例仍缺乏有效干预措施。此外,神经毒性的病理机制尚未完全阐明,涉及系统性细胞因子风暴、血脑屏障破坏、神经胶质细胞激活及靶抗原在健康神经组织的脱靶效应等多重因素。因此,深入探索神经毒性的分子机制、优化风险预测模型,并开发新型CAR设计(如可调控“安全开关”)是未来研究的重点方向。
2025年6月25日,哈佛医学院的Jörg Dietrich(通讯作者)和Philipp Karschnia(第一作者)在《Nature Reviews Neurology》期刊上发表了一篇题为:Neurological complications of CAR T cell therapy for cancers的综述文章,系统总结了CAR-T细胞治疗相关神经毒性的类型、临床表现、潜在机制及管理策略,涵盖了免疫效应细胞相关神经毒性综合征(ICANS)、肿瘤炎症相关神经毒性(TIAN)以及靶向BCMA治疗后的迟发性神经并发症等多种表现形式。文章强调了这些神经毒性对疗效和患者生活质量的影响,并介绍了当前的对症治疗和免疫调节手段,同时展望了通过机制研究推动CAR-T细胞设计优化和治疗策略创新,以提高治疗安全性的前景。

免疫效应细胞相关神经毒性综合征(ICANS)
ICANS是CAR T细胞疗法最常见的急性神经毒性反应,发生率高达70%,通常在输注后10天内出现。其临床表现包括注意力障碍、定向力下降、语言障碍(如表达性失语)、癫痫发作,严重时可进展为脑水肿甚至昏迷。病理机制涉及系统性炎症反应(如IL-6、IL-1β升高)、血脑屏障破坏及神经胶质细胞激活。研究表明,CD28共刺激域的CAR T细胞比4-1BB共刺激域产品更易引发严重ICANS。诊断主要依据ASTCT共识分级标准(ICE评分),治疗以糖皮质激素(如地塞米松)和IL-1受体拮抗剂(阿那白滞素)为主,多数患者可在数周内恢复,但约5%的病例可能致命。
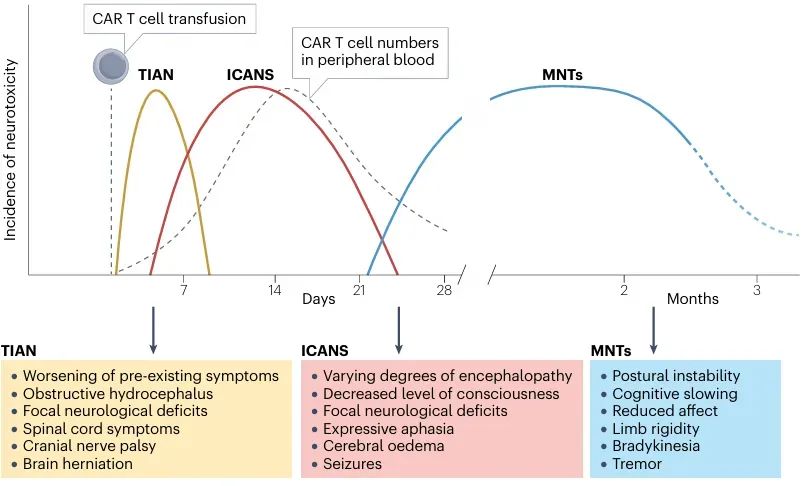
图 1:嵌合抗原受体 (CAR) T 细胞介导的神经毒性发作的相对时间尺度。

表1 | ASTCT关于ICANS的分级共识标准
肿瘤炎症相关神经毒性(TIAN)
TIAN是CAR T细胞治疗中枢神经系统(CNS)肿瘤时特有的局部神经毒性,分为两种亚型:
TIAN 1型:由肿瘤周围炎症性水肿引起,表现为占位效应(如脑疝、梗阻性脑积水)。
TIAN 2型:由局部电生理功能障碍导致,表现为原有神经症状恶化(如运动或感觉障碍)。
其机制与CAR T细胞穿透血脑屏障后引发局部免疫反应相关,影像学可见肿瘤周围T2-FLAIR高信号。治疗需结合高剂量糖皮质激素、IL-1拮抗剂(如阿那白滞素)及必要时脑脊液引流(如脑室外引流术)。目前,TIAN的预后较ICANS更复杂,部分患者可能长期遗留神经功能缺损。
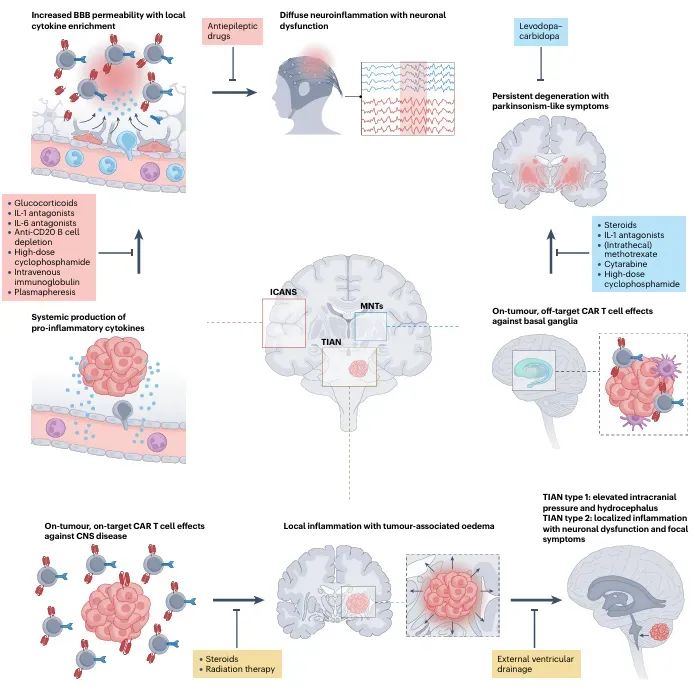
图 2:嵌合抗原受体 (CAR) T 细胞介导的神经毒性的潜在病理机制和治疗方法。
BCMA靶向CAR T细胞疗法的神经毒性
靶向B细胞成熟抗原(BCMA)的CAR T细胞(如西达基奥仑赛)可导致独特的迟发性神经毒性,主要包括:
帕金森样综合征(运动迟缓、肌强直、震颤),可能与CAR T细胞对基底神经节的交叉反应有关,MRI可见基底节区T2高信号或FDG-PET代谢减低。
颅神经病变(如面神经麻痹),通常在输注后3周出现,多数可逆,但帕金森样症状常不可逆,对左旋多巴反应不佳。
目前认为,这些毒性可能与CAR T细胞的长期持续性相关,部分病例可通过强化免疫抑制(如环磷酰胺)缓解症状,但最佳治疗方案仍需探索。
其他罕见神经系统毒性
除ICANS和TIAN外,CAR T细胞疗法还可能引起:脊髓炎或脊髓水肿(表现为肢体无力或感觉障碍);周围神经病变(如吉兰-巴雷样综合征);自主神经功能障碍(如体位性低血压)。
这些毒性机制尚不明确,可能涉及CAR T细胞直接浸润神经组织或细胞因子介导的间接损伤。由于病例稀少,治疗主要依赖经验性免疫调节(如静脉免疫球蛋白、糖皮质激素)。
风险因素与自然病程
ICANS的高危因素包括:疾病相关(高肿瘤负荷、CNS受累);治疗相关(CD28共刺激域CAR、CRS严重程度);生物标志物(基线NfL升高、EASIX评分预测内皮损伤)。
自然病程方面,ICANS和TIAN通常可逆,而BCMA相关运动障碍可能持续进展,提示不同毒性的病理机制存在差异。
诊断策略
神经毒性的诊断需结合临床评估(ICE评分、神经系统查体);影像学(MRI显示脑水肿或基底节异常);实验室检查(CSF细胞因子分析、血清NfL);电生理监测(EEG评估脑病或癫痫样放电)。需注意排除感染、代谢性脑病或肿瘤进展等鉴别诊断。
治疗进展与挑战
目前的管理策略包括:
一线治疗:糖皮质激素(如地塞米松)、IL-1/IL-6抑制剂(阿那白滞素、司妥昔单抗)。
难治性病例:B细胞清除(如利妥昔单抗)、血浆置换或鞘内化疗。
预防措施:临床试验探索阿那白滞素或他汀类药物的预防价值。
新型CAR设计(如“自杀开关”、可控细胞因子分泌)有望降低神经毒性,但仍需临床验证。

表2 | 治疗或预防嵌合抗原受体(CAR)T细胞疗法神经系统并发症的在研药物临床试验
结论与未来展望
尽管CAR T细胞疗法的神经毒性机制逐渐明晰,但针对迟发性或罕见毒性的管理仍缺乏标准方案。未来研究方向包括:优化风险预测模型(如结合多组学数据);开发神经保护策略(如靶向微胶质细胞激活);改进CAR设计(如组织特异性靶向、可调控活性)。
通过多学科协作和前瞻性临床试验,有望在提高疗效的同时最小化神经毒性风险,推动CAR T细胞疗法的更安全应用。
原文链接:
https://doi.org/10.1038/s41582-025-01112-8
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)