首页 > 医疗资讯/ 正文
将多发性骨髓瘤与B细胞淋巴瘤区分开来可能有一定诊断难度,它们在形态学、免疫表型和临床表现上可能存在显著的重叠,
大多数浆细胞肿瘤在采样充分的情况下,其诊断过程通常能显示出清晰的形态学特征、经典的临床表现以及浆细胞的异常特征(例如,浆细胞标记物的表达、CD19的异常丢失、CD56的异常表达、细胞质轻链限制)。然而,一部分浆细胞肿瘤可能最初在骨髓外部位出现,表现出非典型的形态学和免疫表型,或者由于采样有限而无法进行进一步特征分析的辅助研究。在这些情况下,肿瘤性浆细胞可能与其他成熟B细胞肿瘤在临床和病理学上有显著的重叠。这种情况下可能就需要额外的分子遗传学辅助研究以及仔细的临床回顾,结合病史、实验室数据、形态学、免疫表型、细胞遗传学研究和分子测序分析,以便做出准确的诊断。
《Seminars in Diagnostic Pathology》近日发表综述,重点阐述了多发性骨髓瘤的鉴别诊断,特别是具有浆细胞分化特征的低级别B细胞淋巴瘤,以及具有浆母细胞形态的侵袭性B细胞淋巴瘤,这些淋巴瘤可能类似真正的浆细胞肿瘤。文中讨论了浆母细胞肿瘤的诊断方法,包括骨髓外浆母细胞浆细胞瘤,以及具有浆母细胞形态的B细胞淋巴瘤的鉴别特征。文中还涉及了具有浆细胞分化的低级别B细胞淋巴瘤,包括淋巴浆细胞淋巴瘤、边缘区淋巴瘤、慢性淋巴细胞白血病/小淋巴细胞淋巴瘤,以及其他较少表现出浆细胞分化的低级别B细胞淋巴瘤,如滤泡性淋巴瘤和套细胞淋巴瘤。文中还讨论了具有CCND1:IGH的多发性骨髓瘤,这种骨髓瘤类似低级别B细胞淋巴瘤,以及在治疗具有浆细胞分化的B细胞淋巴瘤后出现的浆细胞增殖。

浆母细胞淋巴瘤与浆母细胞骨髓瘤
浆细胞肿瘤(PCN)可累及骨骼和骨髓外组织,表现为克隆性浆细胞,作为浆细胞(多发性)骨髓瘤(MM)的一部分,或者在骨髓(BM)中没有MM的证据或由于PCN导致的终末器官损伤的孤立性病变。孤立性骨浆细胞瘤(SBP)主要发生在具有活跃造血功能的骨骼中,更常累及轴骨而非四肢骨。髓外浆细胞瘤(EMP)最常发生在上呼吸道(例如,鼻腔、副鼻窦、鼻咽、喉部),偶尔累及淋巴结、肺部、胃肠道和皮肤。EMP和偶尔的SBP可能表现出浆母细胞或间变性形态,具有大的核、开放的染色质、显著的核仁、高核质比和高增殖指数(图1A)。这种亚型被称为骨髓外浆母细胞/间变性浆细胞瘤(P-EMP),需要与浆母细胞淋巴瘤(PBL)进行鉴别诊断。
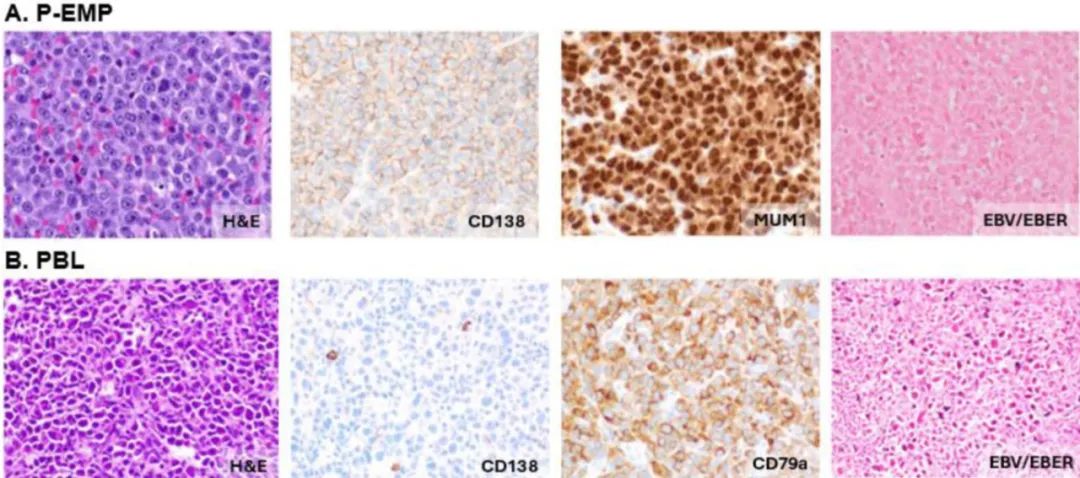
图1.浆母细胞骨髓外浆细胞瘤和浆母细胞淋巴瘤。
A.浆母细胞骨髓外浆细胞瘤,由中到大的浆细胞组成,具有浆母细胞形态学特征,包括高核质比(N:C)、偏心核、泡状染色质、显著的核仁和中等两性细胞质。这些浆母细胞CD138和MUM1阳性,EB病毒(EBER探针原位杂交)阴性。
B.浆母细胞淋巴瘤,由具有轻微多形性的浆母细胞组成,这些细胞CD138阴性,CD79a和EB病毒(EBER探针原位杂交)阳性。
浆母细胞淋巴瘤(PBL)是一种具有临床侵袭性的大细胞淋巴瘤,通常与免疫缺陷/失调相关(例如,HIV感染、骨髓干细胞和实体器官移植的免疫抑制治疗,或自身免疫性疾病)。EB病毒(EBV)再激活(以I型偶尔II型潜伏形式)参与淋巴瘤的发病机制。PBL通常发生在结外部位,如鼻腔/口腔和消化系统。其特征为大细胞的弥漫性增殖,具有浆母细胞或免疫母细胞形态,细胞形态多样,增殖指数高,表型上表现为终末分化的B细胞免疫表型(即浆细胞样免疫表型)。浆细胞样免疫表型包括B细胞标记物(CD19、CD20和PAX5)的减弱或缺失,以及浆细胞标记物CD138、CD38、MUM-1的表达,以及不同程度限制的κ或λ轻链表达(图1B)。PBL患者通常预后较差,即使接受积极化疗。
P-EMP与PBL的鉴别诊断非常重要,因为这两种疾病在临床和治疗上有很大的不同。然而,由于它们在形态学和免疫表型上有共同之处,鉴别诊断可能存在困难。表1总结了有助于区分P-EMP和PBL的关键特征。尽管它们在形态学和免疫表型上有共同之处,但的临床特征、EBV状态和遗传特征的重叠较少,可有助于鉴别诊断。
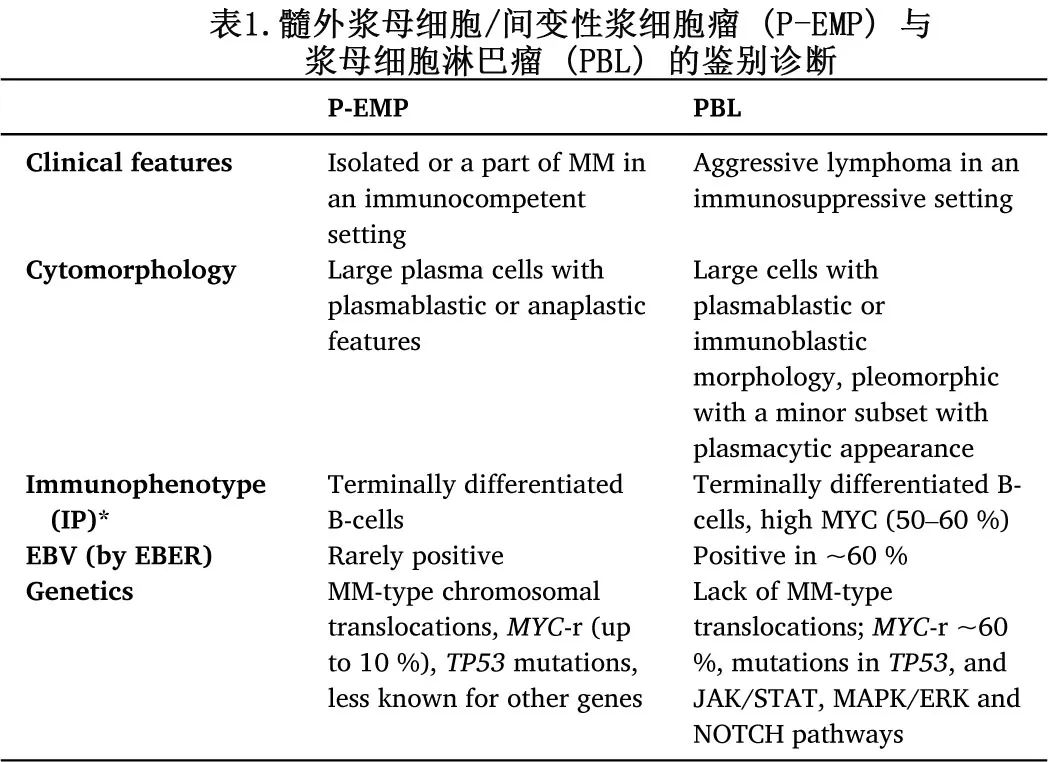
P-EMP通常发生在免疫功能正常的患者中,可能源自并发的浆细胞肿瘤,而PBL通常发生在免疫抑制的患者中,表现为新发(de novo)疾病。通过EBV编码的小RNA(EBER)定义的EBV阳性,在PBL中(约60%)比P-EMP中更常见(很少检测到,但最近一项研究报告EMP中阳性率为10%[60%为P-EMP];值得注意的是,SBP中EBV阳性率约为10%)更为常见。P-EMP和PBL均缺乏KSHV/HHV8和ALK的表达,这些特征有助于将它们与胸腔外/实体原发性渗出性淋巴瘤和ALK阳性大B细胞淋巴瘤区分开来。从遗传学角度来看,除了MYC重排外,MM中常见的主要染色体易位(MM型易位)在de novo PBL中尚未报道。MYC重排在PBL中较为常见,多常见于EBV阳性病例;约50%的PBL存在MYC重排,免疫组化显示高MYC表达,几乎所有报道的病例中都存在MYC::IGH融合。正如预期,P-EMP中存在主要的MM型易位,但MYC重排比PBL少见,最近一项研究报告MM中约10%存在MYC::IGH融合。在PBL中,经常检测到涉及JAK/STAT、MAPK/ERK和NOTCH通路的体细胞突变,以及TP53突变。EBV阴性PBL病例显示出更高的突变负荷,TP53、CARD11和MYC突变更为频繁,而EBV阳性PBL则倾向于更多地影响JAK/STAT通路的突变。相比之下,除了TP53突变外,P-EMP的基因突变谱尚不清楚,尽管激活RAS或NF-kB通路的突变,以及推动疾病前体阶段向MM发展的DIS3或FAM46C突变已有报道。总的来说,P-EMP和PBL的不同特征可能有助于通过对临床特征、EBV状态和遗传学的综合评估,在大多数患者中做出正确的诊断。
浆细胞肿瘤与低级别B细胞淋巴瘤
尽管大多数浆细胞肿瘤可以根据临床表现(例如,溶骨性病变、高钙血症、单克隆免疫球蛋白病等)、独特的形态学和免疫表型与B细胞淋巴瘤区分开来,但也有一些不常见的浆细胞肿瘤变体可能类似成熟B细胞淋巴瘤。除了形态学检查外,流式细胞术也是区分具有浆细胞分化的B细胞淋巴瘤(小到中等细胞大小,BCL-SM)与浆细胞肿瘤(PCN)的有用工具。识别具有CD19(+)、CD45(+)、CD56(-)免疫表型的浆细胞,以及克隆性B细胞群体,更符合BCL-SM的特点,而PCN浆细胞具有CD19(-)、CD45(-)、CD56(+)免疫表型(图2)。
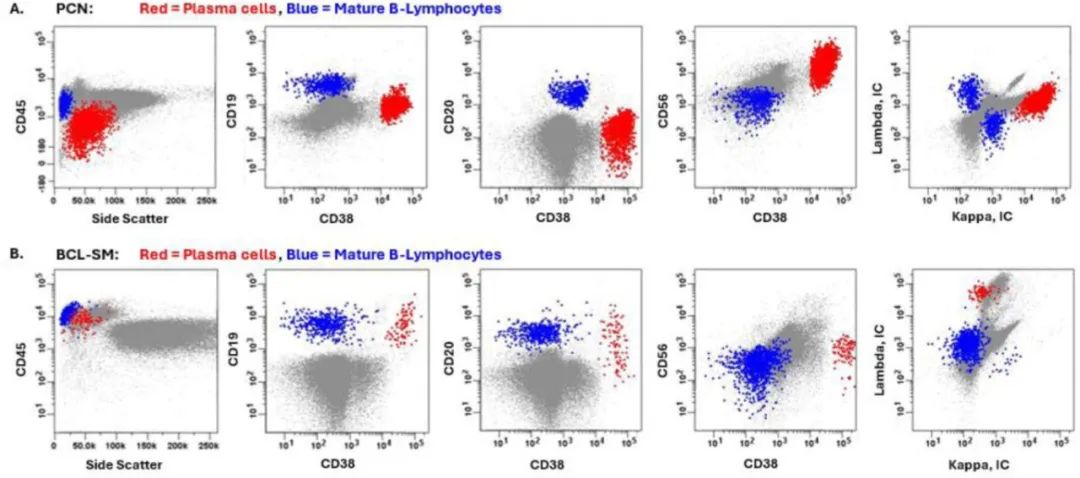
图2.浆细胞肿瘤和具有浆细胞分化的低级别B细胞淋巴瘤的流式细胞术图。
A.浆细胞肿瘤群体(红色)相对于背景反应性多克隆成熟B淋巴细胞(蓝色)显示出以下免疫表型:CD45(-)、CD19(-)、CD20(-)、CD38((bright+)、CD56(+)、细胞质内κ轻链(+)。
B.具有浆细胞分化的低级别B细胞淋巴瘤(如淋巴浆细胞淋巴瘤,LPL)显示出相关的异常成熟B淋巴细胞群体(蓝色)和浆细胞群体(红色)。成熟B淋巴细胞表现为:CD45(+)、CD19(+)、CD20(+)、CD38(-)、CD56(-)、细胞质内λ轻链(+)。浆细胞表现为:CD45(+)、CD19(+)、CD20(可变/dim+)、CD38(bright+)、CD56(-)、细胞质内λ轻链(bright+)。
多发性骨髓瘤的小细胞亚型(MMsc)占多发性骨髓瘤病例的不到5%,这种罕见的亚型以具有小淋巴细胞样形态的浆细胞为特征,类似于B细胞淋巴瘤(图3)。肿瘤性浆细胞通常表现出骨髓弥漫性间质浸润模式,其免疫表型为:CD19(-/dim+)、CD20(+)、CD38(bright+)、CD45(-)、CD56(-)、CD138(+)。CD20的频繁表达和CD56的较少表达可能会使基于免疫表型的细胞分类变得具有挑战性。大多数MMsc与由于t(11;14) CCND1::IGH导致的cyclin D1过表达有关,可能类似套细胞淋巴瘤,且有报道称B细胞基因(如CD20、PAX5和VPREB3)高表达。MMsc也可能存在涉及cyclin D3(CCND3)的遗传改变。缺乏CD56(神经细胞黏附分子,NCAM)是一种黏附分子,当其在肿瘤性浆细胞上缺失时,可能会减少细胞间相互作用,并增强外周血和骨髓外器官的受累,从而进一步模拟B细胞淋巴瘤。缺乏CD45表达、CD19表达弱至阴性、CD138阳性以及包括溶骨性病变在内的多发性骨髓瘤的临床表现,有助于做出正确诊断。
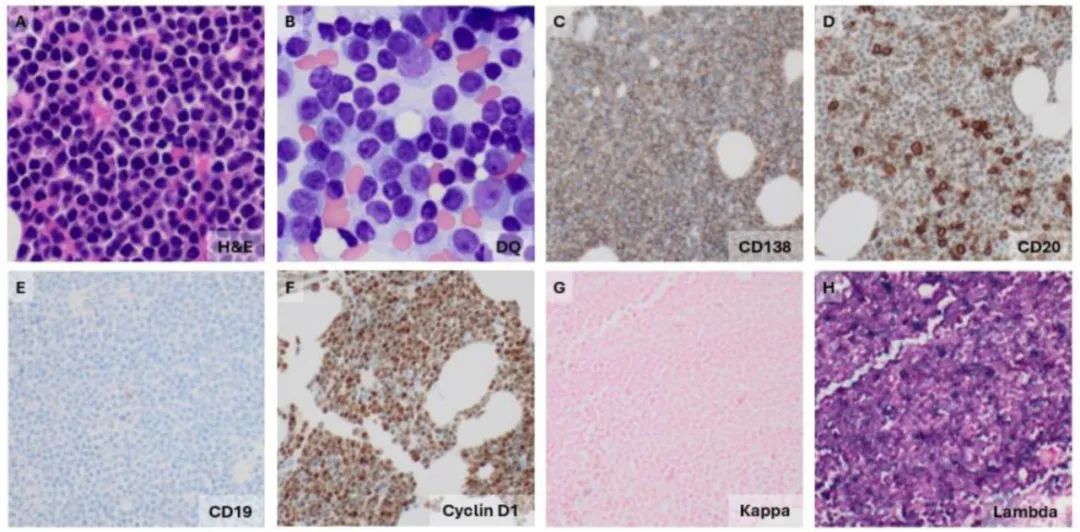
图3.浆细胞骨髓瘤,具有t(11;14) CCND1::IGH的小细胞变异型累及骨髓。
A-B.淋巴细胞样小浆细胞的弥漫性增殖,这些细胞具有偏心核、聚集的染色质以及少量至中等量的细胞质。
C. CD138弥漫性阳性。
D. CD20不同程度的阳性。
E. CD19阴性的浆细胞。
F. cyclin D1弥漫性阳性。
G. Kappa免疫球蛋白轻链阴性(原位杂交)。
H. Lambda免疫球蛋白轻链阳性(原位杂交)。
伴浆细胞分化的低级别B细胞淋巴瘤
浆细胞样/浆细胞分化是成熟低级别 B 细胞淋巴瘤亚组中已充分描述的特征,尤其是在淋巴浆细胞淋巴瘤 (LPL) 中,浆细胞分化是诊断要求,即边缘区淋巴瘤 (MZL) 和慢性淋巴细胞白血病/小淋巴细胞淋巴瘤 (CLL/SLL)。较少见的是,滤泡性淋巴瘤(FL)和套细胞淋巴瘤(MCL)也可能表现出浆细胞分化。B淋巴细胞分化为长寿浆细胞是一个由抗原介导的过程,源自生发中心的活化B细胞,而短寿浆细胞可以源自淋巴组织的滤泡外区域的幼稚B细胞。由于这些过程,生发中心后B细胞淋巴瘤更常表现出浆细胞分化。综合诊断方法有助于将这些疾病与多发性骨髓瘤区分开来。
淋巴浆细胞淋巴瘤
淋巴浆细胞淋巴瘤(LPL)是一种成熟B细胞淋巴瘤,在临床、形态学和免疫表型上与浆细胞肿瘤有较多重叠。根据定义,LPL是一种成熟B淋巴细胞的增殖,这些细胞表现出浆细胞分化的谱系。肿瘤细胞包括成熟B淋巴细胞、浆细胞样B淋巴细胞和成熟浆细胞。LPL病变可能以一种细胞类型为主,其中浆细胞的占优势时可能类似真正的浆细胞肿瘤。LPL的临床表现可能与多发性骨髓瘤相似,因为大多数患者会出现单克隆免疫球蛋白病,尽管大多数LPL副蛋白为IgM亚型(表2)。
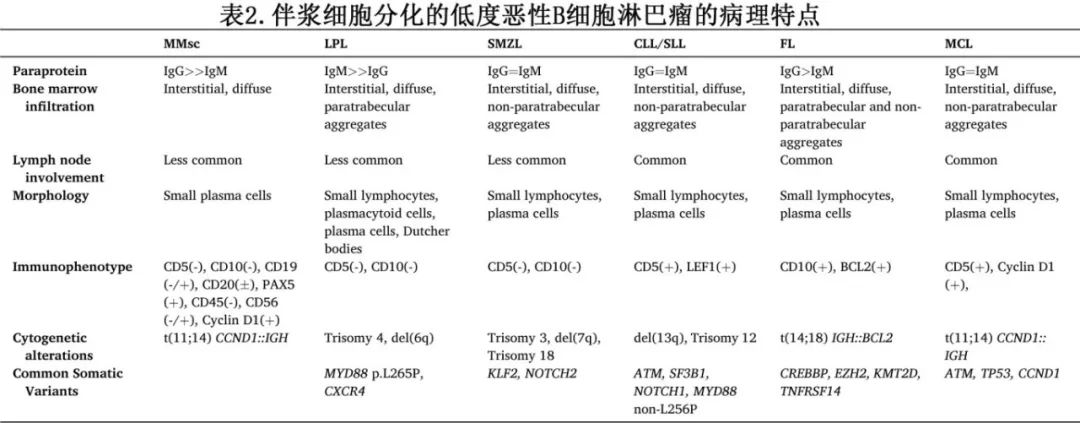
当存在 IgM 单克隆丙种球蛋白病和 LPL 累及骨髓时,就符合华氏巨球蛋白血症(WM)的临床诊断标准。大多数LPL患者(约90%)符合WM的标准。其余的LPL变体包括非IgM/非华氏变体,其中LPL可能产生其他单克隆免疫球蛋白亚型(例如,IgG、IgA),或者可能不产生副蛋白(非分泌性LPL)。值得注意的是,只有不到1%的浆细胞肿瘤产生IgM(表2)。IgM副蛋白血症也可能与高黏滞度、凝血病、溶血性贫血、冷球蛋白血症和周围神经病变有关。非Waldenstrom LPL更有可能在诊断时累及骨髓外部位,并且可能由于检测到非IgM单克隆免疫球蛋白病而类似多发性骨髓瘤,但LPL的形态学、免疫表型和分子遗传学发现与真正的浆细胞肿瘤是不同的。
病变细胞包括一系列成熟的较小B细胞、浆细胞样B细胞和成熟浆细胞(图4)。
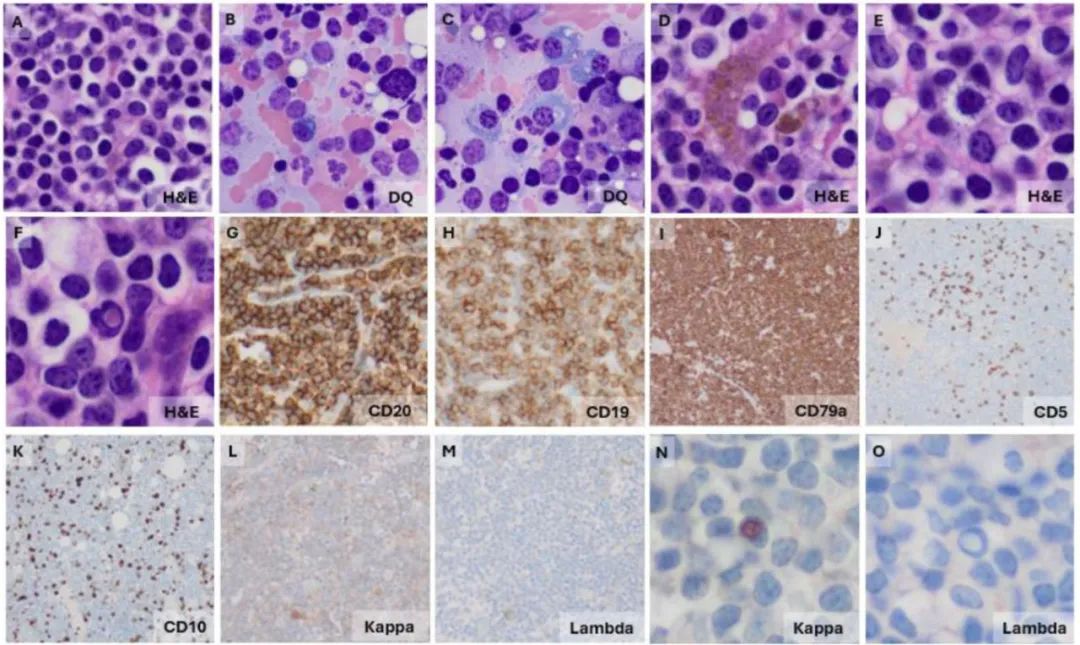
图4. 淋巴浆细胞淋巴瘤累及骨髓。
A. 骨髓活检核心显示小淋巴细胞和浆细胞样淋巴细胞的弥漫性增殖。 B. 骨髓抽吸物显示散在的成熟淋巴细胞、浆细胞样淋巴细胞(中央)和圆形肥大细胞(右侧)。 C. 骨髓抽吸物显示小淋巴细胞和成熟浆细胞(中央)。 D. 含有含铁血黄素的巨噬细胞(噬铁细胞)与淋巴浆细胞样细胞混杂。 E. 圆形肥大细胞与淋巴浆细胞样细胞混杂。 F. 嗜酸性粒细核内假包涵体(“Dutcher小体”)。 G. CD20阳性淋巴浆细胞样细胞。 H. CD19阳性淋巴浆细胞样细胞。 I. CD79a阳性淋巴浆细胞样细胞。 J. CD5阴性淋巴浆细胞样细胞。 K. CD10阴性淋巴浆细胞样细胞。 L. Kappa(免疫组化)阳性淋巴浆细胞样细胞。 M. Lambda(免疫组化)阴性淋巴浆细胞样细胞。 N. Kappa(免疫组化)阳性Dutcher小体。 O. Lambda(免疫组化)阴性Dutcher小体。
浆细胞样细胞的特征为成熟的B细胞和浆细胞的重叠形态,包括偏心核、圆形至轻度不规则的核轮廓、尚未完全类似于成熟浆细胞的“时钟面”染色质的聚集染色质、与成熟淋巴细胞的少量细胞质相比的中等量细胞质、在Romanowsky染色(例如,Diff Quik)上比成熟浆细胞染色更浅的轻度嗜碱性细胞质,以及缺乏明显的高尔基区。病变细胞的一个亚群可能含有核假包涵体,即“Dutcher小体”,当免疫球蛋白填充的细胞质内陷到核膜中时就会出现。在组织切片上,可以用免疫球蛋白轻链免疫组化进一步突出显示这些包涵体(图4)。
LPL在骨髓和组织中的浸润模式是多样的。骨髓是最常见的受累部位,LPL通常表现出间质性浸润模式,并形成旁小梁聚集,这在H&E染色上可能会类似滤泡性淋巴瘤,因为滤泡性淋巴瘤的骨髓受累通常与旁小梁聚集有关。这种模式可以帮助区分LPL与如脾边缘区淋巴瘤等类似物,后者在骨髓中与LPL具有相似的形态学和免疫表型,但更一致地形成非旁小梁的结节状聚集(表2)。
LPL病变的细胞环境已报道较多,但可能在不同患者样本中有所不同。淋巴样增殖通常与分散的、成熟的、圆形的肥大细胞有关,这些肥大细胞通过肥大细胞上的CD154(CD40配体)与LPL B淋巴细胞上的CD40之间的相互作用,促进B细胞的信号传导和增殖。也可能看到散在的含铁血黄素的巨噬细胞。这一系列形态学特征有助于区分LPL与多发性骨髓瘤。
病变细胞表现出非特异性的B细胞和浆细胞免疫表型,但应表现出免疫球蛋白轻链限制。大多数LPL细胞缺乏CD5和CD10的表达,尽管这些标志物在高达10-20%的LPL病例中可能存在,这可能会使区分这些病变与其他具有浆细胞分化的低级别B细胞淋巴瘤变得具有挑战性。成熟的B细胞成分应表达B细胞抗原CD19、CD20、PAX5和CD22。肿瘤性浆细胞成分应表达成熟的浆细胞标记物CD19、CD38、CD45、CD138、MUM1,并且通常缺乏异常的CD56表达(图2)。保留CD19和CD45的表达有助于区分LPL浆细胞与多发性骨髓瘤。浆细胞样B细胞通常表现出保留但减少的成熟B细胞抗原CD20、CD22、PAX5、CD19的表达,以及CD38和MUM1的可变表达。广泛的B系抗原CD19和CD79a有助于突出显示LPL细胞的谱系,包括肿瘤性浆细胞(图4)。
髓样分化因子88基因(MYD88)热点激活突变MYD88 p.L265P存在于约90%的LPL/WM中,是一个有用的诊断靶点,有助于区分LPL与其他BCLSM;也有助于区分LPL与通常缺乏MYD88 p.L265P的MM。在LPL中也报告了其他非L265P的MYD88突变。影响C-X-C趋化因子受体4基因(CXCR4)的失功能突变在27-36%的LPL中被检测到,在其他BCL-SM和浆细胞肿瘤中较少见,并且与对伊布替尼治疗的耐药性有关。
边缘区淋巴瘤
边缘区淋巴瘤(MZL)的亚型包括黏膜相关淋巴组织(MALT)的结外MZL、淋巴结MZL、脾MZL(SMZL)、原发性皮肤MZL和儿童结内MZL。本综述重点将放在与多发性骨髓瘤和其他具有浆细胞分化的低级别B细胞淋巴瘤在临床上有最多重叠的MALT淋巴瘤和脾MZL上。当存在明显的浆细胞成分时,具有浆细胞分化的结内边缘区淋巴瘤可能会类似累及淋巴结的多发性骨髓瘤,尽管真正的浆细胞肿瘤在初次发病时很少仅限于淋巴结,这应该促使人们进行评估以排除B细胞淋巴瘤。
与具有浆细胞分化的其他低级别B细胞淋巴瘤相比,脾MZL在形态学和免疫表型上与LPL最相似,可能在区分它与多发性骨髓瘤时表现出类似的诊断挑战。SMZL经常累及脾脏、骨髓、外周血和脾门淋巴结。在初次骨髓评估时,SMZL的显著浆细胞成分可能暗示浆细胞肿瘤的累及。然而,骨髓中支持SMZL而非真正的浆细胞肿瘤或LPL的形态学特征包括结节性间质淋巴样聚集体和窦内分布的淋巴样细胞的存在,这些在多发性骨髓瘤中是不常出现的,而旁小梁聚集体在LPL中更为常见。虽然并非完全特异,但少到没有的肥大细胞更倾向于支持MZL而非LPL。具有丰富的淡嗜酸性粒细质和单核细胞样形态(“单核细胞样淋巴细胞”)的小到中等大小的淋巴细胞有助于做出MZL诊断。据报道,SMZL中有20%至70%的病例出现浆细胞分化。SMZL中的肿瘤性B淋巴细胞具有一种非特异性的免疫表型,即CD19(+)、CD20(+)、CD79a(+)、CD5(-)、CD10(-)、CD23(-)、LEF(-)、Cyclin D1(-)、BCL2(+)和BCL6(-)。SMZL B细胞通常不表达CD43,并表达表面IgM和IgD。浆细胞成分预期将保留CD19和CD45的表达,但缺乏在多发性骨髓瘤中常见的CD56表达。SMZL中的KLF2和NOTCH2突变分别发生在约40%和6%至25%的病例中,在考虑浆细胞肿瘤和其他低级别B细胞淋巴瘤的鉴别诊断时,这些突变有助于诊断。
起源于胃肠道、唾液腺和肺部等结外部位的结外MZL(MALT)可能会表现出浆细胞分化,并可能显示出与浆细胞瘤和骨髓外多发性骨髓瘤的一些重叠特征,包括淀粉样蛋白A(AL-淀粉样蛋白)的产生(图5)。MALT淋巴瘤与慢性炎症状况有关,包括慢性感染(例如,胃部的幽门螺杆菌胃炎)和自身免疫(例如,唾液腺的干燥综合征)。当存在显著的浆细胞成分时,这些临床相关性有助于诊断具有挑战性的 MALT 淋巴瘤,尤其是在小的/有限的活检中。肿瘤性B淋巴细胞在形态学和免疫表型上与上述的其他边缘区淋巴瘤(包括SMZL)有重叠。与SMZL不同,高达约50%的MALT可能会出现CD43的异常表达,这有助于诊断,但在鉴别诊断时也给浆细胞肿瘤带来了诊断挑战,因为浆细胞也可以表达CD43。已在MALT淋巴瘤中描述了几种涉及MALT1(18q21)、BIRC3(11q21)、BCL10(1p22)和FOXP1(3p13)的染色体重排,这些重排有助于将MALT淋巴瘤与浆细胞肿瘤和其他淋巴瘤区分开来。
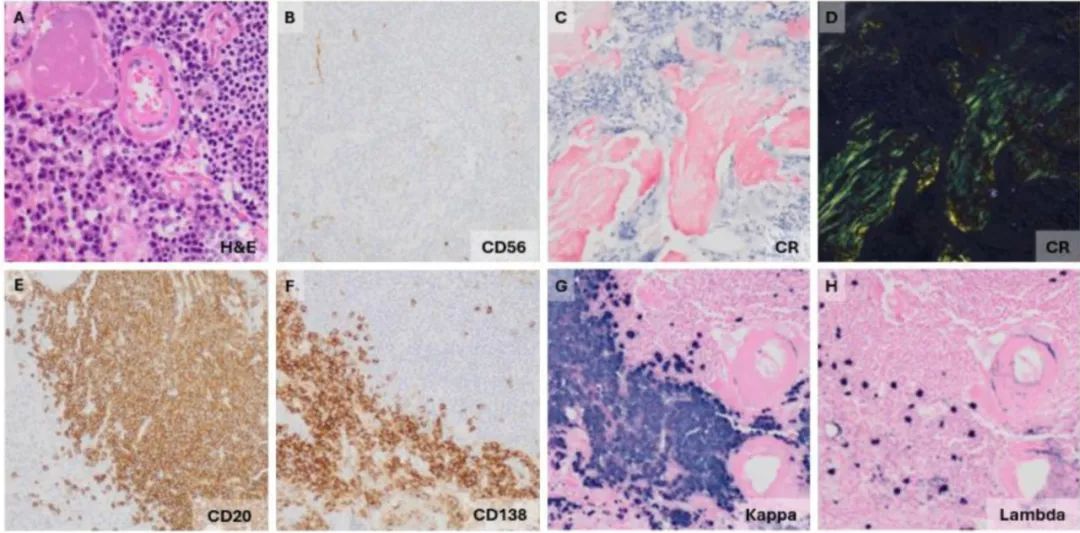
图5.黏膜相关淋巴组织(MALT)结外边缘区淋巴瘤累及肺组织。
A.小单核细胞样淋巴细胞,染色质聚集,细胞质呈中度淡嗜酸性(右上),成熟浆细胞(左下)和淀粉样物质(左上)。
B. CD56阴性淋巴细胞和浆细胞。
C.刚果红染色阳性的淀粉样物质。
D.在偏振光下呈现苹果绿色双折射的刚果红染色阳性淀粉样物质。
E. CD20阳性淋巴细胞(右上)和CD20阴性浆细胞(左下)。
F. CD138阴性淋巴细胞(右上)和CD138阳性浆细胞(左下)。
G-H. Kappa限制性(原位杂交)浆细胞。
慢性淋巴细胞白血病/小淋巴细胞淋巴瘤
慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)表现出浆细胞分化是一种被广泛认可的现象,尽管这种情况较为罕见且病因尚不明确。约15%的CLL/SLL会弱表达PRDM1/BLIMP1,这是一种在浆细胞和CLL/SLL免疫球蛋白分泌细胞中表达的B细胞分化关键调节因子。在大多数情况下,鉴别诊断主要涉及其他具有浆细胞分化的B细胞淋巴瘤,而非多发性骨髓瘤,尤其是在存在明显的淋巴细胞增多时。
异常的B细胞在大多数细胞中表现出CLL/SLL的形态学和免疫表型特征(图6),包括淋巴细胞形态、增殖中心形成、B细胞标记物CD20和PAX5的表达,以及CD5和LEF1的异常表达。浆细胞样群体表达CD5(±)、LEF1(±)、PAX5、MUM1,并与淋巴样群体共享轻链限制,表明存在克隆关系。浆细胞样细胞缺乏通常的浆细胞特征,例如CD138阳性,可能与CLL/SLL之前的伊布替尼和维奈克拉治疗有关。也可以看到成熟的克隆相关浆细胞成分,而没有显著的浆细胞样B细胞成分(图6和7)。有助于区分具有浆细胞分化的CLL/SLL与多发性骨髓瘤的关键特征,包括缺乏明显的浆细胞肿瘤免疫表型异常以及在浆细胞样群体中缺乏CD138表达。LEF1表达和缺乏MYD88 L265P突变有助于区分具有浆细胞分化的CLL/SLL与LPL和其他B细胞淋巴瘤。
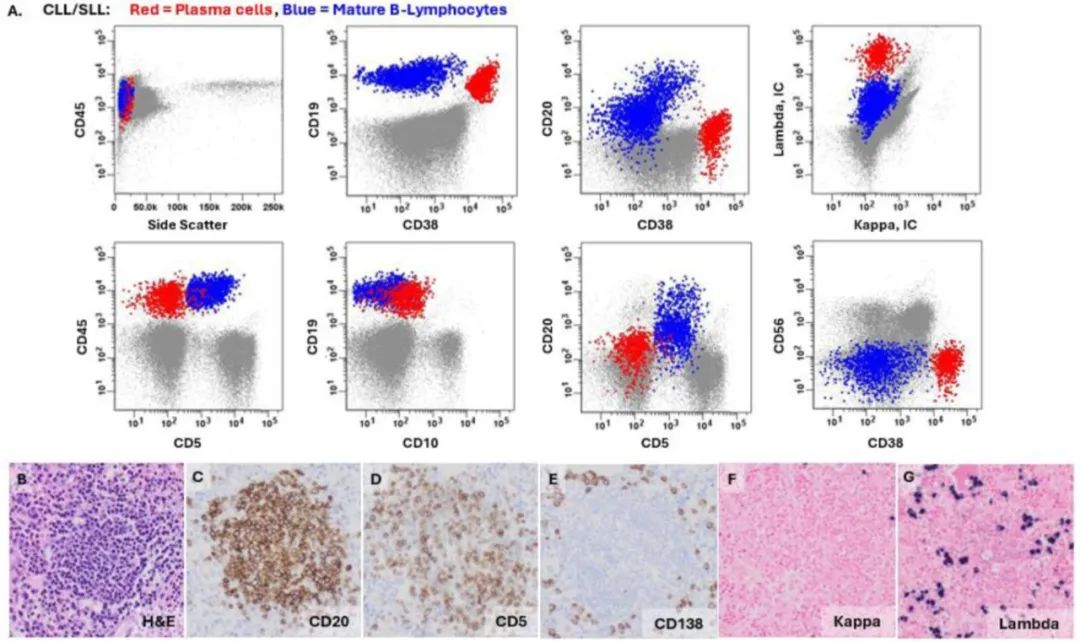
图6. 慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)骨髓中浆细胞分化。
A. 具有浆细胞分化的CLL/SLL及12号染色体三体;流式细胞术显示异常成熟B淋巴细胞(蓝色)和浆细胞(红色)的相关群体。成熟B淋巴细胞表现为:CD5(+)、CD10(-)、CD19(+)、CD20(弱阳性,强度不一)、CD38(部分弱阳性)、CD45(+)、CD56(-)、细胞质内λ轻链(+)。浆细胞表现为:CD5(-)、CD10(-)、CD19(+)、CD20(-)、CD38(强阳性)、CD45(+)、CD56(-)、细胞质内λ轻链(强阳性)。 B. 小淋巴细胞的结节状聚集,染色质聚集。 C. CD20阳性B淋巴细胞和CD20阴性浆细胞。 D. CD5阳性B淋巴细胞和CD5阴性浆细胞。 E. CD138阴性B淋巴细胞和CD138阳性浆细胞。 F. Kappa阴性(原位杂交)浆细胞。 G. Lambda限制性(原位杂交)浆细胞。
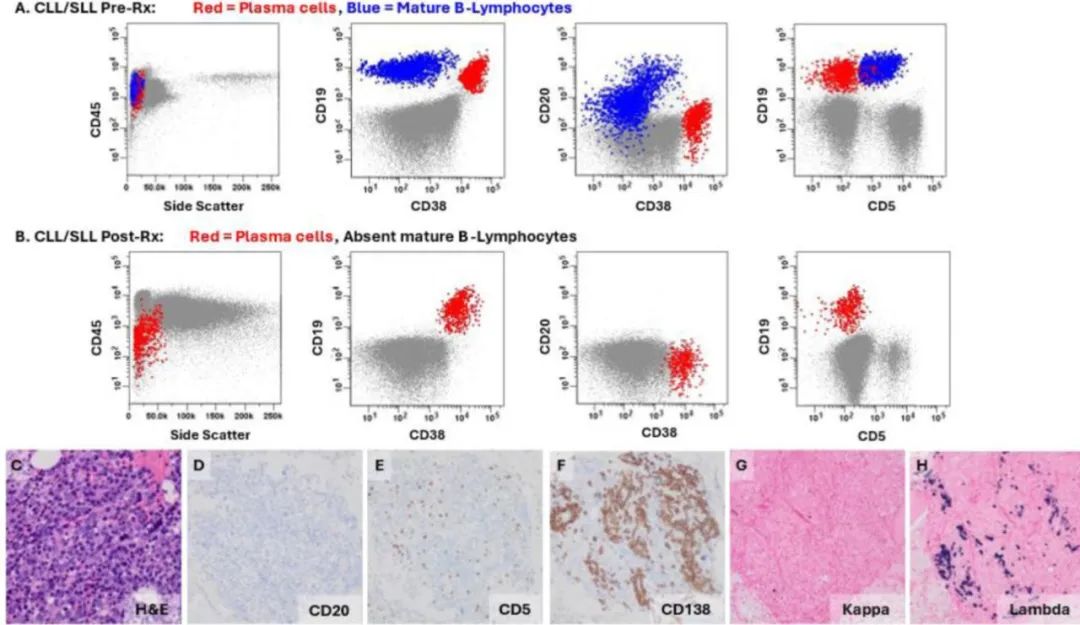
图7.慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)伴骨髓浆细胞分化,抗CD20单克隆抗体治疗后状态。
A.骨髓中具有浆细胞分化的CLL/SLL及12号染色体三体(摘自图6的部分流式细胞图)显示异常成熟B淋巴细胞(蓝色)和浆细胞(红色)的相关群体。
B.经利妥昔单抗(抗CD20)治疗后骨髓中具有浆细胞分化的CLL/SLL,显示成熟B淋巴细胞缺失,但肿瘤性浆细胞(红色)持续存在。
C.成熟浆细胞的散在聚集,背景为骨髓成分。
D. CD20阴性细胞。
E.散在的CD5阳性T淋巴细胞。
F. CD138阳性浆细胞。
G. Kappa阴性(原位杂交)浆细胞。
H. Lambda限制性(原位杂交)浆细胞。抗CD20治疗后,浆细胞成分中12号染色体三体持续存在。
滤泡性淋巴瘤
滤泡性淋巴瘤(FL)表现出浆细胞分化,以存在克隆相关的轻链限制性浆细胞样细胞为特征,这是一种罕见现象,占滤泡性淋巴瘤病例的不到5%。与正常的生发中心B细胞一样,FL B细胞可以表现出生发中心后成熟(浆细胞和记忆B细胞),下调生发中心标记物CD10和BCL6的表达。已经描述了两种具有浆细胞分化的滤泡性淋巴瘤。一种类型显示出典型的FL形态,具有t(14;18) IGH::BCL2,浆细胞在生发中心间区域分布;第二种类型显示出缺乏t(14;18) IGH::BCL2的FL,浆细胞分布在生发中心周围和生发中心内区域。在这种情况下,肿瘤性B淋巴细胞显示出生发中心标记物的可变表达,包括频繁缺乏CD10和保留BCL6表达。在存在BCL2重排的情况下,异常情况预计会出现在CD138阳性浆细胞和CD138阴性淋巴样细胞群体中。
在文献中描述的大多数病例中,主要群体为典型的滤泡性淋巴瘤的成熟淋巴细胞,以及一个较小的轻链限制性浆细胞亚群。在具有浆细胞分化的FL中,不太能出现典型的多发性骨髓瘤临床表现,而淋巴结疾病可预期出现。具有浆细胞分化的滤泡性淋巴瘤中的肿瘤性浆细胞应缺乏常见的多发性骨髓瘤异常(例如,CD19-、CD45-、CD56+)。有少数病例报告称,具有浆细胞分化的FL最初在初次髂嵴活检中呈现大量轻链限制性浆细胞,最初被误诊为浆细胞肿瘤,但最终在随后的淋巴结活检中显示出具有浆细胞分化的FL。
套细胞淋巴瘤
大多数MCL起源于定位在原始淋巴滤泡和含有t(11;14)(q13;q32) CCND1::IGH的B细胞套区的生发中心前幼稚B细胞。具有浆细胞分化的MCL在少数病例报告和小病例系列中有过报道。大多数病例表现出典型的MCL病理特征,例如肿瘤性小淋巴细胞累及淋巴结,呈现结节状和套区生长模式。在具有浆细胞分化的MCL中,克隆性浆细胞预计会出现在肿瘤结节内以及反应性生发中心内。淋巴瘤B细胞和浆细胞在克隆上相关,并且带有t(11;14)(q13;q32) CCND1::IGH。
治疗效应
在靶向治疗时代(例如,单克隆抗体、CAR-T、双特异性T细胞衔接剂等),当使用针对B细胞的药物时,尤其是在随访样本中,可能会出现诊断上的挑战。在接受如抗CD20(例如,利妥昔单抗、奥妥珠单抗等)治疗的具有浆细胞分化的B细胞淋巴瘤患者中,在初次诊断后,这些药物对浆细胞成分的作用可能有限(图7)。在随访中,样本可能仅显示出残留的肿瘤性、CD19(+)、轻链限制性浆细胞,这些浆细胞可能会模仿浆细胞肿瘤。为了做出准确的诊断,仔细回顾病史和免疫表型非常重要,特别是如果患者在接受初次诊断和治疗后成为您的新患者。这些浆细胞预计不会表现出如之前所述的多发性骨髓瘤中常见的异常生物标志物表达(图2)。
参考文献
Semin Diagn Pathol . 2025 Aug 7:150944. doi: 10.1016/j.semdp.2025.150944.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)