首页 > 医疗资讯/ 正文
溃疡性结肠炎(ulcerative colitis,UC)是炎症性肠病(IBD)中最常见的表型之一,以反复腹痛、黏液脓血便、体重下降及肠道外并发症为主要临床特征。近二十年来,其全球发病率与患病率持续攀升,我国亦不例外。传统“三步疗法”——5-氨基水杨酸、糖皮质激素、免疫抑制剂——虽可暂时缓解症状,但长期应用易诱发感染、骨髓抑制、肝肾功能损害等不良反应;生物制剂如抗TNF-α单抗又存在原发/继发失应答、高昂费用及潜在结核激活等瓶颈。更为棘手的是,现有药物几乎均以“全身免疫抑制”为核心,难以精准作用于病变肠段,导致疗效-安全窗狭窄。因此,开发能够特异性靶向病灶、调控关键免疫环节且毒副作用低的新型制剂,成为中西医消化界共同关注的焦点。
南京中医药大学“中药功效物质”团队长期致力于药食同源植物活性组分的研究,他们发现乌梅(Prunus mume,PM)自古被《本经》《本草纲目》载录“下气、止痢、厚肠胃”,却苦于其物质基础与作用机制晦暗不明。借助近年兴起的“植物源性类外泌体囊泡(extracellular vesicle-like particles,EVLPs)”技术,该团队首次从新鲜乌梅汁液中分离纯化获得PM-EVLPs,证实其可通过口服途径精准富集于发炎结肠,以miR159为关键效应分子,阻断巨噬细胞NEK7-NLRP3相互作用,从而选择性抑制NLRP3炎症小体活化,显著缓解DSS及TNBS两种经典小鼠结肠炎模型。论文2025年6月在线发表于《Journal of Nanobiotechnology》,为中医“果药同源”理念走向现代精准医学提供了坚实证据,也为临床UC治疗带来一条安全、高效、经济的新思路。

图1 论文首图
PM-EVLPs的表征与稳定性
PM-EVLPs的物理-化学表征显示其平均粒径约124 nm,Zeta电位−27 mV,透射电镜下呈典型茶托状双层膜结构,符合外泌体形态学标准。梯度离心后30%/45%蔗糖界面条带最致密,纳米颗粒跟踪分析(NTA)提示产率稳定、批间差异小。组分学层面,深度RNA-seq揭示miRNA占比最高,长度集中20 nt左右;蛋白组学发现其主要参与“单细胞过程”“嘌呤核苷代谢”等通路;脂质组学则检出二酰甘油、溶血卵磷脂及N-花生四烯酰甘氨酸等膜稳定成分。模拟胃肠液稳定性实验表明,PM-EVLPs在pH 2.0胃酸及pH 7.4肠液中静置4 h后粒径几乎不变,提示其可安全跨越胃肠道苛刻环境,为后续口服给药奠定剂型基础。
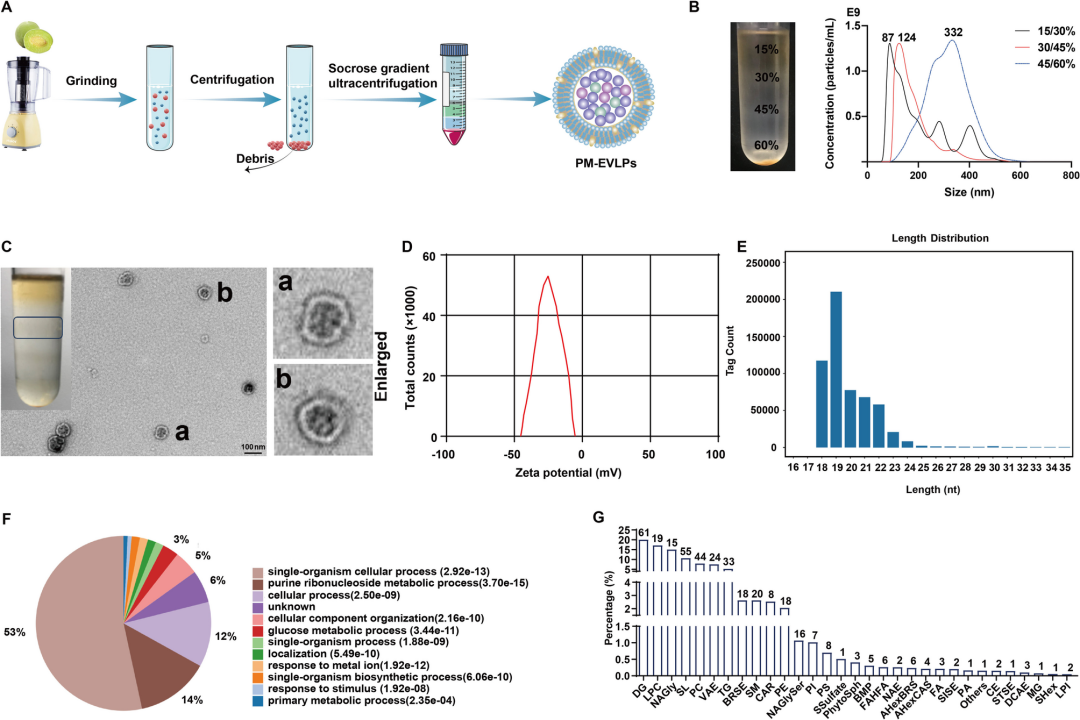
图2 PM-EVLPs的表征与稳定性
口服PM-EVLPs显著缓解小鼠结肠炎
药效学实验采用C57BL/6雌鼠2.8% DSS诱导的急性结肠炎模型。与模型组相比,口服PM-EVLPs(0.5或1.5×10¹⁰ particles/mL,每日1次,连续10 d)可显著抑制体重丢失、降低疾病活动指数(DAI)、逆转结肠缩短,并减少髓过氧化物酶(MPO)活性及组织病理评分;高剂量组疗效与200 mg/kg 5-ASA相当。镜下可见PM-EVLPs明显减轻黏膜溃疡、隐窝缺失及中性粒细胞浸润。为进一步验证普适性,研究者在BALB/c雄鼠TNBS模型上重复实验,发现PM-EVLPs将存活率由50%提升至80%,结肠大体及镜下损伤均显著改善,且雌雄鼠对制剂均无明显肝肾毒性及免疫器官异常,提示其安全窗宽。
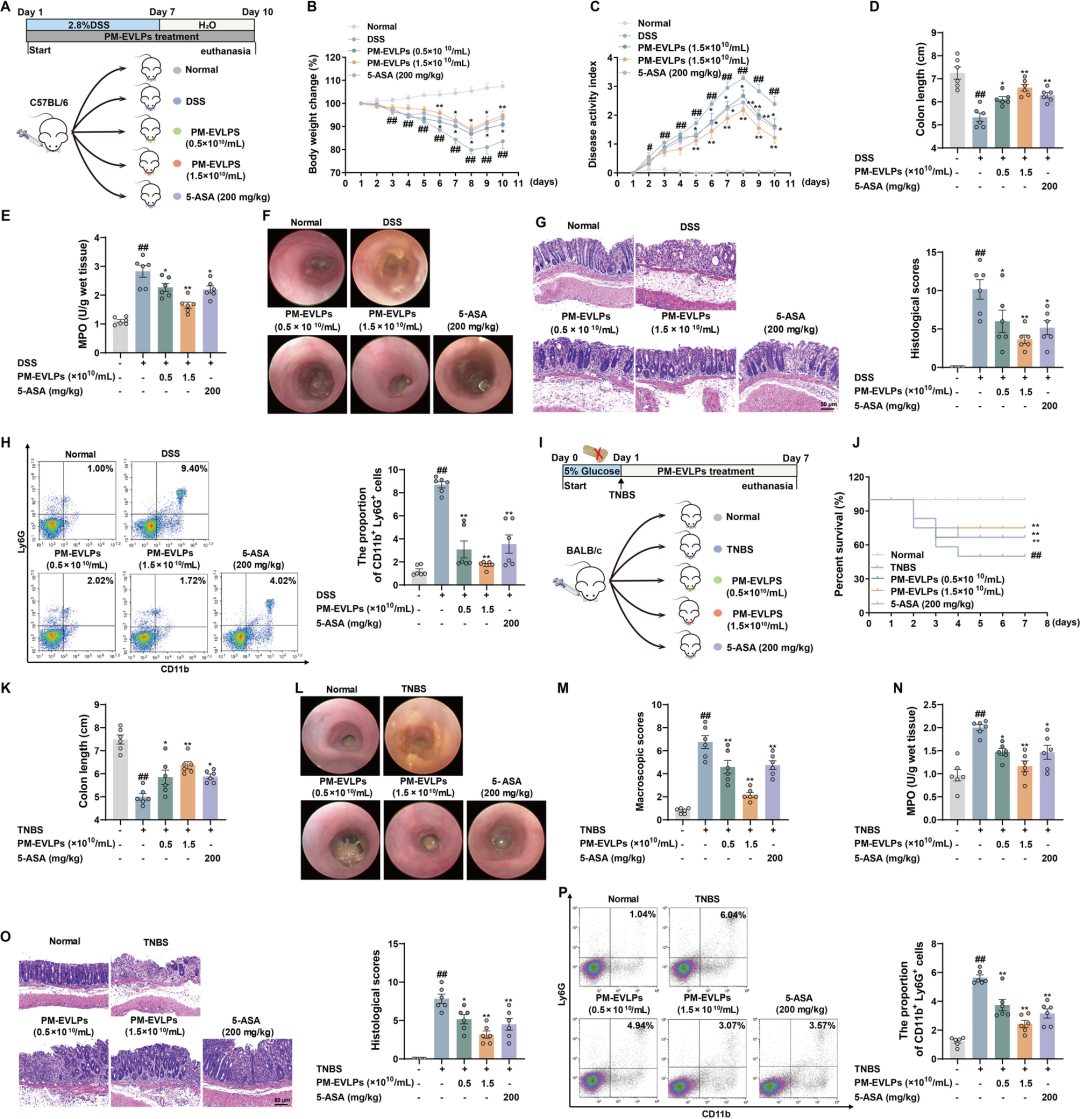
图3 口服PM-EVLPs显著缓解小鼠结肠炎
口服PM-EVLPs可靶向结肠巨噬细胞
靶向性是现代纳米药物的核心优势。团队利用近红外荧光探针DiR标记PM-EVLPs,经口灌胃后动态示踪发现:健康小鼠囊泡主要滞留于胃及小肠;而DSS结肠炎小鼠的炎症结肠在0.25 h即可见荧光信号,24 h达峰,48 h基本清除,说明PM-EVLPs能“主动寻靶”至病灶部位。分层免疫荧光进一步显示,DiR信号主要富集于黏膜固有层(lamina propria),该处恰为巨噬细胞、树突细胞及淋巴细胞聚集区。体外细胞摄取实验表明,无论是骨髓来源巨噬细胞(BMDMs)还是PMA诱导的THP-1巨噬细胞,对DiO标记PM-EVLPs的摄取率均显著高于CD4⁺或CD8⁺ T细胞;共聚焦成像亦证实口服后囊泡与F4/80⁺巨噬细胞高度共定位。上述结果首次揭示“植物外泌体-口服-巨噬细胞”这一跨物种递送路径的可行性。
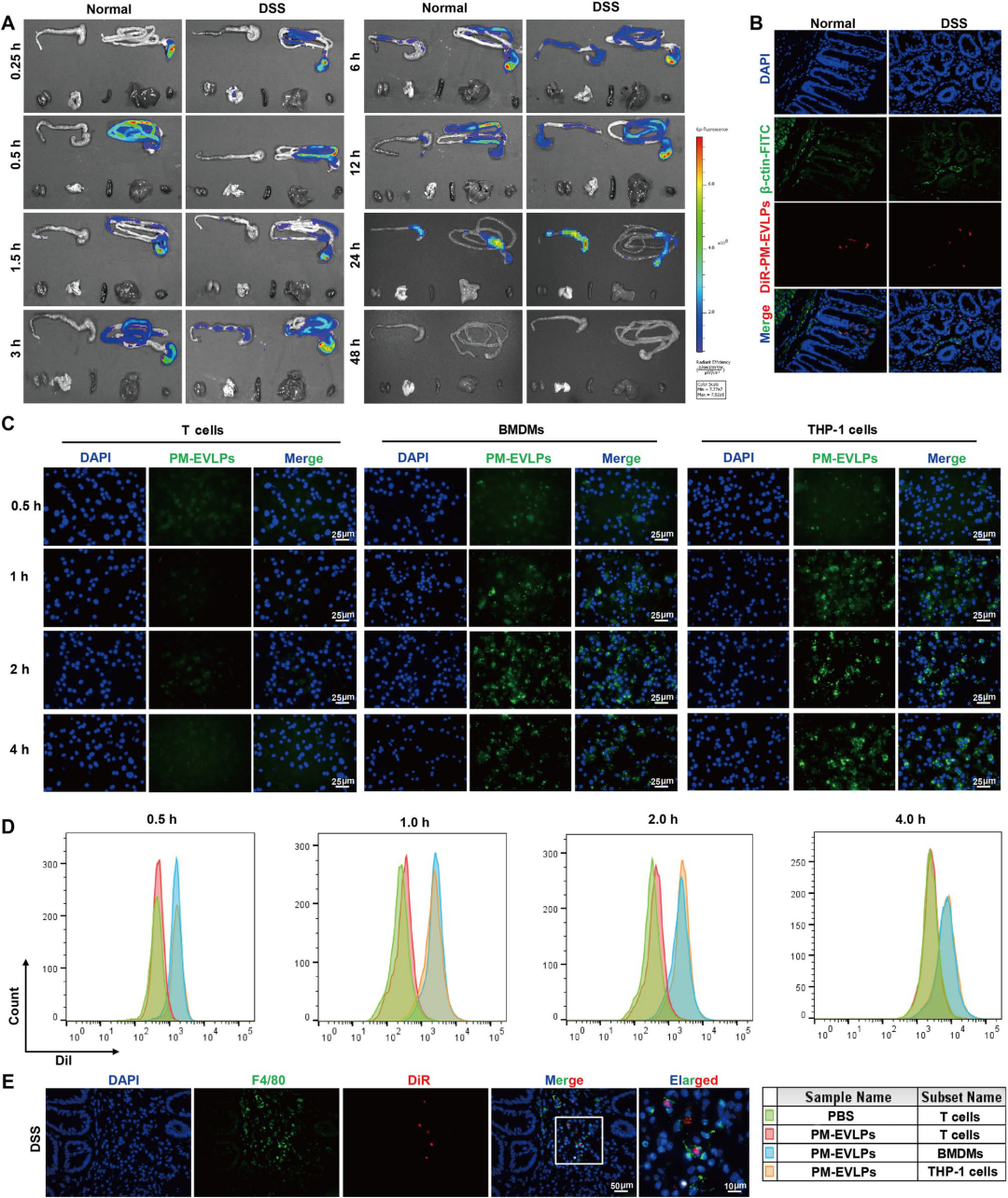
图4 口服PM-EVLPs可靶向结肠巨噬细胞
巨噬细胞是PM-EVLPs缓解结肠炎的关键细胞
为明确巨噬细胞的功能必要性,研究者在DSS及TNBS模型中预先腹腔注射氯膦酸二钠脂质体(clodronate liposomes)剔除巨噬细胞。结果显示,巨噬细胞耗竭后PM-EVLPs的抗炎优势几乎完全消失,DAI、结肠长度、MPO及病理评分均回到模型组水平;而对照脂质体组仍显著受益。该“loss-of-function”实验从正反两面锁定巨噬细胞是PM-EVLPs发挥抗结肠炎作用的唯一关键“执行者”,排除了其通过上皮细胞或淋巴细胞间接起效的可能。
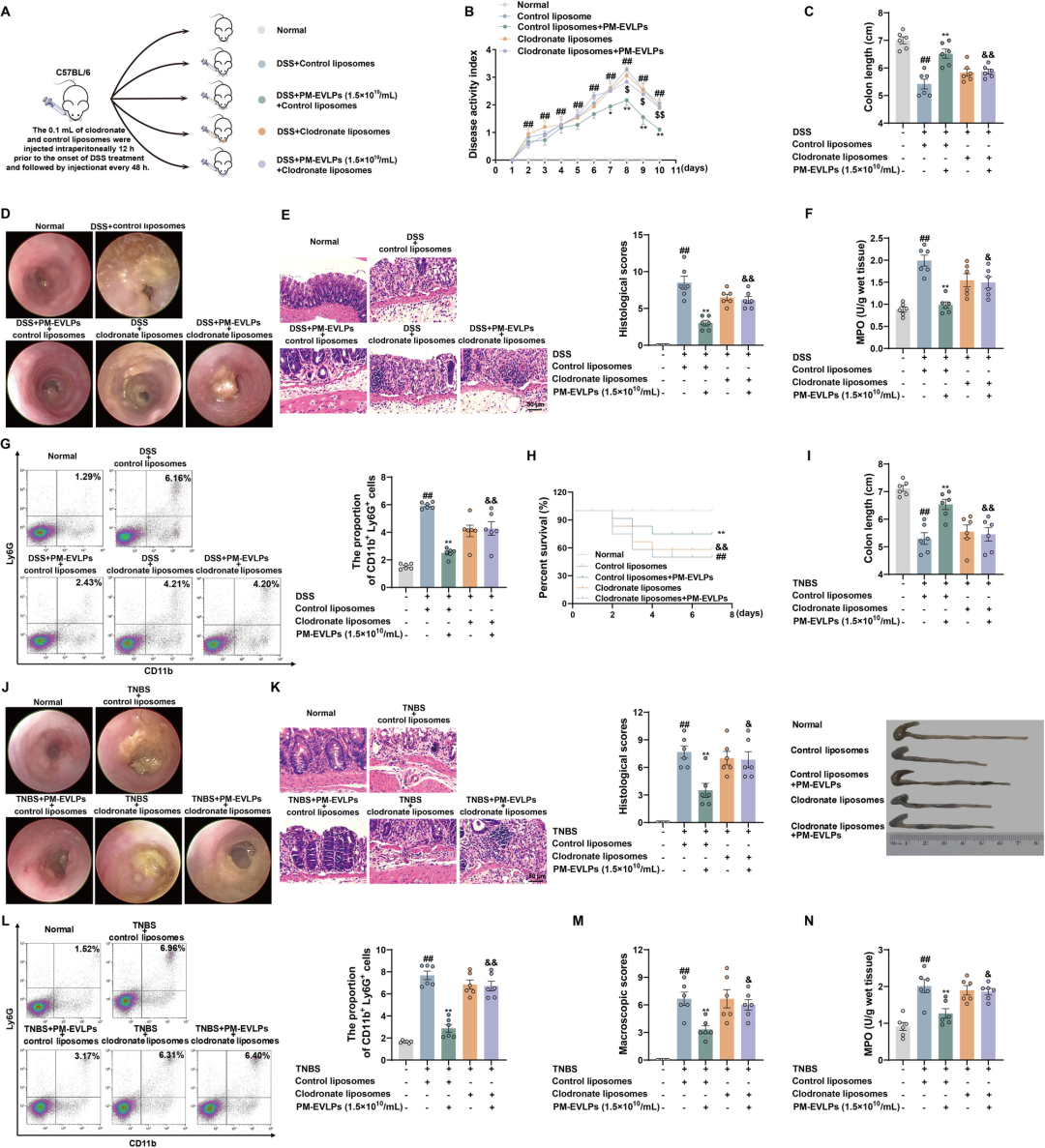
图5 巨噬细胞是PM-EVLPs缓解结肠炎的关键细胞
PM-EVLPs选择性抑制结肠巨噬细胞中NLRP3炎症小体的激活
机制层面,NLRP3炎症小体被公认为UC炎症级联的“点火器”。研究者首先分离结肠炎小鼠结肠原代巨噬细胞与上皮细胞,发现PM-EVLPs仅在前者显著降低caspase-1 p20、IL-1β及IL-18的蛋白水平,而对后者无明显影响,提示细胞选择性。进一步在BMDMs与THP-1细胞模型中,PM-EVLPs可浓度依赖地抑制ATP、Nigericin及单钠尿酸盐(MSU)诱导的NLRP3炎症小体激活,却不影响AIM2、NLRP1或NLRC4等其它类型炎症小体,表明其具有“亚型专一性”。值得注意的是,PM-EVLPs并不影响LPS触发的NF-κB核转位及NLRP3转录上调,也不改变线粒体ROS、K⁺外流或Ca²⁺内流等上游第二信号,说明其直接作用于“炎症小体组装”环节。
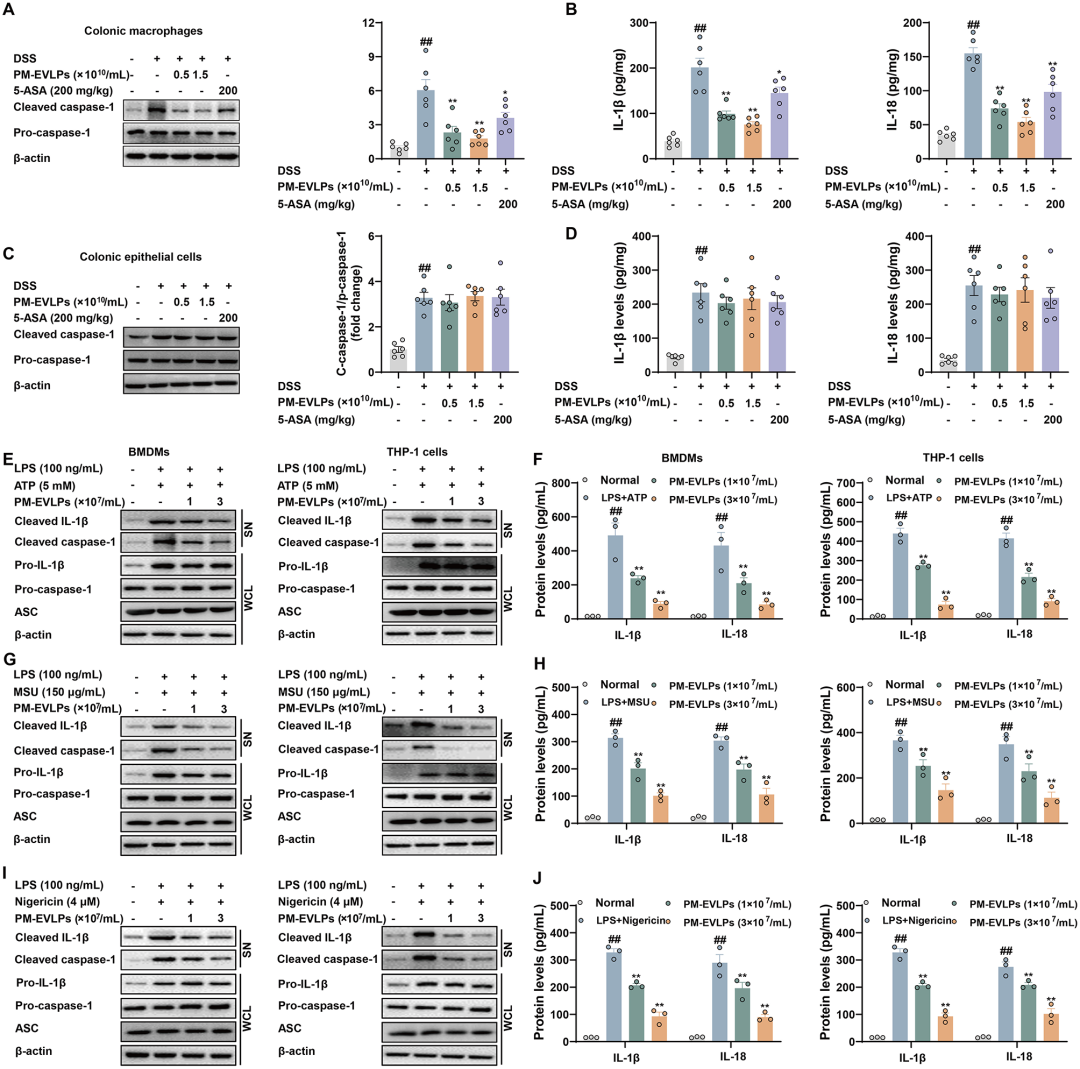
图6 PM-EVLPs选择性抑制结肠巨噬细胞中NLRP3炎症小体的激活
PM-EVLPs阻断NEK7-NLRP3相互作用,干扰NLRP3炎症小体组装
NLRP3炎症小体组装的关键节点是NEK7蛋白与NLRP3寡聚化。通过免疫共沉淀、邻位连接(PLA)及双分子荧光互补(BiFC)三重技术,研究者观察到PM-EVLPs可显著削弱NEK7-NLRP3相互作用,阻断NLRP3-ASC-pro-caspase-1复合物形成;而表面等离子共振(SPR)与CETSA实验排除了囊泡直接与NLRP3蛋白结合的可能。由此阐明PM-EVLPs通过“拆解”NEK7-NLRP3桥梁,使炎症小体“骨架”无法搭设,进而抑制caspase-1自剪切及下游IL-1β/IL-18释放。
接下来,团队采用“酶解-萃取-重组”策略锁定活性分子。蛋白酶的K消化、氯仿-甲醇脂质抽提均不能削弱PM-EVLPs的抑制活性,而DNase I/RNase A联合降解则完全取消其效应,提示RNA是核心功能单元。深度miRNA测序发现PM-EVLPs富含94条植物miRNA,其中miR159丰度最高。合成miR159 mimic(20–80 nmol/L)可重现PM-EVLPs对NLRP3炎症小体的全部抑制表型,且呈剂量依赖;而miR159 inhibitor可逆转PM-EVLPs的抗炎效应,确证miR159为“效应miRNA”。生物信息学预测显示,miR159可能与NEK7 3′UTR存在不完全互补位点,为后续“植物miRNA-哺乳动物靶基因”跨物种调控提供线索。
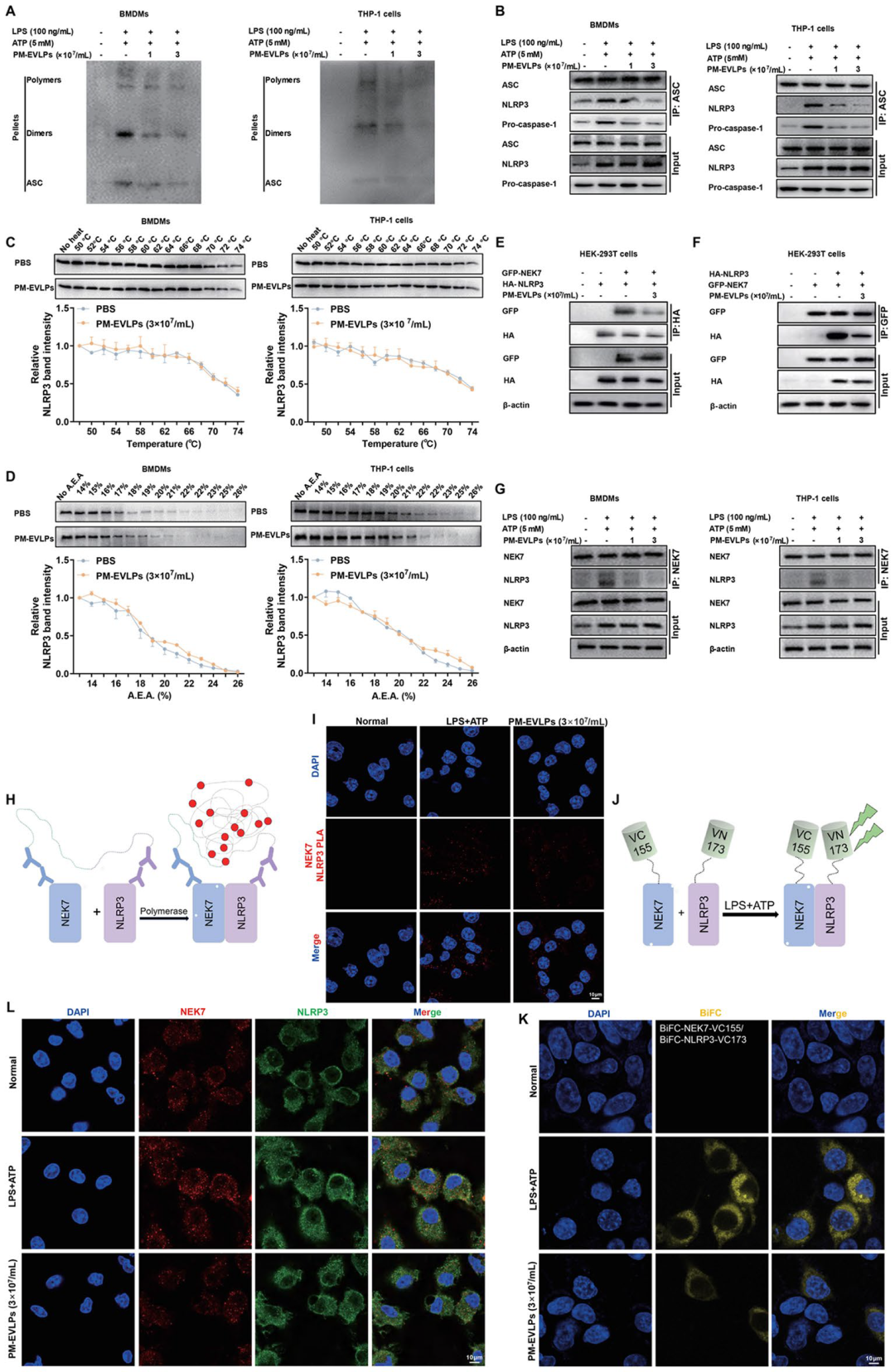
图7 PM-EVLPs阻断NEK7-NLRP3相互作用,干扰NLRP3炎症小体组装
miR159是PM-EVLPs缓解结肠炎的关键成分
最后,研究者在动物水平验证miR159的治疗价值。口服miR159 agomir(400、800 pmol/只,每日1次)可显著改善DSS及TNBS小鼠的体重、DAI、结肠长度、MPO及病理评分,疗效与完整囊泡相近,且高剂量组在降低中性粒细胞浸润方面更具优势。该结果不仅证实miR159是PM-EVLPs抗结肠炎的“最小活性单元”,也为开发“无载体、口服、核酸药”奠定概念基础。
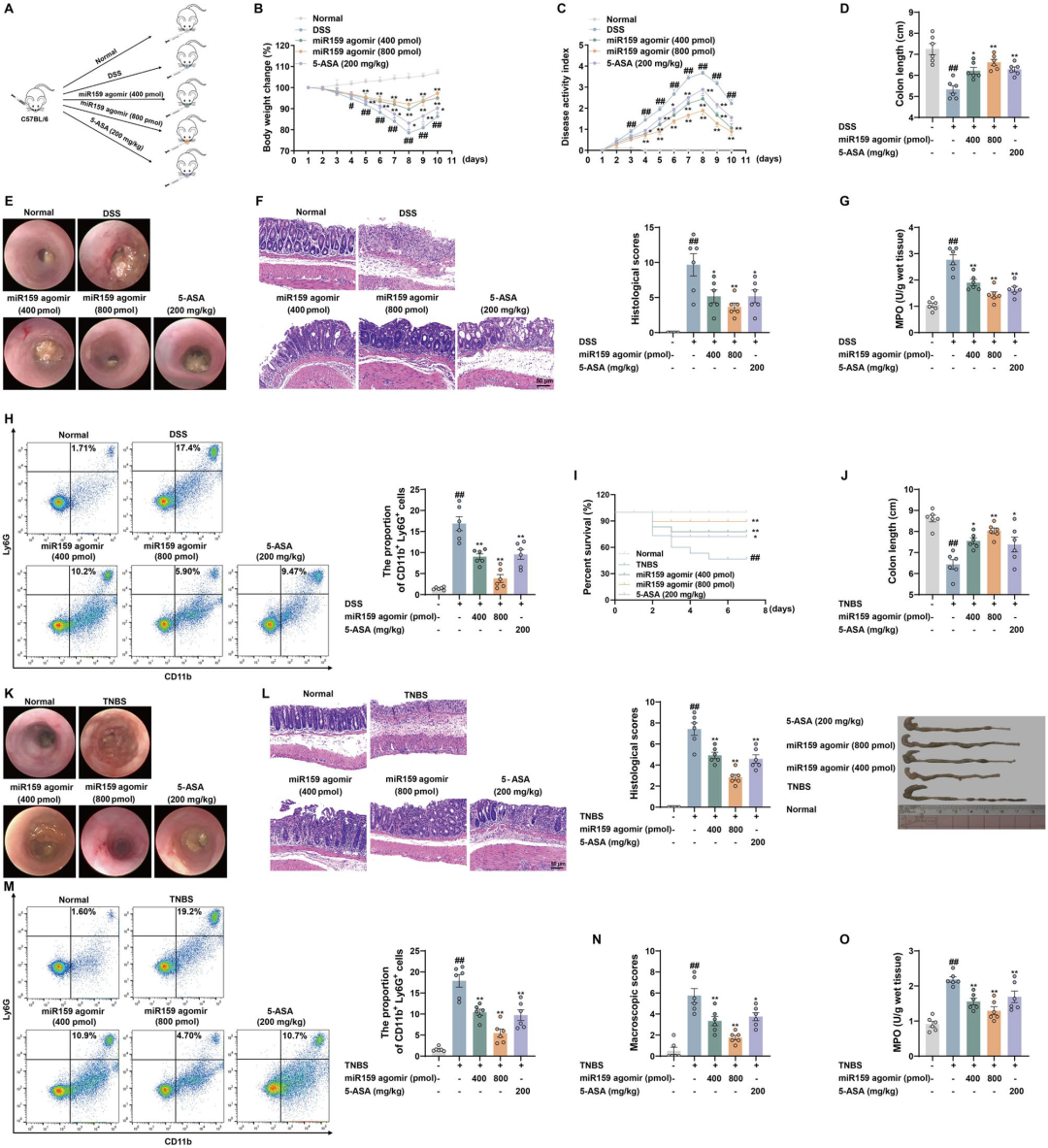
图8 miR159是PM-EVLPs缓解结肠炎的关键成分
小结
综上,该研究以“中医经典-现代外泌体-精准靶点”为主线,首次阐明青梅类外泌体囊泡通过miR159阻断巨噬细胞NEK7-NLRP3相互作用,选择性抑制NLRP3炎症小体,从而口服治疗溃疡性结肠炎的全新机制。其意义在于:①为药食同源植物“果药”开发提供示范,突破传统“提取-分离-纯化”难以富集活性组分的瓶颈;②利用可食用的天然纳米载体,实现核酸药物的口服靶向递送,规避合成材料潜在毒性;③从“炎症小体组装”这一更上游环节干预UC,克服现有IL-1β单抗“下游阻断”之不足;④发现植物miR159跨物种调控哺乳动物靶基因的新范式,为中医“食疗”赋予分子注释。
参考文献:
Lv Q, Yang H, Xie Y, Huang X, Yan Z, Lv Y, Cui Y, Hu L, Qiao H. Prunus mume derived extracellular vesicle-like particles alleviate experimental colitis via disrupting NEK7-NLRP3 interaction and inflammasome activation. J Nanobiotechnology. 2025 Jul 21;23(1):532. doi: 10.1186/s12951-025-03567-9. PMID: 40685348; PMCID: PMC12278495.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)