首页 > 医疗资讯/ 正文
焦虑状态降低个体暴露于危险环境几率,但这一适应性策略机制紊乱后,抑制饮食、环境探索等机体必要需求,因此适应性策略在平衡焦虑状态和竞争性需求状态中发挥关键作用,调控这一策略的机制尚不十分清楚。进食障碍和焦虑高度共患。动物研究证实瘦素可有效缓解焦虑症状,临床研究也表明其对神经性厌食症患者的多动与抑郁症状具有改善作用。外侧下丘脑(LH)表达瘦素受体的神经元(简称LH-LepR神经元)在调控摄食、饮水等机体基础需求中发挥关键作用。
2025年10月20日德国科隆大学Tatiana Korotkova团队在Nature Neuroscience杂志发表“A lateral hypothalamic neuronal population expressing leptin receptors counteracts anxiety to enable adaptive behavioral responses”文章揭示LH-LepR神经元可降低焦虑状态促进饮食等基本需求行为。

1 LH-LepR神经元在焦虑状态下缓解焦虑促进进食
利用在体光纤钙成像系统对十字高架实验中的小鼠进行实时记录,结果显示LH-LepR神经元的钙信号在开放臂区域的活性显著高于闭合臂区域。光激活或化学激活LH-LepR神经元均能显著增加小鼠在开放臂区域停留时间,化学激活这群神经元可增加在旷场实验中中心区域停留时间。反之,诱导 LH-LepR神经元凋亡减少在开放臂区域停留时间。
已有研究表明高焦虑状态小鼠摄食行为减少。在新奇抑制摄食实验(该实验范式通过将食物置于明亮的中心区域,使处于饥饿状态的小鼠面临进食本能与焦虑样情绪之间的冲突,其行为抉择为:要么克服焦虑进入中心区域获取食物,要么因无法对抗焦虑而滞留于安全的周边区域)中,小鼠的LH-LepR神经元存在功能异质性:其中一部分神经元对食物刺激作出响应,另一部分则对环境安全线索作出响应,分别编码冲突情境下的不同行为动机,食物刺激激活的神经元比例更高一些。
在高焦虑状态下小鼠并不会出现上述响应特征。在高焦虑小鼠中,成功进食前会先出现接近食物时LH-LepR神经元活性升高的现象,这种现象并不出现在低焦虑小鼠中。慢性激活LH-LepR神经元可阻断新奇抑制摄食实验中摄食减弱行为。
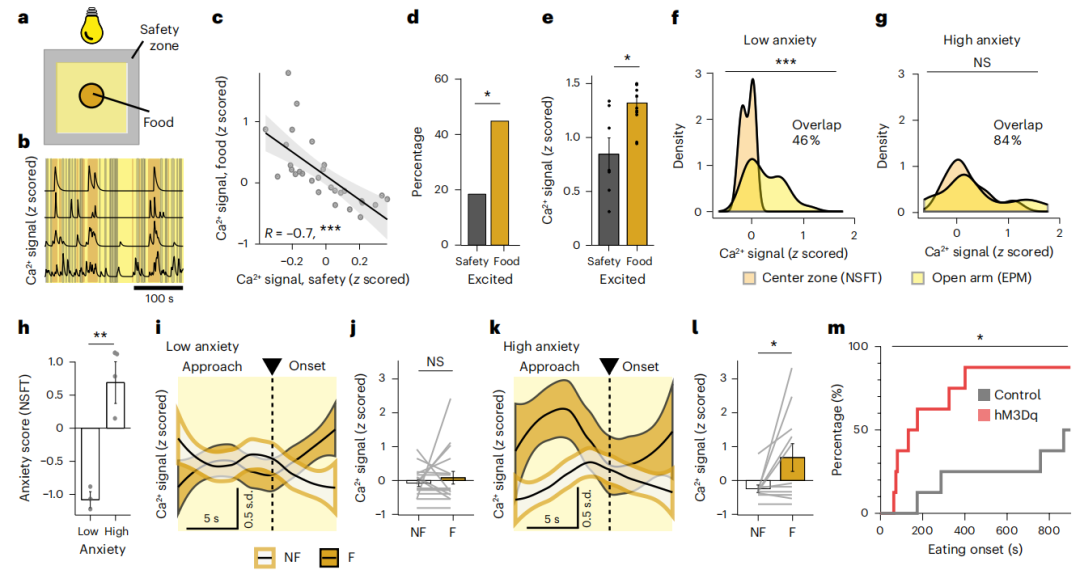
图1、LH-LepR神经元在焦虑状态下缓解焦虑促进进食
2 高焦虑状态下激活PFC→LH环路抑制LH-LepR神经元活性
前额叶皮层(PFC)神经元编码焦虑状态,并投射到LH,激活该环路可抑制摄食行为。此外,在摄食过程中该环路被抑制。光纤钙成像记录到在开放臂停留期间投射到LH脑区的PFC神经元钙离子活性显著增加。光激活PFC→LH环路后减少在开放臂的停留时间。离体脑片实验发现光激活PFC→LH环路后可减弱LH-LepR神经元钙离子活性。激活低焦虑状态小鼠PFC→LH环路不影响LH-LepR神经元钙离子活性,但在高焦虑状态小鼠激活该环路后减弱LH-LepR神经元钙离子活性。
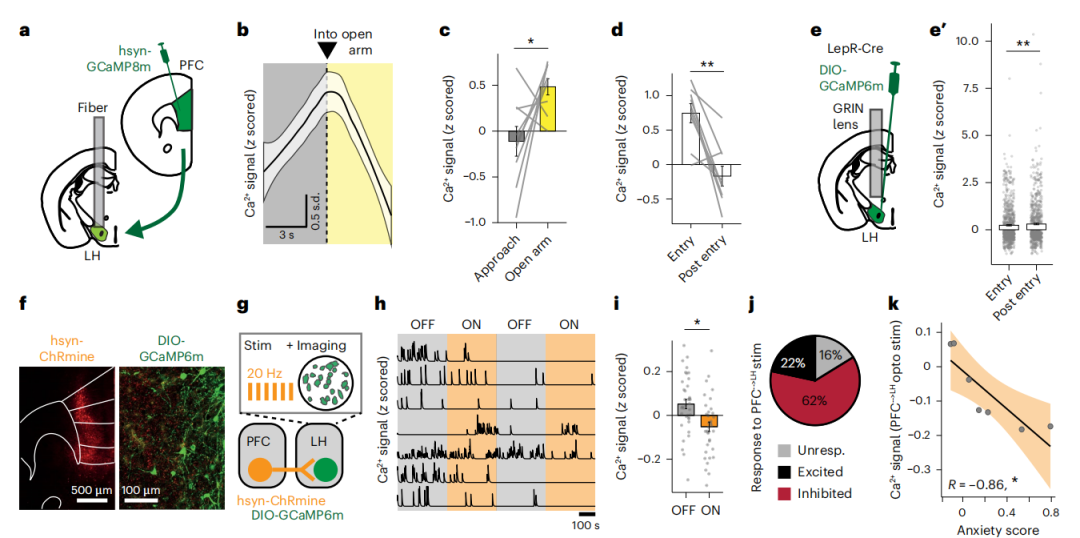
图2、高焦虑状态下激活PFC→LH环路抑制LH-LepR神经元活性
3 激活厌食症模型小鼠LH-LepR神经元建立适应性行为
运动厌食症模型小鼠出现过度活跃和焦虑状态,在靠近和接触食物时PFC→LH环路神经元钙离子活性显著增加,在进入跑步轮装置中活性降低。在自由进食阶段,食物与跑步所引发的LH-LepR神经元钙活性无显著差异;但在限制摄食阶段,跑步所激发的钙活性显著高于食物。与自由进食阶段相比,运动厌食症模型小鼠对跑步响应的LH-LepR神经元比例更高一些。此外,对跑步响应的LH-LepR神经元在低焦虑小鼠中比例更高,提示该类神经元与低焦虑状态相关。化学激活LH-LepR神经元后运动厌食症模型小鼠过度活跃与焦虑的不再存在关联。
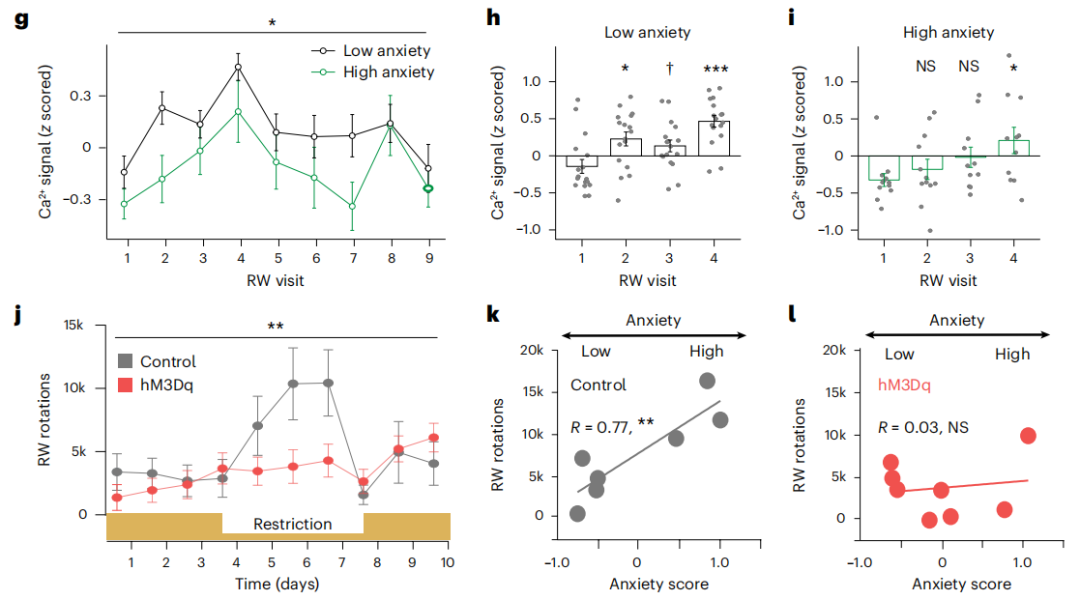
图3、激活厌食症模型小鼠LH-LepR神经元建立适应性行为
总结:
本文发现PFC→LH环路处理饱足状态与饥饿诱导的焦虑状态中的焦虑信息,并通过对抗焦虑驱动适应性行为,维持机体基本需求行为。
参考文献
https://doi.org/10.1038/s41593-025-02078-y
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)