首页 > 医疗资讯/ 正文
癌症是一种高度异质性的疾病,其发病机制复杂,涉及多种基因突变和蛋白质表达的异常。尽管近年来基因组学研究取得了显著进展,但仅依靠基因组学数据难以全面理解癌症的生物学特征和治疗靶点。蛋白质作为细胞功能的主要执行者,其表达和修饰状态直接反映了细胞的生理和病理状态。因此,蛋白质组学研究在癌症的诊断、治疗和预后评估中具有重要价值。
近年来,随着质谱技术的发展,蛋白质组学研究逐渐从单一癌种扩展到泛癌研究。泛癌蛋白质组学通过分析多种癌症类型的蛋白质表达谱,揭示不同癌症之间的共性和差异,为癌症的分类、诊断和治疗提供了新的视角。然而,目前大多数泛癌蛋白质组学研究仍集中在少数几种癌症类型上,缺乏对多种癌症类型的全面分析。
近日,国际权威期刊Cancer Cell上在线发表了题为“The pan-cancer proteome atlas, a mass spectrometry-based landscape for discovering tumor biology, biomarkers, and therapeutic targets”的最新研究成果,该研究通过高通量DIA-MS技术建立了覆盖22种癌症的Pan-Cancer Proteome Atlas(TPCPA),系统分析了癌种间和同种癌症内的蛋白表达特征,识别出多个泛癌与特异性蛋白标志物、潜在靶点和亚型分类器,特别在结直肠癌的CMS亚型与免疫特征分析中展现出良好的临床应用前景,并通过在线平台对外开放了全部数据资源。

研究首先对所有样本进行了无监督聚类分析,发现样本主要根据癌症类型聚集,且实体瘤和液体瘤之间存在明显分离。通过单样本基因集富集分析(ssGSEA),研究团队进一步验证了已知的癌症生物学特征,例如前列腺癌中的雄激素反应、乳腺癌中的雌激素反应以及肝癌中的代谢特征。此外,研究还发现了一些特定肿瘤类型中高表达的E3泛素连接酶,这些酶可能成为未来蛋白质降解靶向治疗的潜在靶点。
为了更深入地理解癌症的分子特征,研究团队应用了加权基因共表达网络分析(WGCNA),识别了13个与癌症生物学相关的蛋白质模块。这些模块涵盖了细胞黏附、免疫反应、代谢过程等多个方面。例如,模块5与结直肠癌的细胞黏附和糖基化过程密切相关,而模块6则与热休克蛋白和线粒体功能相关。这些模块的发现不仅揭示了癌症的共性特征,还为特定癌症类型的诊断和治疗提供了潜在的生物标志物和靶点。
在免疫浸润分析方面,研究团队利用ESTIMATE算法和ssGSEA分析了不同癌症类型的免疫细胞浸润情况。结果显示,血液癌症和黑色素瘤等癌症类型具有较高的免疫细胞浸润水平,而前列腺癌、脑癌和卵巢癌则表现出较低的免疫细胞浸润。此外,研究还发现,结直肠癌的免疫亚型与共识分子亚型(CMS)之间存在显著关联,且免疫亚型的预后价值可能优于CMS亚型。
为了进一步验证蛋白质组学数据的临床应用价值,研究团队构建了一个基于75种蛋白质的癌症类型分类器,能够准确区分17种实体瘤的来源。该分类器在多个独立数据集上表现出良好的预测性能,为未知原发灶转移癌的诊断提供了新的工具。此外,研究团队还开发了一个基于52种蛋白质的结直肠癌CMS亚型分类器,能够在蛋白质组学水平上准确预测CMS亚型,为结直肠癌的精准治疗提供了新的依据。
综上所述,本研究通过构建泛癌蛋白质组学图谱,系统地分析了22种癌症类型的蛋白质表达谱,揭示了癌症的共性和特异性生物学特征。研究不仅发现了多个与癌症发生发展相关的蛋白质模块,还为癌症的诊断和治疗提供了潜在的生物标志物和靶点。此外,研究开发的癌症类型分类器和结直肠癌CMS亚型分类器在独立数据集上表现出良好的预测性能,为癌症的精准医学研究提供了新的工具和思路。未来,随着更多癌症类型的蛋白质组学数据的积累和技术的进一步发展,蛋白质组学有望在癌症的早期诊断、个性化治疗和预后评估中发挥更大的作用。
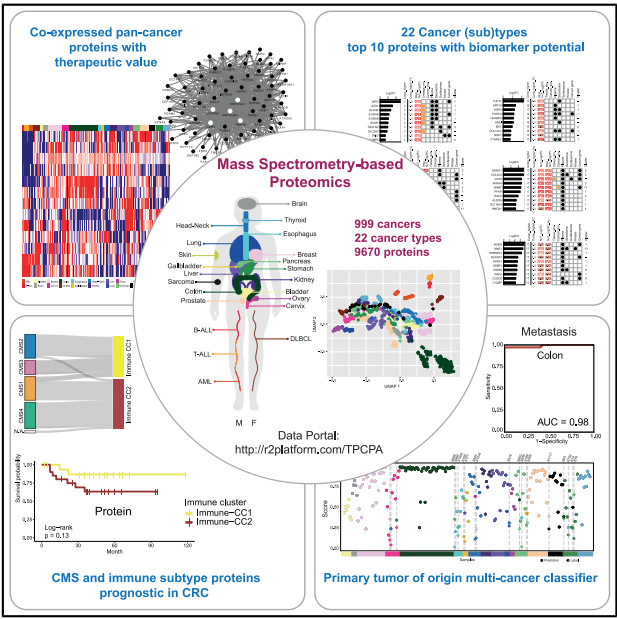
图 本研究模式图
原始出处:
Jaco C. Knol, et al. 2025. The pan-cancer proteome atlas, a mass spectrometry-based landscape for discovering tumor biology, biomarkers, and therapeutic targets. Cancer Cell.
猜你喜欢
- Immunity:中山大学邝栋明/魏瑗发现免疫检查点治疗引起的免疫球蛋白G抗体唾液酸化会损害肝细胞癌中抗原性I型干扰素的应答
- 你知道糖尿病对人身体会造成多大的危害和影响吗?糖尿病严重了会出现什么症状还能治好吗?
- 经常跑步真的能减肥吗?坚持跑步会带来哪些好处?
- NEJM:乳腺癌患者新希望!Inavolisib联合疗法,大幅提高PIK3CA突变患者的疗效
- 熬夜之后牙龈开始出血的原因是什么
- 五花八门的养生茶 不是每个人都能喝
- 四川省药品技术检查中心检查装备采购项目采购结果公告
- AM:上海药物研究所李亚平/尹琦联合构建个性化多表位纳米疫苗开启B细胞介导的多途径抗肿瘤免疫
- 为何乘客被困地铁两站之间? 事情的经过到底是怎样的
- 失眠也分真伪 遇到“伪失眠”怎么办
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)