首页 > 医疗资讯/ 正文
近期,中国科学技术大学研究团队在国际权威期刊 Science Advances 发表了一项重磅研究:发现传统中药“常山”中的活性成分常山酮(Halofuginone,HF)具有显著的抗肥胖作用,在动物实验中甚至超过了当下临床常用减肥药物利拉鲁肽(Liraglutide)的效果。这一发现不仅为解决肥胖这一全球重大公共健康难题提供了新的思路,也再次提示中药宝库中可能蕴藏着被现代科技低估的“分子金矿”。

常山,最早记载于《神农本草经》,在中医药中以治疗疟疾著称。其提取物常山酮(HF)是国际公认的抗原虫药,早已用于治疗疟疾、硬皮病、癌症等疾病的实验性治疗。但本项研究首次系统评估了HF对肥胖及代谢综合征的干预潜力。(见:Nature:中药常山活性成分常山酮halofuginone作用机制被揭示)(STM:科学家揭示中药常山抗疟机理)

研究显示,在饮食诱导性肥胖小鼠模型中,HF以显著剂量(100 μg/kg)连续干预后,使体重下降了高达22.3%,相比之下,利拉鲁肽的对照组仅为15.96%。更为重要的是,HF能够减少脂肪含量的同时,不显著影响肌肉质量,这一优势在目前多种抗肥胖药中尚属罕见。
这项研究显示,HF在多种动物模型中都展现出了强大的减重效果。对饮食诱导的肥胖小鼠,HF能显著抑制食物摄入,增加能量消耗,并最终导致体重减轻。在最高剂量(100 μg/kg)下,小鼠体重相比对照组减少了惊人的22.3% ,这甚至超过了阳性对照药物利拉鲁肽的15.96%减重效果。即使在较低剂量(25和50 μg/kg)下,HF也表现出显著的减重作用。

有意思的是,HF还能减少总脂肪量而不影响肌肉量,并有效减轻脂肪组织(如腹股沟白色脂肪组织iWAT和附睾白色脂肪组织eWAT)的重量和脂肪细胞的大小。除了直接减重,HF还改善了胰岛素抵抗和肝脂肪变性(脂肪肝),它显著降低了血清甘油三酯和总胆固醇水平,并改善了葡萄糖耐受和胰岛素敏感性。
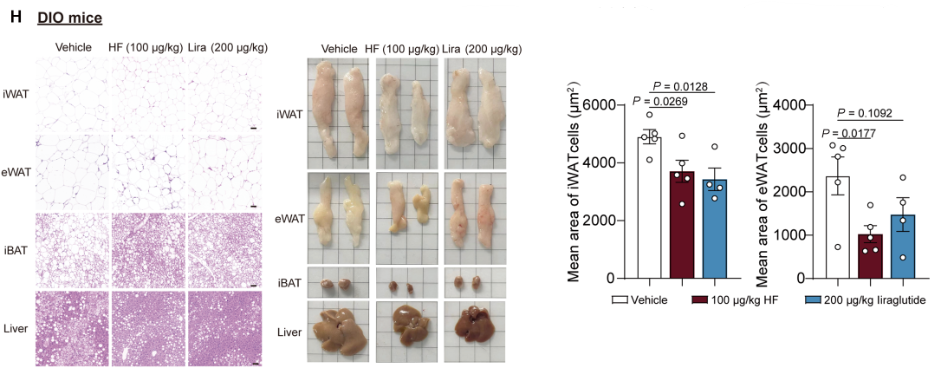
常山酮HF减肥背后的双重机制:抑制食欲与加速燃烧。
在抑制食欲方面,HF能显著降低小鼠的累积食物摄入量,即使在快速再喂食实验中也有效抑制了食物摄入。有趣的是,在瘦小鼠中,HF主要通过抑制食物摄入发挥作用,对能量消耗没有显著影响。
在增加能量消耗方面,HF处理后,肥胖小鼠的能量消耗显著增加。在冷刺激下,HF处理的小鼠体温维持在较高水平;促进棕色脂肪组织活化:HF上调了肩胛间棕色脂肪组织iBAT中解偶联蛋白1的表达,UCP1是产热的关键蛋白;促进脂肪燃烧:呼吸交换率分析显示,HF促使身体将脂肪作为主要的能量来源。
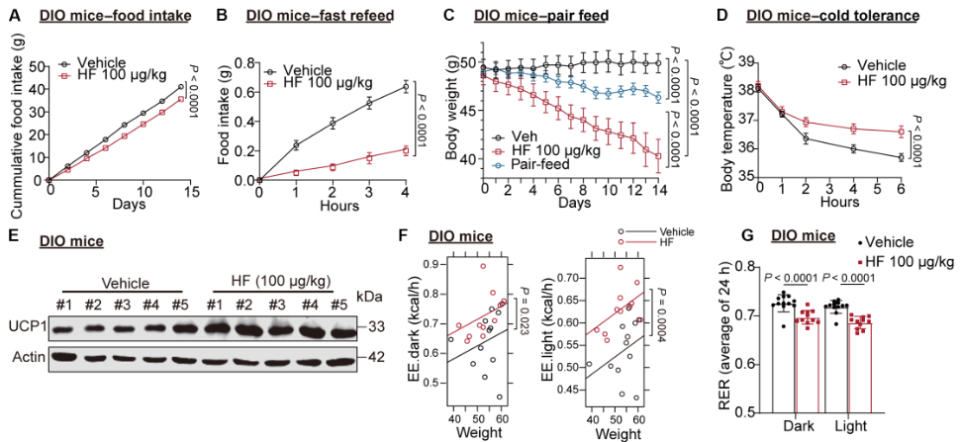
进一步研究发现,HF通过ISR通路,显著提升了两种关键的代谢激素:生长分化因子15(GDF15)和成纤维细胞生长因子21(FGF21)的水平。
ISR通路的激活是核心:HF抑制EPRS,导致非带电tRNA积累,进而激活氨基酸感应器GCN2,引起eIF2α磷酸化,最终增加激活转录因子4(ATF4)的表达。ATF4正是调节GDF15和FGF21表达的关键转录因子。急性HF治疗后,GDF15和FGF21的血清水平迅速升高,主要在肝脏中观察到它们的基因表达显著上调。进一步的研究揭示了GDF15和FGF21在HF介导的减重过程中各自扮演的独特角色。
在缺乏GDF15的基因敲除小鼠(Gdf15 KO)中,HF抑制食物摄入的能力完全丧失。同时,HF的减重和减脂效果也大打折扣。这表明GDF15是HF抑制食欲和减重效果的关键介质。在肝细胞特异性FGF21基因敲除小鼠(Fgf21hep−/−)中,HF对能量消耗的提升作用被抑制。虽然FGF21缺乏对HF抑制食物摄入的影响较小,但HF的减重效果也显著减弱 。这表明FGF21在HF促进能量消耗和体重减轻中发挥着重要作用。

该研究从分子机制层面揭示了HF的独特作用通路:
-
激活ISR通路(Integrated Stress Response):
-
HF抑制EPRS,诱导非带电tRNA积累 → 激活GCN2 → 磷酸化eIF2α → 上调ATF4;
-
ATF4作为关键转录因子,调控下游代谢激素 GDF15 与 FGF21 的表达。
-
-
GDF15:抑制食欲的核心因子
-
GDF15水平提升直接作用于食欲调节中枢;在Gdf15基因敲除小鼠中,HF几乎完全失效于抑制食物摄入。
-
-
FGF21:提升能量消耗的关键激素
-
FGF21促进脂肪氧化和产热能力,尤其在棕色脂肪组织中表现显著;其缺失显著削弱HF提升能量消耗和减肥的能力。
-
此外,HF还在猪模型和瘦小鼠中展现出代谢调节作用,提示其不依赖于肥胖状态,对多种代谢水平具有普适性调节潜力。
尽管结果令人振奋,但梅斯医学编辑认为,当前研究仍属于前临床的基础研究阶段,从动物模型到人体之间仍有漫长转化路径:
-
药物剂量与毒性窗需验证:虽然现阶段研究显示HF在推荐剂量下无明显器官毒性,但长期使用是否安全、剂量依赖性副作用仍待进一步系统验证;
-
药代动力学与人群异质性考量:HF在人体内的代谢方式、半衰期、靶点表达分布等尚不清楚,不能简单类比动物数据;
-
单体药物开发路径漫长:从发现活性化合物到完成临床前研究、I~III期临床试验,再到获批上市,周期往往在8-12年以上。
中药现代化的“范式样本”?
这项研究再次提醒人们,中药作为几千年积累的医学经验体系,蕴藏着大量尚未被充分利用的活性物质与靶向机制。梅斯医学认为,在大数据、人工智能、组学技术日益成熟的背景下,以现代科学手段系统解析中药活性成分,或将成为推动新药发现的重要“增量路径”。
政策与监管维度同样值得关注。当前FDA已宣布通过AI工具(如Elsa)加速临床试验审评流程,释放监管效率,未来中国NMPA也可能通过引入AI辅助药物研发、靶点识别与安全性审查,在源头推动中药现代化转化。例如,HF这类中药来源单体的临床价值评估可与AI辅助建模、真实世界数据验证等工具结合,形成高效率、低风险的转化通道。
常山酮是“中药分子宝藏”的冰山一角?
虽然常山酮HF离成为真正的抗肥胖新药还有不少距离,但这项研究提供了一个令人兴奋的方向:传统中药不是过时的经验包袱,而是未来精准医学与系统药理的宝藏资源。在AI、合成生物学与现代药理学交汇的新阶段,中西融合有望催生更多真正“以证据为基”的创新中药物质。
未来,我们期待HF或其优化衍生物真正走向临床,为攻克肥胖这一“慢病之母”提供全新武器,也期待更多“古老药材”在新工具体系下焕发出新的生命力。
参考资料:
The clinical antiprotozoal drug halofuginone promotesweight loss by elevating GDF15 and FGF21,Sci Adv .2025 Mar 28;11(13):eadt3142. doi: 10.1126/sciadv.adt3142
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)