首页 > 医疗资讯/ 正文
研究亮点
- 慢性肾脏病(CKD)显著增加心血管疾病(CVD)的发病风险和死亡率,尤其是心衰、冠心病和心律失常。
- 新兴药物如SGLT2抑制剂、非甾体类MRAs(如Finerenone)和GLP-1受体激动剂为CKD合并心血管疾病患者提供了重要的疗效支持,显著降低心血管事件和肾脏进展风险。
- 全面心血管风险管理需强调跨学科合作,早期筛查CKD、精准风险评估及个体化综合干预,提升患者生存率和生活质量。
研究概述
近日,发表在European Heart Journal一篇前沿综述文章,对慢性肾脏病与心血管疾病交叉领域进行了系统汇总与深入解析。本文由德国亚琛大学医院和加拿大多伦多综合医疗中心等多国专家团队合作完成,聚焦CKD患者心血管疾病的流行病学、发病机制、风险评估及最新治疗进展,强调了跨学科管理模式的重要性。文章内容涵盖了当前临床诊治中的挑战、指南推荐、关键临床试验数据及未来治疗展望,具备较高的临床指导价值。

研究背景与意义
CKD患者心血管疾病负担沉重,其发病率及死亡率远高于非CKD人群,表现为冠状动脉病变、心力衰竭、脑卒中及致命性心律失常等多种心血管并发症。伴随CKD病程进展,心血管风险不断累积,促进治疗难度增大。传统风险管理策略(如降压、降糖、降脂)虽有帮助,但部分患者仍存在高风险未被有效控制。原因之一在于CKD患者通常被排除在多数心血管大型临床试验之外,缺乏特异化循证依据。此外,CKD自身的代谢紊乱、炎症状态、矿物质代谢异常及尿毒症毒素积累,均加重心血管病理损伤,显示心肾交互作用的复杂性。本综述归纳了CKD患者CVD的病理机制及最新治疗证据,旨在为临床提供系统和科学的治疗建议。
方法学
作为一篇综述性“State of the Art”文章,本文基于国际权威指南、注册试验及高质量荟萃分析数据,结合多国大型队列研究、跨学科合作经验,充分整合现有CKD与CVD交叉领域的核心知识,无临床试验设计和实验方法细节。作者重点评述了关键临床试验和实践指南,形成系统的治疗策略框架。
主要研究内容与结果
1. CKD诊断与CVD风险预测
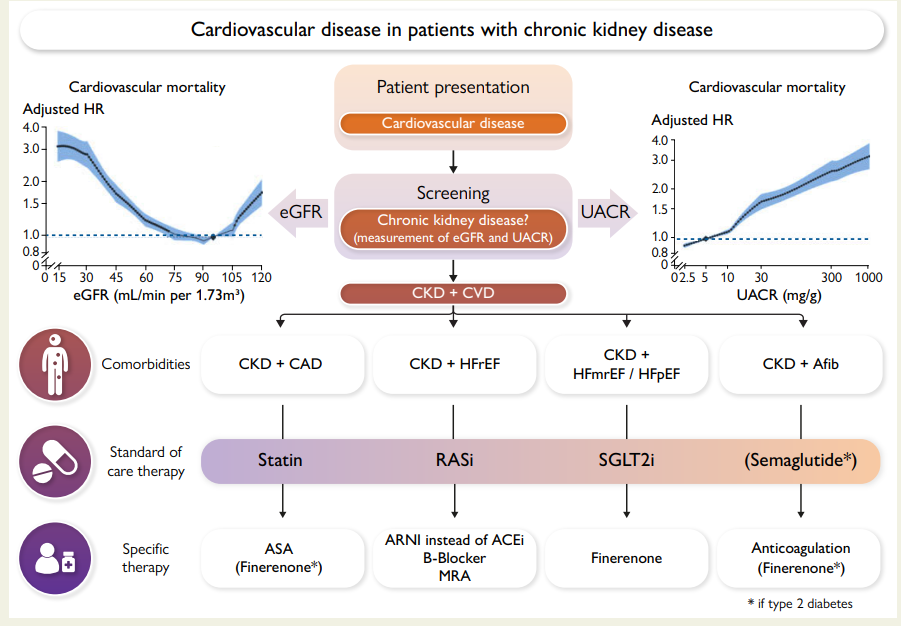
- CKD定义为肾功能或结构异常持续≥3个月。主要以估算肾小球滤过率(eGFR)及尿白蛋白-肌酐比(UACR)评估。
- eGFR≥60 ml/min/1.73m²时,如存在蛋白尿或结构改变,仍可确诊CKD。
- UACR升高与心血管及肾脏不良事件风险独立相关。
- CKD全球患病率达10-20%,主要病因包括糖尿病和高血压。
- CKD显著提升包括冠心病、中风、心衰、心律失常(特别是房颤)及猝死等多种CVD的发病率和死亡率。
- 最近的CKD预后联盟数据显示,eGFR下降及UACR升高均与心血管死亡和心衰风险密切相关(见Fig2)。
2. CKD与CVD的病理机制
- 传统风险因素如糖尿病、高血压广泛存在,驱动基础病变;CKD特殊因素包括慢性炎症、氧化应激、RAS激活、容量超负荷、尿毒素及矿物质代谢紊乱。
- 血管中,CKD促进平滑肌细胞转型导致血管和瓣膜钙化。
- 慢性炎症加重内皮功能障碍,促进动脉粥样硬化。
- 心脏则表现为纤维化和左室肥厚,构成尿毒症性心肌病。
- 这些机制共同加速CKD患者的心血管病变进展(见Fig3)。
3. 心血管风险评估工具的革新
- 传统风险模型(如SCORE2、美国Pooled Cohort Equation)未纳入CKD特异指标。
- 新开发的“CKD Add-on”工具和美国AHA的PREVENT模型,将eGFR和UACR加入风险评估,显著提升预测准确性。
- 例如,一位中年男性原估计10年心血管风险5.9%,如存在eGFR25及UACR500,风险升至23%。
4. CKD患者的心血管风险管理策略
4.1 传统风险因素管理
- 血压控制:现行指南推荐CKD患者SBP目标降至130 mmHg以下甚至120 mmHg以下,强调个体耐受性(参见2024年ESC和KDIGO指南)。
- 血糖控制:糖尿病CKD患者需个体化HbA1c控制,目标通常为6.5%-7.5%。
- 血脂管理:CKD期早期患者获益于他汀类药物降低LDL-C,血液透析期患者效果有限,PCSK9抑制剂显示安全性和有效性。
4.2 新型药物治疗
- Finerenone在糖尿病CKD患者中既具备心脏保护效果,也有显著肾脏获益(减少HF住院14%、肾组合终点23%)。
- Semaglutide在FLOW试验中证实其可降低肾衰和心血管事件,且表现出大幅的宏观蛋白尿改善。
- 目前多项研究正在探讨这些药物联合使用及在非糖尿病CKD患者中的疗效。
5. 特异性CVD疾病管理
冠心病(CAD)
- CKD患者ACS和CCS的药物治疗原则同非CKD患者,但药物剂量需根据肾功能调整。
- ISCHEMIA-CKD试验中,晚期CKD患者的介入治疗未显示死亡率或非致死性MI的显著获益,且伴随较高中风和透析率。
- 因此,CKD晚期患者的冠脉介入需严格评估风险/收益。
心力衰竭
- HFrEF治疗强调四大基石药物(ARNI/ACEI、β受体阻滞剂、MRA、SGLT2i),推荐尽早联合应用并密切监测。
- CKD晚期患者数据有限,建议根据耐受性个体化调整。
- HFpEF患者同样获益于SGLT2i,Finerenone表现出心衰事件减少潜力。
房颤
- CKD患者房颤明显增加卒中及出血风险,现行评分不足以完全反映风险。
- 维生素K拮抗剂在CKD 3期患者安全有效,但透析患者存在争议。
- DOACs在CKD中表现出更佳的疗效与安全性,但剂量需调整。
- 个别情况下可考虑左心耳封堵术。
讨论—研究价值与临床意义
本综述深刻揭示了慢性肾脏病与心血管疾病之间的复杂相互作用,明确CKD作为重大且独立的心血管风险因素的重要性。文章总结的临床试验数据不仅增强了心血管风险管理的循证基础,也为医生提供了合理用药的依据,尤其是在多病共存、病情复杂的CKD患者群体中。新兴药物如SGLT2i、Finerenone和GLP-1RA的引入,极大延展了治疗选择空间,标志着心肾协同治疗时代的来临。同时,文中强调的早期筛查、精准风险评估和跨学科合作管理,为临床路径优化提供了方向。未来,针对CKD不同分期患者的个体化治疗方案、安全性监测体系及复合治疗模式的完善,将进一步改善患者预后,降低心血管事件和肾功能恶化风险。
梅斯编辑点评
本篇综述文将慢性肾脏病患者的心血管疾病风险与管理进行了系统且深入的整合,充分呈现了心肾交互作用的病理机制与临床实践指导意义。新兴疗法的纳入,特别是Finerenone与GLP-1RA的推荐,开辟了治疗新篇章。对于临床工作者而言,文章提供了清晰的风险评估工具进阶路径,以及药物联合应用的最新证据。未来研究方向应聚焦于多药联合疗法的安全性研究,晚期CKD患者人群的专门临床试验设计,以及心肾综合管理模式在不同医疗体系的落地实践,进一步促进这一高危人群的预后改善。
原始出处
Matsushita K, Cherney DZI, Jankowski J, Matsushita K, Nardone M, Marx N, et al. Cardiovascular disease in chronic kidney disease. European Heart Journal (2025) 46(23):2148–2160. Published by Oxford University Press on behalf of the European Society of Cardiology. DOI: https://doi.org/10.1093/eurheartj/ehaf167
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)