首页 > 医疗资讯/ 正文
摘 要
近年来,随着介入技术的不断发展与成熟,先天性心脏病(先心病)介入治疗已逐步向县市级医院普及。同时,成人先心病(特别是卵圆孔未闭)的规范化管理以及复杂先心病的终身管理日益受到临床重视。新技术和新产品的涌现持续推动着学科的向前发展。本文旨在综述2024年度我国先心病介入治疗领域取得的新进展。重点回顾和分析了以下几个方面:(1)先心病介入封堵年度数据;(2)卵圆孔未闭封堵的最新认识;(3)经导管肺动脉瓣置换术进展;(4)复杂先心病介入治疗及终身管理策略;(5)获得性心脏病介入新技术;(6)人工智能在先心病管理中的应用。通过对上述内容的梳理与探讨,本文旨在细致剖析我国先心病介入治疗的现状,并展望其未来的发展方向。
正 文
先天性心脏病(先心病)介入治疗近年来随着技术发展,已逐渐在广大县市级医院开展普及。成人先心病尤其是卵圆孔未闭的规范化管理和复杂先心病的终身管理越来越受到重视,新技术和新产品不断发展,持续推动学科进步。本文就2024年度我国先心病介入治疗新进展着手,从先心病封堵年度统计、卵圆孔未闭封堵新认识、经导管肺动脉瓣置换进展、复杂先心病介入终身管理、获得性心脏病新技术、人工智能在先心病管理中的应用等方面细致剖析先心病介入治疗的现状与未来。
1 先天性心脏病介入封堵年度手术量
笔者汇总了10家封堵器厂商(美国雅培公司、北京华医圣杰公司、上海乐普心泰公司、深圳先健公司、徐州亚太公司、北京佰仁公司、上海普实公司、上海锦葵公司、威海维心公司、武汉唯柯公司)封堵器终端植入量,综合估计,2024年全国总体上先心病封堵器植入量约为13.2万枚,较2023年有所回落。主要细分病种中,房间隔缺损(atrial septal defect,ASD)封堵器植入量约5万枚,卵圆孔未闭(patent foramen ovale,PFO)封堵器植入量约5.4万枚,动脉导管未闭(patent ductus arteriosus,PDA)封堵器植入量约1.5万枚,室间隔缺损(ventricular septal defect,VSD)封堵器植入量约1.1万枚(表1)。ASD与PFO封堵仍然占比较高,接近80%,PDA和VSD封堵量也有不同程度增减。
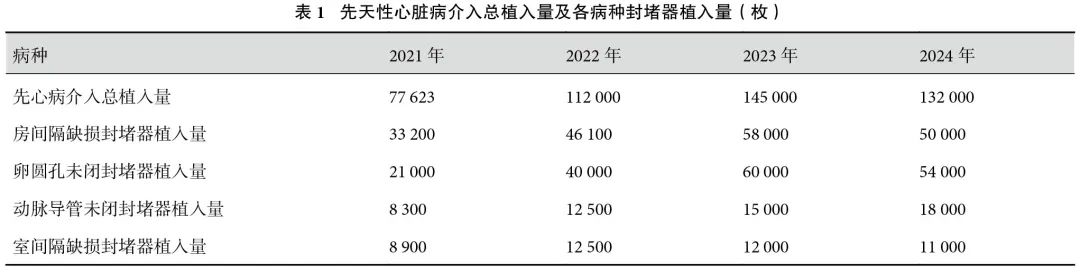
先心病介入封堵手术量今年以来的变化,分析原因可能与几方面因素有关:(1)随着产检的普及和优生优育的深入,先心病总发病率(尤其是复杂先心病)呈略微下降趋势,并带来了封堵手术量的变化;(2)超声检查经验技术的不断提高,使得小儿先心病的诊出和治疗年龄逐渐低龄化,婴幼儿期实施手术比例增加,导致更多低龄VSD因为介入风险而选择外科微创小切口手术,PDA封堵基本不受年龄限制,同时1岁以内干预率增加,导致二者植入量的不同变化;(3)先心病行业学会以及国家相关部门的规范化管理和干预,对于小ASD和PFO手术指征把控逐渐收紧,先心病术者对封堵时机把握更加规范和理性,减少了相当一部分超适应证手术情况,从而2024年尤其下半年ASD和PFO手术量降低。
可降解封堵器作为“介入无植入”的代表产品之一,是封堵器技术发展迭代的重要方向。自2022年起,国内可降解Memosorb VSD封堵器、Memosorb PFO封堵器、Memosorb ASD封堵器接连获国家药品监督管理局批准上市,累计植入量已>4 000例。欧美在可降解封堵器方面同样有所进展。Atheart Medical开发的reSept ASD可降解封堵器近期公布其首次人体研究的10年结果[1]:这款无金属、框架可吸收的封堵器显示出良好的长期安全性和有效性,进一步ASCENT ASD关键研究仍在进行中。在可降解封堵器的研发应用上我国在世界上居于领先地位,未来还将有多款可降解尤其是可降解PFO封堵器的应用,以解决金属封堵器植入后的长期痛点,但同时可降解封堵器自身也需密切关注降解不均匀、结构变形、残余漏等临床问题,而且可降解封堵器操作相对复杂、回收相对困难、出现并发症时处理困难大,应用安全性也是临床开展面临的首要问题。
2 卵圆孔未闭封堵新认识
PFO封堵手术量近年来高速增长,在所有先心病介入病种中稳居首位,但也已引起了行业担忧。据厂商官网公布数据,Amplatzer PFO封堵器自2016年美国食品药品监督管理局批准上市以来,累计植入量达到25万例,Gore Cardioform PFO封堵器自2018年上市以来累计植入量达到6.8万例,而中国近15年来累计完成19万例PFO介入封堵,近3年已达5万余例/年(绝大部分为国产化器械)。Goldsweig等[2]发现,从2006—2019年美国PFO封堵应用率已增长至6.6/10万人∙年(约2.2万人/年),在纳入的5 315例患者中,58.6%为卒中/栓塞,其余超适应证应用中,偏头痛仅占8.8%,≥60岁患者占29.2%;同时在历年手术量变化趋势中,仅有卒中/栓塞手术量持续增长,而偏头痛、短暂脑缺血发作(TIA)等指征基本无变化。在美国近半数PFO封堵患者为超适应证使用,而中国目前比例可能达80%,PFO规范化诊疗是亟待解决的问题。
最新临床指南/共识方面,2024年先后发布了《卵圆孔未闭相关非卒中性疾病防治中国专家共识》《卵圆孔未闭规范化诊疗中国专家共识》《ESC卒中委员会/EACVI/EHRA临床共识声明:来源不明的栓塞性卒中》《欧洲卒中组织ESO:卒中后卵圆孔未闭诊断和管理指南》[3-6],对于规范PFO诊治流程、规范超适应证应用有重要指导意义。指南强调了“PASCAL分类系统”及“高度临床相关性”对于判断适宜封堵人群的重要性,在临床实践中“心脏-卒中”团队对PFO相关卒中的管理和决策至关重要。
在PFO新型器械应用方面,国内已有4款产品上市、8款产品正在持续推进注册临床研究,技术方向覆盖了传统镍钛编织网塞封堵器(±无铆涂层)、金属骨架封堵器、可降解封堵器(部分/完全可降解)、直接缝合装置4个类型,在充分验证了PFO关闭的安全性和有效性后,未来将带来更多的临床选择,以适应不同患者、不同解剖特征、终身安全考虑等需求。
新型PFO封堵器的设计和临床应用过程中,对于残余分流的控制尤为重要。主流封堵器双盘腰部仅为细短连接杆,直径2~2.5 mm,无法完全填充卵圆孔隧道,其主要通过伞盘与房间隔的充分贴合和内皮化才能逐渐完成“封盖”效果。这一传统封堵器结构已有充足的临床数据证实,无论如何选择,完全封堵率(无右向左分流)仅约70%~80%,有效封堵率(无或少量右向左分流)仅86%~97%[7],仍有相当一部分患者在术后数年检查右心声学造影仍有大量右向左分流。残余分流形成的机制主要包括[8]:(1)当选择封堵器为小伞盘(如1825或1818)时,小伞盘无法覆盖宽口PFO,尤其是老年大型PFO(有文章称之为新月形ASD),使用小型号PFO伞会导致装置尺寸不匹配。PFO隧道的三维空间结构的尺寸中,通常仅在短轴或两房切面测的隧道的长度和高度,隧道宽度的测量往往未受重视,由于在二维食管超声无法直接获取,一般需3D食管超声或者光学相干断层扫描(OCT)中才能获得。因此隧道过宽的大量右向左分流者,尤其是合并房间隔膨出瘤或PFO原发隔活动度大时,可能不适合用小型号封堵器。(2)当选择封堵器为大伞盘(如2530、3030或2535)时,由于卵圆窝组织本身并不平整,且卵圆孔距离主动脉后方的平均距离仅9.1 mm,当封堵盘过大或距离主动脉过近时会出现贴壁不紧从而形成死腔,残留血流会通过伞盘与间隔之间的隧道形成穿梭分流,因此不合理使用大伞/尤其是大的对称伞,可能导致残余分流的增加。(3)其他机制包括:长隧道型在封堵后原发隔将伞盘角度蹩变形反而撑大了分流孔;继发隔肥厚导致伞形态扭曲或伞盘未夹在房间隔两侧;PFO本身为双出口或合并筛孔ASD结构;合并肺动静脉瘘;封堵器边缘对房间隔组织的磨损或糜烂形成再通等。基于此,新型封堵器在设计时或许应考虑腰部“堵塞”式封堵器以进一步提升封堵效果,包括腰部更大更软以在空间自适应性填充不同长度角度和宽度的隧道,额外的阻流促栓,以及避免疲劳断裂风险。
关于残余分流,2024年几个研究得出了一些值得关注的结论。一项来自北京宣武医院的研究[9],纳入247例患者,其中36.8%为复杂结构的PFO,结果发现简单PFO与复杂PFO中-重度残余分流率并无区别(6.4% vs 6.6%)。一项来自土耳其的研究[10],分析123例PFO封堵患者的资料发现,IVC-PFO隧道角度过小与残余RLS相关。一项来自土耳其的研究[11]:144例长隧道型、使用房间隔精准穿刺封堵长隧道型PFO显着降低残余分流率,术后6月仅1.4%。这让我们重新认识曾被摒弃的使用房间隔穿刺法进行PFO封堵。
通过OCT识别PFO原位血栓及内膜损伤是近几年来由中国学者率先发现的、确证PFO原位血栓学说的重要临床依据。2021年闫朝武等[12]通过OCT首次发现PFO隧道内原位血栓形成和内膜损伤机制。过去1年阜外医院[13]、复旦大学附属中山医院[14]、西安交通大学附属第一医院[15]、淄博市中心医院[16]等发现了原位血栓和内膜损伤在卒中以及偏头痛中的致病性因素。高分辨率OCT成像提高了对PFO解剖风险评估的理解。
PFO封堵术后卒中风险依然偏高。来自丹麦的全国多中心研究[17]发现,对 2008 —2021 年所有接受PFO封堵术患者(n=1 162)和年龄性别相匹配的普通人群对照队列(n=11 620)相比,4年缺血性卒中的绝对风险比普通人群高6倍(2.5% vs. 0.4%),调整后HR为6.3[95%CI(3.1,12.6)],与以往临床试验观察到的相当。但研究中纳入患者中77.2%的反常栓塞风险(risk of paradoxical embolism,RoPE)评分<7分,绝大多数集中在4~6分,考虑到RoPE评分过低时隐源性卒中可能与PFO无关,不能通过PFO封堵减少卒中复发,这一定程度上降低了研究结果的可靠性。考虑到隐源性卒中机制的复杂性,虽然半数以上归因于PFO相关卒中,仍需持续监测和充分筛查其他原因,尤其是隐匿性房颤,并密切关注器械表面/器械内血栓相关及残余漏相关卒中可能。
尽管过去指南中提到PFO相关卒中为年龄<60岁、无明确危险因素的年轻患者(RoPE评分>6分),但在≥60岁患者中,经过充分筛查评价,仍有相当一部分患者可能归因于PFO相关卒中,考虑到这部分人群的PFO往往为解剖高危,PFO封堵仍可能有临床获益。国外近年来密切关注≥60岁人群的PFO封堵适应性。加拿大多中心研究[18]纳入689例老年PFO封堵,复发卒中和TIA事件发生率分别为0.55次/100人年和0.63次/100人年,新发房颤发生率为3.3次/100人年,半数为术后1个月内,这些均不高于既往<60岁年轻患者的报道数据。同时,研究提示高龄、糖尿病、房间隔膨出瘤与上述事件风险增加有关。韩国多中心研究[19]共纳入437例患者,303例(69%)患有高危PFO,161例接受PFO封堵术,与276例药物治疗相比较。倾向评分匹配队列(130对)中,PFO封堵显著降低缺血性卒中或TIA复合风险(HR=0.45,P=0.012),未能降低缺血性卒中发生率(P=0.083)。高危PFO亚组队列(116对)中,PFO封堵显著降低缺血性卒中或TIA风险(HR=0.40,P=0.006),也降低缺血性卒中风险(HR=0.47,P=0.035)。德国多中心研究[20]纳入≥60岁患者143例接受PFO封堵,199例仅接受药物治疗。平均随访(5.5±1.5)年后,封堵组复发性卒中3例(2%),药物组11例(6%)(P=0.021)。两组新发房颤差异无统计学意义。麻省总医院研究[21]纳入741例PFO封堵患者中有184例(24.8%)年龄超过60岁,中位随访43.5个月,≥60岁与<60岁患者的卒中或TIA复发率无显著差异(4.3% vs. 2.3%,P=0.20)。缺血性神经系统事件及神经性死亡事件复合终点无差异。≥60岁组房颤发生率较高(7.6% vs. 2.7%,P=0.007)。加拿大魁北克心肺中心研究[22]纳入>60岁(n=388)和≤60岁(n=883)的PFO封堵患者,中位随访3年,老年组卒中/TIA/外周栓塞发生率为1.61次/100人年(卒中:0.59次/100人年),RoPE评分(4.6±1.1)分,2年TIA/卒中发生率为3.3%,低于RoPE评分预期的10.6%。年轻组复发率0.34次/100人年(卒中:0.09次/100人年),糖尿病和慢性肾脏疾病可能与TIA/卒中复发率高有关。
这些最新研究结果显示,PFO封堵指征应进行个体化临床评估,年龄并不是排除因素。与此同时,正在进行的两项随机对照研究CLOSE-2(NCT05387954)和STOP(NCT05907694)试验[23],比较了≥60岁隐源性卒中患者的药物治疗与PFO关闭治疗的效果。另一项正在进行的观察性研究COACH ESUS(NCT05238610),旨在比较PFO关闭治疗与药物治疗的疗效与安全性差异。DefenseElders(NCT04285918)观察性研究,旨在评估房颤对>60岁ESUS和高危PFO患者的临床影响,并将其与无高危PFO的类似患者进行比较。>60岁隐源性卒中患者能否从PFO封堵中获益,相信不久的将来会有定论。
术后房性心律失常(atrial arrhythmia,AA)发作一直都是PFO封堵安全性问题中备受关注的重点,Meta分析报道术后短期房颤发生率可达5.1%,因此带来的复发卒中风险尚不明确。最新发表的AFLOAT研究[24]由法国多中心所开展,PFO封堵后1∶1∶1随机接受标准护理、氟卡尼3个月、氟卡尼6个月组。观察植入式心内监测器记录≥30 s AA发生率。结果显示186例患者(平均年龄54岁,男性68.8%),6个月内53例(28.5%)患者发生AA(≥30 s),86.8%发生在第1个月,75.5%的AA事件≥6 min。AA中房颤占89.1%,房扑占4.9%,房速占6.0%。37例患者AA无症状,只有12例患者有症状。这与此前PFO-AF研究(NCT04926142)[25] 报道的数据相似。非治疗与治疗组在0~3个月AA发生率分别为25.4%、26.8%。三个组在3~6个月内AA发生率分别为7.9%、6.3%、5.0%,提示氟卡尼不能预防术后AA发作。另一项来自英国的研究[26],446例PFO封堵共获得48例植入式心内监测器的监测数据,其中男32例,平均年龄47岁,总体AA发病率为28.6%(14/48)。术后6个月,Amplatzer组5.0%(1/20)、Cardioform组46.4%(13/28)检测到AA(P<0.001)。所有心律失常发作均自限,21.4%(3/14)患者有症状需要治疗,首次发作时间为术后6(7~62)d,最后一次发作在术后118 d,每例患者平均发作2次,持续时间7 min至17 h。术后6个月后有3例检测到AA(均17个月后),早期晚期间隔2年。Cardioform封堵器AA发生率远高于其他封堵器,推测其原因与装置夹合力大、机械应力和组织刺激大有关。两项结果均显示,PFO封堵术后真实的AA发生于较以往超出5倍以上,但其仍然是自限性、绝大多数无症状,对患者长期影响有限。来自美国加州大学洛杉矶分校的研究[27]发现,445例PFO封堵患者中30例(6.7%)在6个月内发生房颤或房扑,在不同器械之间存在显著差异。Gore Cardioform的闭合后房颤或房扑事件发生率最高(16.8%)。使用Gore Cardioform装置、较大的装置尺寸和男性与封堵后房颤或房扑的风险更大有关。Cardioform装置虽然完全闭合率更高,房颤或房扑发生率也更高。这些也对PFO封堵装置的选择及未来新型封堵器的开发提出了新的要求。
3 经导管肺动脉瓣置换术新进展
经导管肺动脉瓣领域在球囊扩张瓣膜应用不断扩大的基础上,自膨胀瓣膜上市后也迎来了持续的推广和植入量增加。球囊扩张瓣膜Melody在全球累计植入量约1.8万例,Sapien全球累计植入量超过5 000例,并显示了远优于Melody的长期安全性和Native RVOT的适用性,Sapien瓣膜因其型号范围覆盖更大,自2019年起年植入量已逐步超过Melody瓣膜。根据 Schmidt[28]的报道,美敦力Harmony瓣膜全球植入量已超过1500枚,爱德华Alterra Prestent+Sapien瓣膜全球植入量超过850枚,而启明Venus P在欧盟CE MDR认证获批后全球植入量也已超过1500枚,其中中国大陆植入超过400枚。这些新产品的出现大大推动了这一技术进步和适应证拓展,同时临床研究的结果也促进了临床对于经导管肺动脉瓣置换术(TPVR)的一些新认识。
过去1年几款自膨胀瓣膜发表了其最新的临床研究数据。Harmony瓣膜在美国的多中心上市后研究[29]显示,共纳入243例Harmony植入患者,66%为跨环补片,91%使用TPV25,技术成功率99.6%(1例因压差大而再植入球囊扩张瓣膜),仅1例进行冠状动脉压迫试验,无瓣膜移位和围术期死亡。1年随访98%患者肺动脉瓣反流轻度或以内、100%患者瓣周漏轻度或以内,平均压差10 mm Hg。1年随访瓣膜相关心内膜炎6例(2%),2例再干预取出、2例死于血液感染。1年随访瓣膜相关血栓形成8例(3.4%,含1例支架断裂),其中4例再干预。19%的患者经历需处理的室性心律失常,单因素及多因素分析中只有术前为肺瓣狭窄与术后室性心律失常相关。ALTERRA瓣膜的关键注册试验(美国多中心研究)公布了其两年随访结果[30],共筛选了97例患者,其中60例成功接受手术,14例为肺动脉瓣狭窄(23%)。2例因反流植入瓣中瓣,仅1例接受分期手术(因回撤输送时支架移位)2个月后植入瓣膜。6例新发或三尖瓣反流恶化,与输送器有关。2年随访92.5%的患者瓣膜反流为轻度或以内,平均压差8.6 mm Hg。2年内无支架断裂、再干预、心内膜炎、取出、肺动脉损伤和死亡病例。1例医源性右心室流出道梗阻再干预、植入新支架和瓣膜。20%患者出现早期室性心动过速,2例(3%)出现早期装置相关血栓,后无其他患者再发,14例患者发生23处支架断裂,均为1型,无需干预。Venus P瓣膜也公布了其中国注册研究的5年随访结果[31],共纳入55例患者,54例植入成功。5年随访96%患者达到了主要终点(免于死亡和再干预),再干预2例(1例瓣膜移位、1例心内膜炎),均在术后1年内。死亡1例死于感染性心内膜炎,5例患者发生心内膜炎(4例在1年内,1例在5年内)。1例患者肺动脉瓣反流增加至中度,平均峰值压差维持16 mm Hg,跨瓣压差>30 mm Hg者术后1例、1年有2例、5年共4例,3例肺动脉瓣血栓/栓塞。从上述数据来看,与球囊扩张瓣膜不同的是,自膨胀瓣膜更低的冠状动脉压迫风险和球囊压迫试验需求,且中期随访感染性心内膜炎和再干预率发生率不高于球囊扩张瓣Sapien,然而自膨胀瓣膜面临有新的不良反应包括较高的术后早期室性心动过速发生率(与支架近端花冠刺激肌性流出道有关),且有装置相关血栓栓塞的风险,因此对于术后管理和药物治疗方面可能需要更多关注不良反应,而且这些新的证据在未来有望更新现行指南。
TPVR手术风险主要包括瓣膜移位、冠状动脉压迫、肺动脉损伤破裂等,随着技术的不断成熟发生率已不断降低。迄今为止最大样本量的研究[32],美国心脏病学会国家心血管数据登记处IMPACT(改善儿童和成人先心病治疗)收集了接受球囊扩张瓣膜TPVR患者的特征和结果。纳入2016年4月—2021年3月共4 513次TPVR手术,57%患者使用Melody,43%的患者使用Sapien。总体手术成功率95%,2.4%的患者发生主要心血管不良事件(死亡、心脏骤停、中转开胸、血管并发症、装置移位、冠状动脉压迫、管道破裂、机械辅助、起搏器)。先前为生物瓣的主要心血管不良事件发生率(1.4%)明显低于同种异体移植物(2.9%)或自体/修补后流出道患者(3.4%),单纯肺动脉瓣反流的不良事件率高于肺动脉瓣狭窄。Sapien管道破裂低于Melody(尤其是同种异体移植物中),瓣膜移位和中转开胸高于Melody,主要与自体/修补后流出道有关,血管并发症也更常见。40岁尤其65岁以上、紧急/急诊手术的不良事件更常见,尤其是管道破裂、心脏骤停、体外膜肺氧合(ECMO)和死亡。关于肺动脉置换的长期耐久性数据对比也有新的研究发表[33],丹麦国家患者登记处和EVITRA研究共纳入384例患者共进行了546次肺动脉瓣置换(463次外科肺动脉瓣置换和 83次TPVR)。肺动脉瓣生物瓣的中位耐久性为17年。植入10年后Perimount/Magna瓣膜的累计置换率为14%,同种移植物为20%,Melody/Sapien为29%,Contegra为47%。由于感染性心内膜炎,经导管肺动脉瓣比其他肺动脉人工瓣膜更常被再次更换。多变量模型中,肺动脉瓣手术时年龄较小和人工瓣真实内径较小与耐久性降低有关,均呈负相关。但调整这两种混杂因素后,不同瓣膜耐久性没有显著差异。
在TPVR解剖适应证方面,合并或不合并分支狭窄的短颈倒漏斗型(也称金字塔型)肺动脉,以及右室流出道及肺动脉全程瘤样扩张(>4 cm,甚至可达8~10 cm)的患者,仍旧被视为经导管肺动脉瓣技术解剖适应证的最后限制。美国埃默里大学医院开发了一项新技术来解决上述难题,即改良腔内裤腿支架辅助固定[34],共6例患者成功实施,手术通过对CUFF裤腿覆膜支架进行体外开窗后,将其远端植入于优势一侧的肺动脉分支内,再通过开窗进入另一侧非优势肺动脉分支植入球囊扩张覆膜支架完成分叉部位的铆定,最后在支架近端主肺动脉水平植入经导管肺动脉瓣膜。除此之外,此前还报道过一种远端植入于分支内的主肺动脉平行支架瓣膜技术以解决肺动脉瘤样扩张的固定难题[35]。这些创新技术均让此前已经历反复开胸的年轻患者有了实施介入治疗的机会,突破了经导管瓣膜设计的瓶颈,以满足各种复杂的、挑战的原生流出道解剖要求。
4 重视复杂先心病终身管理
以法洛四联症为代表的复杂先心病的终身管理受到了越来越多的重视,从新生儿或婴儿期因严重紫绀或肺动脉发育不良而实施的首次介入/外科姑息性手术,到婴幼儿或儿童时期的外科根治性手术(保留瓣膜修复或跨环补片),再到成年后出现右室流出道功能障碍及瓣膜反流等长期问题需要再次干预,法洛四联症等复杂先心病的患者始终面临反复多次手术的终身性管理问题。不仅在不同年龄段最佳手术方案的选择会影响长期疗效和生存率,同时根治性手术术式选择也会影响远期再手术率和再手术时间。Flores-Umanzor等[36]概述了所有年龄组法洛四联症患者的不同介入治疗方法,包括姑息性干预措施如婴儿和儿童的动脉导管未闭支架植入术、右心室流出道支架植入术、球囊肺动脉瓣成形术以及法洛四联症修复术后的成人TPVR。经导管介入治疗在患者的终身管理上发挥了重要作用,可作为传统开胸手术的替代方案,在降低手术风险、减少手术创伤和开胸次数等方面具有优势。美国心脏学会最新发布了科学声明[37],全面详细阐述了法洛四联症修复术后右室流出道功能障碍的评估和管理原则,在患者监测、风险分层、最新疗法与策略选择等方面上更新了证据,以为法洛四联症患者提供更好的终身管理和长期生存质量的获益。
先天性瓣膜疾病也面临严峻的反复多次手术终身管理问题。除法洛四联症、共同动脉干、肺动脉闭锁在内的肺动脉瓣疾患面临着长期瓣膜功能障碍管理的难题外,由于二叶式主动脉瓣的高发病率,相当一部分患者主动脉瓣功能障碍可早期出现,甚至婴幼儿时期即可出现严重症状而不得不及时手术。传统的手术方案包括外科主动脉瓣修复、介入球囊主动脉瓣成形、Ross手术、Ozaki手术,以及人工瓣膜材料包括带瓣管道、机械瓣和生物瓣的应用,需要根据患者年龄和解剖特点不同而量身定制修复和重建手术策略[38]。由于目前的植入物无法生长,导致需进行一系列的再手术直到可以安装成人尺寸的瓣膜植入物。因此,主动脉瓣修复或置换的终身管理倡导尽可能保留天然瓣膜的原则,同时手术方案需兼顾瓣膜的生长性,尽可能推迟人工瓣膜材料置换的需要直到晚年。近年来出现了部分心脏移植的概念和早期临床实践,即只移植包含瓣膜的心脏部分,由于活细胞存在允许移植物可以随年龄生长,并可能修复磨损。2024年部分心脏移植在杜克大学医学中心成功地进行了首例临床应用[39]并很快在美国多个中心开展,近中期结果显示移植物瓣膜表现出适应性生长和出色的功能。这一技术不仅可成为先天肺动脉瓣/主动脉瓣疾患儿童的有前景的治疗方式,可耐受缺血时间更长,也为废弃供心提供了一种新型应用途径,大大拓展了供体库,甚至可考虑进行多米诺部分心脏移植,即通过将心脏移植受体的心脏切除术制备瓣膜部分来进一步用于部分心脏移植,来解决供体竞争问题[40]。部分心脏移植的移植物保存时间和方式、受体免疫排斥等与整体心脏移植方案有很大不同,患者可能不会出现慢性排斥反应引起的心室功能障碍,因而仅需低水平的免疫抑制治疗,这些仍需要进行充分的临床探索。部分心脏移植为需要心脏瓣膜手术的新生儿和婴幼儿治疗开辟了新的前景,同时,进一步将适应证扩展至房室瓣修复、血管/补片修复肺动脉或肺静脉梗阻等也有望作为新的研究方向[41-42]。
此外,对于先天性体肺侧枝或各种异常血管瘘等疾病,血管栓塞材料的选择日渐丰富,尤其是国产化的带纤毛弹簧圈竞相上市,以及国外微血管塞新品的出现,临床应用治疗武器变得更加多样化,展现出百花齐放的态势。
5 获得性心脏病新技术
获得性结构性心脏病常见的包括人工瓣膜植入术后瓣周漏、心肌梗死后室间隔穿孔等,相对于常见先心病封堵而言,由于其往往位置特殊、缺损不规则,介入技术难度和风险更大,封堵后极易出现残余漏。一项来自土耳其的研究[43]纳入了335例外科换瓣术后瓣周漏的患者,300例(89.6%)为二尖瓣瓣周漏,35例(10.4%)为主动脉瓣瓣周漏。171例(51%)采取经导管封堵,164例(49%)采取再次手术修补。导管组和外科组的技术成功率(78.9% vs. 76.2%,P=0.549)和手术成功率(73.7% vs. 65.2%,P=0.093)相似,且成功率随时间和学习曲线逐年升高。随访结果显示,外科组住院死亡率明显高于介入组(15.9% vs. 4.7%),但长期死亡率无差异[HR=0.86,95%CI(0.59,1.25),P=0.435],显示了经导管封堵可作为外科手术风险相对较大患者的替代选择。另一项来自西班牙的研究[44]纳入90例患者,82例(91.1%)的瓣周漏程度减轻了至少1级,47例(52.2%)手术成功,达到术后瓣周残余漏≤1+级。慢性肾脏疾病、既往曾行瓣周漏手术和多发射流的存在与手术失败独立相关。中位随访3.2年后,手术失败与全因死亡、心血管死亡、心力衰竭再住院均显著相关。瓣周漏≤1+级的预后显著优于其他两组,瓣周漏减少≥1级但仍大于轻度的患者组与瓣周漏没有减少的患者组死亡率没有差异。此研究结果提示过去对于瓣周漏手术成功的定义可能需要改写,应尽可能将术后残余漏降至轻度或以下。
为解决瓣周漏形态、出口、入口和长度不规则的问题,美国埃默里大学医院报道了一种新型瓣周漏封堵技术,并命名为Tootsie Roll,即先在瓣周漏内植入覆膜支架,将不规则的漏变得相对规则,然后植入Amplatzer血管塞Ⅱ,同时封堵堵支架隧道的入口和出口。共有8例瓣周漏患者成功实施[45],其中主动脉瓣Sapien 3瓣膜植入术后3例,主动脉瓣Evolut Pro瓣膜术后1例,二尖瓣环钙化内球扩瓣植入术后2例,二尖瓣Sapien M3瓣膜植入术后2例。使用的覆膜支架型号包括有5 mm×2.5 cm、8 mm×2.5 cm、10 mm×5 cm的戈尔Viabahn支架,使用的血管塞型号为AVP Ⅱ 6~12 mm。所有患者都取得了技术上的成功,瓣周漏消除,无残留、无复发,无溶血等并发症。这一新技术显示了卓越的效果,有望能进一步推广实施。
心肌梗死后室间隔穿孔发病急、死亡率高,往往需要机械循环支持直至组织水肿消退后再实施手术,围术期管理和手术时机的把握对挽救患者生命至关重要,欧洲心脏学会及JACC工作小组研讨会均更新了室间隔穿孔的管理建议和共识[46-47]。美国埃默里大学医院开发了一项新型封堵技术Apical BASSINET Concept以解决封堵器贴靠不全、右室盘伸展受限带来的残余漏问题,即经剑突下入路杂交手术经导管修复室间隔穿孔[48],共7例患者成功完成(在心肌梗死后10~50 d进行),无术中死亡。1例术后死于多脏衰,1例残余漏术后9个月再次干预。与同期9例外科手术修复(在心肌梗死后10~134 d进行手术)的患者相比,4例患者出现多器官衰竭。两组均有1例患者需再次干预。杂交组在出院时(86% vs. 56%)和30d时(71% vs. 56%)的存活率较高,但在1年时的存活率相似(57% vs. 56%),显示经导管或杂交手术修复可作为传统手术替代方案。
6 人工智能应用先心病介入治疗
人工智能(AI)技术对心脏病成像产生了重大影响,并在医疗保健服务中有许多应用,如计算机辅助诊断、风险预测和分层、临床决策支持、深度表型、精准医学和个性化处方。当前的大数据时代为临床医生利用AI优化先天性心脏病儿童和成人患者的管理提供了丰富的新机会。但先心病异质性的临床表型和与年龄相关的病理生理变化复杂,特定罕见形式先心病的数据有限,建模需求较高,AI在先心病患者的诊断、预后和管理方面的临床应用仍然严重不足[49],需要制定特定病变的最佳个性化管理策略。AI应用的挑战与机遇并存,仍需不断开发新技术和合作以解决先心病数据集的复杂性和稀有性所带来的技术挑战,并采取战略举措促进基于AI的研究和临床应用。AI研究应包括纵向先心病数据,以绘制整个生命周期的疾病路径、生理学和预后图[50-51]。随着能够处理大数据的新型AI算法的出现,有大量的研究机会,如使用卷积神经网络和循环神经网络的深度学习、联合学习和数字孪生,建立预测模型为先心病患者开发新型治疗策略;可穿戴生物传感器可使儿科或先心病患者能够在家中进行持续、无创的生理和行为监测,允许患者访问其个人数据并监测其健康状况,在高危先心病人群中具有较大潜力[52]。
7 总结与展望
先心病介入治疗历经多年发展,已日趋成熟,但在解决现有诸多临床难题方面,对新器械和新技术的需求依然迫切。以降低残余漏为主要目标的创新性器械和技术发展迅速,不断取得突破性进展,不仅深化了对复杂病变解剖的理解,更带来了更优化合理的治疗选择和更优的临床预后。对先心病(特别是复杂类型及先天性瓣膜病)的终身管理理念日益受到重视,正在深刻改变着心外科的临床实践模式;其中,微创或杂交介入技术已成为降低患者再次外科手术痛苦和风险的重要替代策略。同时,可用于婴幼儿心脏瓣膜和血管修复重建的生物可降解/可生长材料的应用研究尚处于早期探索阶段。此外,“介入无植入”理念的推广应用以及自膨胀经导管肺动脉瓣等技术新临床证据不断涌现,正对先心病介入领域乃至整个心血管疾病治疗的临床实践和市场格局产生深远影响,并持续促进相关指南更新。可以预见,新产品和新技术将持续引领并推动先心病介入治疗领域学科向前发展。
利益冲突:无。
作者贡献:张长东撰写初稿;钟禹成、李庚、田军收集资料,整理数据;尚小珂提出设想,修改稿件。所有作者均同意稿件发表。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)